关于铁生锈的机理有人提出如下4个步骤:
①
②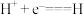
③
④
试根据以上过程回答下列问题。
(1)根据以上机理,判断下列说法正确的是_____ (填序号,下同)。
A.以上锈蚀过程发生的是化学腐蚀
B.从锈蚀反应的最终结果看,水既是氧化剂,又是还原剂
C.反应的实质是氧气被还原,金属铁被氧化
D.从反应机理看,锈蚀过程发生的是析氢腐蚀
(2)某铁件需长期浸于水下,为了减缓腐蚀,采取的下列措施正确的有_______ 。
A.给铁件铆上一些锌板
B.给铁件通入直流电,把铁件与电源正极连接
C.在制造铁件时,在铁中掺入一定比例的铜制成合金
D.在铁件表面涂上一层较厚的沥青
(3)质量为1000g的某铁件已在水下生锈,若已知整个锈蚀过程中有6mol电子发生转移,则参加反应的 在标准状况下的体积为
在标准状况下的体积为__ L。生锈后铁件的质量为__ g(已知铁锈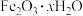 中x的值为1)。
中x的值为1)。
①

②
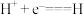
③

④

试根据以上过程回答下列问题。
(1)根据以上机理,判断下列说法正确的是
A.以上锈蚀过程发生的是化学腐蚀
B.从锈蚀反应的最终结果看,水既是氧化剂,又是还原剂
C.反应的实质是氧气被还原,金属铁被氧化
D.从反应机理看,锈蚀过程发生的是析氢腐蚀
(2)某铁件需长期浸于水下,为了减缓腐蚀,采取的下列措施正确的有
A.给铁件铆上一些锌板
B.给铁件通入直流电,把铁件与电源正极连接
C.在制造铁件时,在铁中掺入一定比例的铜制成合金
D.在铁件表面涂上一层较厚的沥青
(3)质量为1000g的某铁件已在水下生锈,若已知整个锈蚀过程中有6mol电子发生转移,则参加反应的
 在标准状况下的体积为
在标准状况下的体积为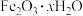 中x的值为1)。
中x的值为1)。
更新时间:2020-10-08 13:34:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】含氯化合物在日常生活中有多种用途,根据要求完成下列问题:
(1)漂白粉的有效成分是___________ ,家庭中使用漂白粉加水配置消毒液,与空气发生反应的化学方程式为___________ 。
(2)84消毒液的有效成分中NaClO中Cl的化合价为___________ ,请写出氯气与NaOH反应的化学方程式:___________ 。向NaOH溶液中通入11.2L(标准状况)氯气恰好完全反应生成三种含氯盐:0.7molNaCl、0.2molNaClO和X。则X是___________ 。
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为___________ ,被氧化的物质为___________ 。若反应中电子转移为2mol,生成的氯气为___________ mol。
(1)漂白粉的有效成分是
(2)84消毒液的有效成分中NaClO中Cl的化合价为
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,
①该反应中的氧化剂是__________ ,还原剂是__________ ,每生成1 mol Na2FeO4转移__________ mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:____________________________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:___________________________ 。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?_____________________________________________ 。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,
①该反应中的氧化剂是
②简要说明K2FeO4作为水处理剂时所起的作用:
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知: ,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在
,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在 晶体上,并用表面皿盖好。
晶体上,并用表面皿盖好。
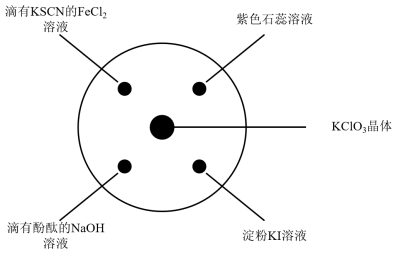
(1)在 反应中
反应中___________ 是氧化剂(填化学式),氧化剂与还原剂物质的量之比为__________ 。
(2)滴有KSCN的 溶液颜色变化为
溶液颜色变化为___________ 。
(3)滴有酚酞的NaOH溶液颜色变化为___________ 。
(4)紫色石蕊溶液颜色变化为先变红后褪色,褪色是因为___________ 有漂白性。
(5)淀粉KI溶液变为蓝色,用离子方程式表示反应原理___________ 。
 ,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在
,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在 晶体上,并用表面皿盖好。
晶体上,并用表面皿盖好。
(1)在
 反应中
反应中(2)滴有KSCN的
 溶液颜色变化为
溶液颜色变化为(3)滴有酚酞的NaOH溶液颜色变化为
(4)紫色石蕊溶液颜色变化为先变红后褪色,褪色是因为
(5)淀粉KI溶液变为蓝色,用离子方程式表示反应原理
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】装置甲、乙、丙的烧杯中都盛有稀硫酸。
(1)装置丙中的Fe电极上的反应式:____________________ 。
(2)装置乙中被腐蚀的金属是________________ (填元素符号),比较装置甲、乙、丙中纯铁被腐蚀的速率由快到慢的顺序是_____________ 。

(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图丁。请回答:
A电极对应的金属是____________ (写元素名称),B电极的电极反应式是______________________ 。
镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_____________________ 。
(1)装置丙中的Fe电极上的反应式:
(2)装置乙中被腐蚀的金属是

(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图丁。请回答:
A电极对应的金属是
镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是_______ 腐蚀(填“析氢"或“吸氧”)
(2)写出铁锅腐蚀时负极的电极反应式:_______
(3)写出铁锅在中性条件下正极的电极反应式_______ 。
(4)写出电化学反应的总方程式_______
(1)铁锅的锈蚀是
(2)写出铁锅腐蚀时负极的电极反应式:
(3)写出铁锅在中性条件下正极的电极反应式
(4)写出电化学反应的总方程式
您最近一年使用:0次



