在下列分子中,①H2,②CO2,③H2O2,④HCN(填序号)
分子中只有σ键的是_________ ,分子中含有π键的是 _________ ,分子中所有原子都满足最外层为8个电子结构的是_________ ,分子中含有由两个原子的s轨道重叠形成的σ键的是 _________ ,分子中含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是 _________ ,分子中既含有极性键又含有非极性键的是_________ 。
分子中只有σ键的是
20-21高二上·宁夏银川·阶段练习 查看更多[2]
(已下线)2.1 共价键(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)宁夏回族自治区银川市宁夏大学附属中学2020-2021学年高二上学期第一次月考化学试题
更新时间:2020/10/15 22:07:39
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O,根据等电子原理,CO分子的结构式为___________ ,1molCO2中含有的σ键数目为___________
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在元素周期表中,同一主族元素化学性质相似。目前也发现有些元素的化学性质在周期表中左上方或右下方的另一主族元素性质相似,这称为对角线规则。据此请回答:
(1)锂在空气中燃烧,除了生成_______ 外,也生成微量的________ 。
(2)铍的最高价氧化物对应水化物属于两性化合物,证明这一结论的有关离子方程式________ ,________ 。
(3)科学家证实,BeCl2是共价化合物,设计一个简单实验证明,其方法是_________ 。用电子式表示BeCl2的形成过程__________
(1)锂在空气中燃烧,除了生成
(2)铍的最高价氧化物对应水化物属于两性化合物,证明这一结论的有关离子方程式
(3)科学家证实,BeCl2是共价化合物,设计一个简单实验证明,其方法是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据氢气分子的形成过程示意图(如下图)回答问题:
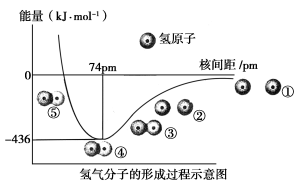
(1)H—H键的键长为_______ ,①~⑤中,体系能量由高到低的顺序是_______ 。
(2)下列说法中正确的是_______。
(3)几种常见化学键的键能如下表:
比较Si—Si键与Si—C键的键能大小:x_______ (填“>”、“<”或“=”)176。

(1)H—H键的键长为
(2)下列说法中正确的是_______。
| A.氢气分子中含有一个π键 |
| B.由①到④,电子在核间出现的几率增大 |
| C.由④到⑤,必须消耗外界的能量 |
| D.氢气分子中含有一个极性共价键 |
| 化学键 | Si—O | H—O | O=O | Si—Si | Si—C |
| 键能/kJ·mol-1 | 460 | 464 | 498 | 176 | x |
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)CH2=CH—C≡N分子中含有 ______ 个σ键,______ 个π键。
(2)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素名称是______ 。
(2)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素名称是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】PM2.5中的某些物质,易引发光化学烟雾污染,光化学烟雾中含有NOx、OCS、CH2=CH-CHO、HCOOH、以及光气等二次污染物。水污染程度可通过测定水体中铅、铬等重金属的含量判断。
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______ (用元素符号表示),CH2=CH-CHO分子醛基中碳原子杂化方式为____________ 。
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为_________ ;光气(COCl2)各原子最外层都满足8电子稳定结构,则光气分子的空间构型为_________ (用文字描述);
(3)1molHCOOH中含σ键和π键数目之比为______________ 。
(4)基态Cr原子核外电子排布式是_______ ,配合物[Cr(NH3)4(H2O)2] Cl3中心离子的配体为_______ 。
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=______ (填数字)。若两个相邻面心的Kr原子的核间距为acm,用NA表示阿伏伽德罗常数,M表示Kr的相对原子质量。该晶体的密度计算式为______ g/cm3。
(1)C、N、O三种元素的第一电离能从大到小的顺序为
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为
(3)1molHCOOH中含σ键和π键数目之比为
(4)基态Cr原子核外电子排布式是
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=

您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】完成下列各题:
(1)写出电子式NH4Cl_______ ,它的阳离子价层电子对对数为______ ,该离子空间构型为_______ 。
(2)周期表一共18列,第四周期第11列元素A,表示A所在族的符号为_________ ,它的基态原子结构示意图为_____ ,A+离子的价层电子排布图为____________ ,A2+离子的价层电子排布式为_____________ ,A+离子和A2+离子较稳定的是(填离子符号)_______ ,原因________________________ 。
(3)乙炔和乙烯分子,它们的σ键个数之比为______ ,乙烯分子中C原子杂化方式为________ ,C、N、O三种原子第一电离能从大到小排列____________ 。
(1)写出电子式NH4Cl
(2)周期表一共18列,第四周期第11列元素A,表示A所在族的符号为
(3)乙炔和乙烯分子,它们的σ键个数之比为
您最近半年使用:0次



