工业上以氮气为主要原料制备硝酸,其转化过程如下:
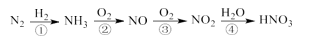
在这四步反应中,氮元素只被还原的一步是( )
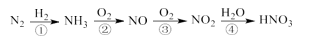
在这四步反应中,氮元素只被还原的一步是( )
| A.① | B.② | C.③ | D.④ |
18-19高一下·广西南宁·期中 查看更多[1]
(已下线)【全国百强校】广西南宁市第三中学2018-2019学年高一下学期期中考试化学(文)试题
更新时间:2019-05-08 20:00:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是
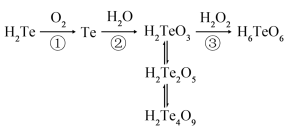

| A.反应①利用了H2Te的还原性 |
| B.反应②中H2O作氧化剂 |
| C.反应③利用了H2O2的氧化性 |
| D.H2Te2O5转化为H2Te4O9发生了氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如下,下列说法中,不正确的是
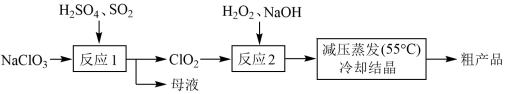

| A.采用减压蒸发可能是为了防止 NaClO2受热分解 |
| B.从母液中可以提取 Na2SO4 |
| C.反应2中,H2O2做氧化剂 |
| D.反应1中,每生成 1 mol ClO2有 0.5 mol SO2被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用空气催化氧化法除掉电石渣浆[含Ca(OH)2]上清液中的S2-,制取石膏(CaSO4•2H2O)的过程如图:
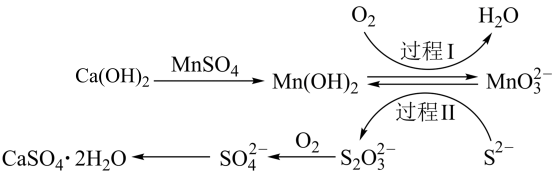
下列说法错误的是

下列说法错误的是
| A.CaSO4•2H2O属于盐类和纯净物 |
B.过程I中,反应的离子方程式为2Mn(OH)2+O2+4OH-=2MnO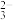 +4H2O +4H2O |
| C.过程II中,S2-为还原剂 |
| D.上述流程中,只有钙元素的化合价没有变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】关于氧化还原反应,下列说法正确的有( )
①氧化还原反应的本质是有化合价升降;②物质所含元素化合价变化是判断氧化还原反应的依据;③当反应中有一种元素被氧化时,一定有另一种元素被还原;④含有高价态元素的化合物不一定具有强氧化性;⑤阳离子只能得到电子被还原,阴离子只能失去电子被氧化;⑥在化学反应中,得电子越多的物质,其氧化性越强;⑦在氧化还原反应中非金属单质一定被还原。
①氧化还原反应的本质是有化合价升降;②物质所含元素化合价变化是判断氧化还原反应的依据;③当反应中有一种元素被氧化时,一定有另一种元素被还原;④含有高价态元素的化合物不一定具有强氧化性;⑤阳离子只能得到电子被还原,阴离子只能失去电子被氧化;⑥在化学反应中,得电子越多的物质,其氧化性越强;⑦在氧化还原反应中非金属单质一定被还原。
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2或K2O2的说法正确的个数是
①Na2O2中阴、阳离子的个数比是1∶1
②K2O2分别与水及CO2反应产生等量氧气时,需水和CO2的质量相等
③Na2O2分别与水及CO2反应产生等量氧气时,转移电子的物质的量相等
④Na2O2的漂白原理与SO2的漂白原理相同
⑤Na2O2与SO2反应生成Na2SO3 和O2
⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
⑦K2O2与水反应,K2O2既是氧化剂,又是还原剂
⑧Na2O2投入到紫色石蕊溶液中,溶液先变蓝,后褪色
①Na2O2中阴、阳离子的个数比是1∶1
②K2O2分别与水及CO2反应产生等量氧气时,需水和CO2的质量相等
③Na2O2分别与水及CO2反应产生等量氧气时,转移电子的物质的量相等
④Na2O2的漂白原理与SO2的漂白原理相同
⑤Na2O2与SO2反应生成Na2SO3 和O2
⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
⑦K2O2与水反应,K2O2既是氧化剂,又是还原剂
⑧Na2O2投入到紫色石蕊溶液中,溶液先变蓝,后褪色
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中反应制得:①3SiO2+6C+2N2 Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3
Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3 Si3N4+12HCl。则下列叙述正确的是
Si3N4+12HCl。则下列叙述正确的是
 Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3
Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3 Si3N4+12HCl。则下列叙述正确的是
Si3N4+12HCl。则下列叙述正确的是| A.反应②属于离子反应 |
| B.若制取等量的Si3N4,则反应①②转移电子数目必然相等 |
| C.反应①的氧化剂是N2 |
| D.反应①中氧化产物与还原产物物质的量之比为1∶6 |
您最近一年使用:0次




