标准状况下,0.2 mol CH4 的体积是_____ L,其中含有的 CH4分子数是_____ 个,含氢原子数是_____ 个,其中含有的电子数是_____ 个,其 中含有的质子数是_____ 个。
更新时间:2020-10-21 19:32:46
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在标准状况下,①5 g H2 ②11.2 L O2 ③2 mol H2O ④6.02×1023个 CO2分子。
(1)5gH2 的物质的量是_______ ,体积是_______ ;
(2)6.02×1023个CO2分子的物质的量是_____ ,质量是______ ;
(3)所含分子数最多的是______ (请用序号回答,后同);
(4)所含原子数最多的是______ ;
(5)质量最大的是_______ ;
(6)体积最大的是_______ ;
(7) 体积最小的是_______ 。
(1)5gH2 的物质的量是
(2)6.02×1023个CO2分子的物质的量是
(3)所含分子数最多的是
(4)所含原子数最多的是
(5)质量最大的是
(6)体积最大的是
(7) 体积最小的是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】完成下列与“物质的量”相关的计算。
(1)标准状况下,33.6LCO2的物质的量为___ mol,质量为___ g,所含O原子的数目是____ 个。
(2)同温同压下,同体积的氨(NH3)和硫化氢(H2S)气体的质量之比是____ ,同质量的氨和硫化氢气体所含氢原子个数之比是___ 。
(3)agCl2中有b个氯原子,则阿伏加 德罗常数NA的数值可表示为____ 。
(1)标准状况下,33.6LCO2的物质的量为
(2)同温同压下,同体积的氨(NH3)和硫化氢(H2S)气体的质量之比是
(3)agCl2中有b个氯原子,则阿伏加 德罗常数NA的数值可表示为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)0.3 mol NH3分子中所含原子数_____ ,质量是____ ,标准状况下的体积是____ 。
(2)含有0.4 mol Al3+的Al2(SO4)3溶液中所含SO42-的物质的量是______ 。
(3)等质量的SO2和SO3中, 硫原子个数之比为____ ,氧原子个数之比_______ 。
(4)配制100 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O质量为__________ ;0.5L0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为___________ 。
(2)含有0.4 mol Al3+的Al2(SO4)3溶液中所含SO42-的物质的量是
(3)等质量的SO2和SO3中, 硫原子个数之比为
(4)配制100 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)标准状况下,0.8g 与
与_______ 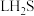 含有相同的氢原子数。
含有相同的氢原子数。
(2)19g某二价金属的氯化物 中含有0.4mol的
中含有0.4mol的 ,则R的摩尔质量为
,则R的摩尔质量为_______ 。
(3)如图是“康师傅”牌饮用矿泉水的标签的部分内容。
请认真阅读标签内容,计算:一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过_____ mol。
(4)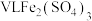 溶液中含
溶液中含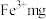 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为_______  ,若取出V/3L溶液,又加水稀释到溶液体积为2VL,则此时
,若取出V/3L溶液,又加水稀释到溶液体积为2VL,则此时 的物质的量浓度为
的物质的量浓度为_______ 。
(5)如果定义1mol粒子的集合体的数目约为 ,那么此时标准状况下,气体摩尔体积的数值约为
,那么此时标准状况下,气体摩尔体积的数值约为_______ L/mol,标准状况下,3.36L 的质量是
的质量是_______ g。
(1)标准状况下,0.8g
 与
与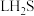 含有相同的氢原子数。
含有相同的氢原子数。(2)19g某二价金属的氯化物
 中含有0.4mol的
中含有0.4mol的 ,则R的摩尔质量为
,则R的摩尔质量为(3)如图是“康师傅”牌饮用矿泉水的标签的部分内容。
| 康师傅饮用矿物质水 净含量:500mL 配料表:纯净水 硫酸镁 氯化钾 保质期:12个月 主要成分: 钾离子(  ):1.0~27.3mg/L ):1.0~27.3mg/L镁离子(  ):0.1~4.8mg/L ):0.1~4.8mg/L氯离子(  ):10~27.3mg/L ):10~27.3mg/L硫酸根离子(  ):0.4~19.2mg/L ):0.4~19.2mg/L |
(4)
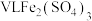 溶液中含
溶液中含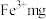 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为 ,若取出V/3L溶液,又加水稀释到溶液体积为2VL,则此时
,若取出V/3L溶液,又加水稀释到溶液体积为2VL,则此时 的物质的量浓度为
的物质的量浓度为(5)如果定义1mol粒子的集合体的数目约为
 ,那么此时标准状况下,气体摩尔体积的数值约为
,那么此时标准状况下,气体摩尔体积的数值约为 的质量是
的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】填空题
(1)2 mol 和3 mol
和3 mol  的分子数之比为
的分子数之比为___________ ,原子数之比___________ 。
(2)某氯化物 19 g,含有0.4 mol
19 g,含有0.4 mol  ,M的摩尔质量为
,M的摩尔质量为___________ 。
(3)同温同压下,同体积的 气体和CO气体质量之比为
气体和CO气体质量之比为___________ ,质子数之比为___________ 。
(4)11.6 g 和
和 的混合气体在标准状况下的体积为11.2 L,则混合气体中
的混合气体在标准状况下的体积为11.2 L,则混合气体中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(5)从100 mL 0.1 mol/L 溶液中取出10 mL,则10 mL溶液中,
溶液中取出10 mL,则10 mL溶液中, 物质的量为
物质的量为_____ , 的物质的量浓度是
的物质的量浓度是___________ 。
(1)2 mol
 和3 mol
和3 mol  的分子数之比为
的分子数之比为(2)某氯化物
 19 g,含有0.4 mol
19 g,含有0.4 mol  ,M的摩尔质量为
,M的摩尔质量为(3)同温同压下,同体积的
 气体和CO气体质量之比为
气体和CO气体质量之比为(4)11.6 g
 和
和 的混合气体在标准状况下的体积为11.2 L,则混合气体中
的混合气体在标准状况下的体积为11.2 L,则混合气体中 和
和 的物质的量之比为
的物质的量之比为(5)从100 mL 0.1 mol/L
 溶液中取出10 mL,则10 mL溶液中,
溶液中取出10 mL,则10 mL溶液中, 物质的量为
物质的量为 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】化学计量在化学中占有重要地位,请回答下列问题:
(1)现有mg某气体,它由双原子分子构成,其摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为________ ;
②该气体所含原子总数为_______________ 个;
③该气体在标准状况下的体积为__________ 。
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是_______ (用分式表示)。
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是______________ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4 mol/L,则c(SO42-)=__________ 。
(1)现有mg某气体,它由双原子分子构成,其摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为
②该气体所含原子总数为
③该气体在标准状况下的体积为
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4 mol/L,则c(SO42-)=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)0.3molNH3分子中所含氢原子数与___ 个H2O分子中所含氢原子数相等。
(2)含0.4molFe3+的Fe2(SO4)3中所含的SO42-的物质的量是___ 。
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为____ 。
(4)2.3gNa中含___ mole-,在反应中生成Na+共失去___ mole-。
(5)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)____ 。
(2)含0.4molFe3+的Fe2(SO4)3中所含的SO42-的物质的量是
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)2.3gNa中含
(5)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】6.02×1024个Na+约含________ mol Na+,其质量为___________ g;4.5molCH4约含有____________ 个CH4,其质量为_______ g;3.01×1023个SO42-约含_____ molSO42-,其质量为_____ g;49gH2SO4约含有___________ 个H,共含有______ mol原子。
您最近一年使用:0次



