请从下列化学方程式中选择正确答案,将其编号填入相应括号内。
A.2KClO3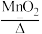 2KCl+3O2↑B.2Fe+3Cl2
2KCl+3O2↑B.2Fe+3Cl2 2FeCl3
2FeCl3
C.NH4HCO3 NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3
NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3
E.Cl2+H2O=HCl+HClO
Ⅰ.(1)既是分解反应又是氧化还原反应的是___________
(2)是分解反应但不是氧化还原反应的是___________
(3)既是化合反应又是氧化还原反应的是___________
(4)是化合反应但不是氧化还原反应的是___________
(5)不属于四种基本反应类型的氧化还原反应的是___________
Ⅱ.将A中方程式用双线桥表示电子转移方向和数目,2KClO3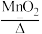 2KCl+3O2↑
2KCl+3O2↑___________ ,将B中方程式用单线桥表示电子转移方向和数目2Fe+3Cl2 2FeCl3,
2FeCl3,___________
A.2KClO3
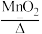 2KCl+3O2↑B.2Fe+3Cl2
2KCl+3O2↑B.2Fe+3Cl2 2FeCl3
2FeCl3C.NH4HCO3
 NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3
NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3E.Cl2+H2O=HCl+HClO
Ⅰ.(1)既是分解反应又是氧化还原反应的是
(2)是分解反应但不是氧化还原反应的是
(3)既是化合反应又是氧化还原反应的是
(4)是化合反应但不是氧化还原反应的是
(5)不属于四种基本反应类型的氧化还原反应的是
Ⅱ.将A中方程式用双线桥表示电子转移方向和数目,2KClO3
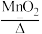 2KCl+3O2↑
2KCl+3O2↑ 2FeCl3,
2FeCl3,
更新时间:2020-10-19 22:02:44
|
相似题推荐
【推荐1】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。根据氧化还原知识填空:
①Fe2+→Fe3+的转化时,Fe2+在反应中发生_______ 反应(填“氧化”或“还原”);
②“服用维生素C可使食物中的Fe3+转变成Fe2+”,这句话说明维生素C作_______ 剂(填“氧化”或“还原”)。
(2)砒霜(As2O3)可与Zn反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。其中,As2O3显示出来的性质是_______ (填“还原性”或“氧化性”),氧化产物是_______ 。
(3)钛金属具有硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。在工业上常常采用钠还原TiCl4的方法制取,该反应的反应方程式如下:TiCl4+4Na=Ti+4NaCl。
①用单线桥法标出上述化学方程式的电子转移情况_______ ;
②若4个Na全部参加反应,则该过程转移的电子是_______ 个。
(4)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。请将方程式补充完整:_______ 。
_______NaClO+_______HCl(浓) =_______NaCl+_______Cl2↑+_______H2O
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。根据氧化还原知识填空:
①Fe2+→Fe3+的转化时,Fe2+在反应中发生
②“服用维生素C可使食物中的Fe3+转变成Fe2+”,这句话说明维生素C作
(2)砒霜(As2O3)可与Zn反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。其中,As2O3显示出来的性质是
(3)钛金属具有硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。在工业上常常采用钠还原TiCl4的方法制取,该反应的反应方程式如下:TiCl4+4Na=Ti+4NaCl。
①用单线桥法标出上述化学方程式的电子转移情况
②若4个Na全部参加反应,则该过程转移的电子是
(4)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。请将方程式补充完整:
_______NaClO+_______HCl(浓) =_______NaCl+_______Cl2↑+_______H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(1)煤燃烧时会产生大量的SO2,可向煤中加入_____________ 吸收SO2。检验脱硫后废气中是否含有SO2的简单方法是________________________________________________ 。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①由图1可知SCR技术中的氧化剂是__________________
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图3所示,脱氮效果最佳的c(NO2)/c(NO)=______ 。
(3)某工厂拟综合处理含NH 废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
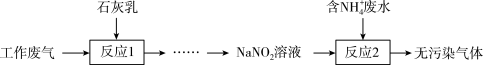
“反应2”的离子方程式为________________________________ 。
(1)煤燃烧时会产生大量的SO2,可向煤中加入
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①由图1可知SCR技术中的氧化剂是
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图3所示,脱氮效果最佳的c(NO2)/c(NO)=
(3)某工厂拟综合处理含NH
 废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:
“反应2”的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】杭州亚运会主火炬的燃料是“绿色”甲醇,之所以将其称之为“绿色”,是因为该甲醇的制备过程“零增碳”,即从生产甲醇到燃烧甲醇,产生、消耗的二氧化碳量实现完全中和。为解决能源与环境问题,有学者提出如图所示的含碳物质转化的技术路线。回答下列问题:

(1)上述涉及的物质中属于非电解质的是___________ (填化学式)。
(2)K2CO3既属于钾盐,也属于碳酸盐,该分类方法属于___________ 。
(3)上述反应中,属于氧化还原反应的是___________(填序号)。
(4)写出NaHCO3在水溶液中的电离方程式___________ ;
(5)反应③中,参加反应的 H2 和生成的CH3OH的分子数目之比为___________ ,每生成1个H2O分子,转移___________ 个电子。

(1)上述涉及的物质中属于非电解质的是
(2)K2CO3既属于钾盐,也属于碳酸盐,该分类方法属于
(3)上述反应中,属于氧化还原反应的是___________(填序号)。
| A.反应① | B.反应② | C.反应③ | D.反应④ |
(4)写出NaHCO3在水溶液中的电离方程式
(5)反应③中,参加反应的 H2 和生成的CH3OH的分子数目之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】有以下几种物质:①铁丝;②液态 ;③75%酒精溶液;④稀盐酸;⑤
;③75%酒精溶液;④稀盐酸;⑤ ;⑥
;⑥ 固体;⑦熔融
固体;⑦熔融 。
。
(1)以上物质属于单质的是_______ (填序号,下同),属于电解质的是_______ 。
(2)①与⑤的稀溶液反应的化学方程式为_______ 。
(3)⑦的电离方程式为_______ 。
(4)在发生离子反应的反应物或生成物中,一定存在的是_______(填字母)。
(5)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
①下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母)。

②碱式碳酸铜 可以看作是
可以看作是 和
和 按照1∶1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:
按照1∶1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:_______ 。
 ;③75%酒精溶液;④稀盐酸;⑤
;③75%酒精溶液;④稀盐酸;⑤ ;⑥
;⑥ 固体;⑦熔融
固体;⑦熔融 。
。(1)以上物质属于单质的是
(2)①与⑤的稀溶液反应的化学方程式为
(3)⑦的电离方程式为
(4)在发生离子反应的反应物或生成物中,一定存在的是_______(填字母)。
| A.单质 | B.氧化物 | C.酸 | D.化合物 |
①下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

②碱式碳酸铜
 可以看作是
可以看作是 和
和 按照1∶1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:
按照1∶1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1000℃左右冶炼,可能涉及的反应有:
①Cu2(OH)2CO3 2CuO+CO2↑+H2O;②2CuO+C
2CuO+CO2↑+H2O;②2CuO+C 2Cu+CO2↑;③CuO+CO
2Cu+CO2↑;③CuO+CO Cu+CO2;④CO2+C
Cu+CO2;④CO2+C 2CO。
2CO。
(1)从四种基本反应类型来看,①②④的反应类型分别为①____________ ,②____________ ,④____________ 。
(2)从氧化还原反应的角度看,属于氧化还原反应的有____________ 。
(3)反应③中,____________ 发生氧化反应,__________ 发生还原反应。
(4)请在下图中用斜线表示反应③所属的区域。
 ;
;_______
①Cu2(OH)2CO3
 2CuO+CO2↑+H2O;②2CuO+C
2CuO+CO2↑+H2O;②2CuO+C 2Cu+CO2↑;③CuO+CO
2Cu+CO2↑;③CuO+CO Cu+CO2;④CO2+C
Cu+CO2;④CO2+C 2CO。
2CO。(1)从四种基本反应类型来看,①②④的反应类型分别为①
(2)从氧化还原反应的角度看,属于氧化还原反应的有
(3)反应③中,
(4)请在下图中用斜线表示反应③所属的区域。
 ;
;
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学反应按照不同的分类方法,可以分为化合反应、分解反应、置换反应、复分解反应,或者分为氧化还原反应和非氧化还原反应。有下列一组反应:
① ;②
;②
③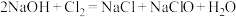 ;④
;④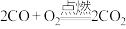
⑤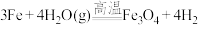 ;⑥
;⑥
⑦Fe+CuSO4=FeSO4+Cu;⑧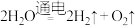
⑨2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑;⑩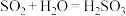
请将适当的序号填空
(1)其中属于化合反应的有_____ ,属于置换反应的有_____ 。
(2)在化学反应前后元素的化合价没有变化的是_____ 。
(3)上述反应中,既是分解反应又是氧化还原反应的是_____ 。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是_____
(5)根据你的理解,氧化还原反应的实质是_____。
①
 ;②
;②
③
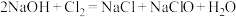 ;④
;④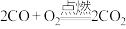
⑤
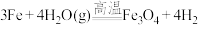 ;⑥
;⑥
⑦Fe+CuSO4=FeSO4+Cu;⑧
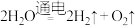
⑨2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑;⑩
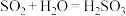
请将适当的序号填空
(1)其中属于化合反应的有
(2)在化学反应前后元素的化合价没有变化的是
(3)上述反应中,既是分解反应又是氧化还原反应的是
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是
(5)根据你的理解,氧化还原反应的实质是_____。
| A.分子中的原子重新组合 |
| B.氧的得失 |
| C.电子的得失或共用电子对的偏移 |
| D.元素化合价的改变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】工业上次磷酸( )常用于化学镀银,反应原理如下:
)常用于化学镀银,反应原理如下:
 (未配平)
(未配平)
回答下列问题:
(1) 中,P元素的化合价为
中,P元素的化合价为___________ ;该反应中, 被
被___________ (选填“氧化”或“还原”)。
(2)配平化学方程式并用单线桥标出电子转移的方向和数目___________ 。反应每消耗1个 ,转移
,转移___________ 个电子。
(3)已知 是一元弱酸,其电离方程式为
是一元弱酸,其电离方程式为________________ 。 与足量
与足量 溶液反应生成的钠盐属于
溶液反应生成的钠盐属于___________ (选填“正盐”“酸式盐”或“碱式盐”)
 )常用于化学镀银,反应原理如下:
)常用于化学镀银,反应原理如下: (未配平)
(未配平)回答下列问题:
(1)
 中,P元素的化合价为
中,P元素的化合价为 被
被(2)配平化学方程式并用单线桥标出电子转移的方向和数目
 ,转移
,转移(3)已知
 是一元弱酸,其电离方程式为
是一元弱酸,其电离方程式为 与足量
与足量 溶液反应生成的钠盐属于
溶液反应生成的钠盐属于
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题。
(1)请用双线桥标出下列反应的电子转移情况:
①Cl2+2NaOH=NaCl+NaClO+H2O:___________ 。
②MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O:
MnCl2+Cl2↑+2H2O:___________ 。
(2)请写出下列反应的离子方程式。
①钠与水反应的离子方程式:___________ 。
②氢氧化铜与盐酸反应的离子方程式:___________ 。
(3)小苏打可做胃药,治疗胃酸过多,请用化学方程式写出其反应原理:___________ 。
(1)请用双线桥标出下列反应的电子转移情况:
①Cl2+2NaOH=NaCl+NaClO+H2O:
②MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O:
MnCl2+Cl2↑+2H2O:(2)请写出下列反应的离子方程式。
①钠与水反应的离子方程式:
②氢氧化铜与盐酸反应的离子方程式:
(3)小苏打可做胃药,治疗胃酸过多,请用化学方程式写出其反应原理:
您最近一年使用:0次

 2Fe+3CO2。
2Fe+3CO2。

