I.药物X是由五种短周期元素组成的纯净物,利用下列过程推断其组成:

已知:气体C为常见的温室气体。经分析混合气体G中含有280 mL气体C(标准状况)。固体F焰色反应呈黄色。请回答:
(1)组成药物X的非金属元素是_________ ,药物X的化学式是_________ 。
(2)药物X分解生成固体A的化学方程式:__________________ 。
(3)药物X可通过溶液E与A制备,写出相应的化学方程式:__________________ 。
II.某兴趣小组利用如下实验装置模拟含Mn2+废水的处理。
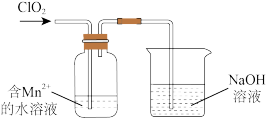
请回答:
(1)广口瓶中出现黑色沉淀,溶液呈强酸性,用一个离子方程式表示:_________ 。
(2)NaOH吸收尾气中的ClO2,可生成NaClO3和NaCl。请设计实验验证有NaClO3生成:________________________________ 。

已知:气体C为常见的温室气体。经分析混合气体G中含有280 mL气体C(标准状况)。固体F焰色反应呈黄色。请回答:
(1)组成药物X的非金属元素是
(2)药物X分解生成固体A的化学方程式:
(3)药物X可通过溶液E与A制备,写出相应的化学方程式:
II.某兴趣小组利用如下实验装置模拟含Mn2+废水的处理。

请回答:
(1)广口瓶中出现黑色沉淀,溶液呈强酸性,用一个离子方程式表示:
(2)NaOH吸收尾气中的ClO2,可生成NaClO3和NaCl。请设计实验验证有NaClO3生成:
更新时间:2020-10-24 09:01:31
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D均为常见的纯净物,A是单质。它们之间有如下的反应关系:
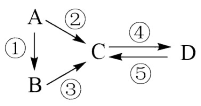
(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。但C也有广泛用途,写出工业上C物质的任意一种主要用途_______ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式并用单线桥法标出反应中电子的转移和数目_______ 。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应时通入过量的一种引起温室效应的主要气体。则工业上生产A的一般方法是_______ 。
A.热分解法 B.热还原法 C.电解法
写出④反应离子方程式_______ 。
(4)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式_______ 。

(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。但C也有广泛用途,写出工业上C物质的任意一种主要用途
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式并用单线桥法标出反应中电子的转移和数目
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应时通入过量的一种引起温室效应的主要气体。则工业上生产A的一般方法是
A.热分解法 B.热还原法 C.电解法
写出④反应离子方程式
(4)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】为探究某固体化合物X(仅含三种元素)的组成和性质,设计并完成如下实验。已知:X、A、B、C、D均为单一物质。请回答:
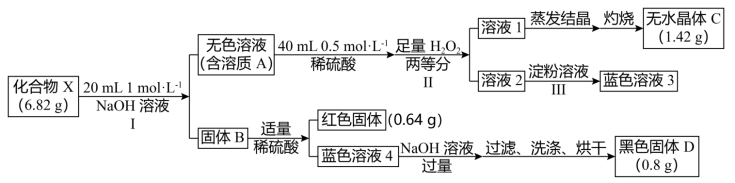
(1)黑色固体D是_______ ,A的电子式是_______ 。
(2)步骤II,无色溶液A与H2O2反应的离子方程式是_______ ,
(3)X的化学式是_______ 。

(1)黑色固体D是
(2)步骤II,无色溶液A与H2O2反应的离子方程式是
(3)X的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图表示中学化学中常见物质的转化关系(部分条件已略去)。其中A属于正盐,B、C、E是常见的气体,C能使湿润的红色石蕊试纸变蓝,D是一种淡黄色固体。

回答下列问题:
(1)A物质的化学式是___________ ,A中存在的化学键有___________ 。
(2)C的电子式是___________ ,在上述①~④反应中属于氧化还原反应的是___________ (填编号)。
(3)写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:___________ 。
(4)请写出反应④的化学方程式:___________ ,写出该反应在工业上的用途:___________ 。

回答下列问题:
(1)A物质的化学式是
(2)C的电子式是
(3)写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:
(4)请写出反应④的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C三种常见的短周期元素,它们的取子序数逐渐增大。A元素原子最外层电子数是次外层电子数的2倍,B元素原子最外层电子数等于其电子层数,且为C元素原子最外层电子数的一半。甲为含B的钠盐,乙为C的最高价氧化物对应的水化物,丙为含A的钠盐。甲、 乙、丙、丁四种物质之间的相互反应关系如下图:

请回答:
(1)写出A的最高价的氧化物的电子式___________________________ ;C在周期表中的位置___________________________________ 。
(2)写出甲溶液与丁溶液反应的离子方程式:_______________________ 。
(3)向甲溶液中通入足量的CO2,写出该反应的离子方程式:_________________________ 。

请回答:
(1)写出A的最高价的氧化物的电子式
(2)写出甲溶液与丁溶液反应的离子方程式:
(3)向甲溶液中通入足量的CO2,写出该反应的离子方程式:
您最近一年使用:0次
【推荐2】我国河南、广西和贵州等省份高硫铝土矿储量较高,其主要成分为Al2O3、Fe2O3,还含有少量SiO2、FeS2。现以高硫铝土矿为原料生产Al2O3和Fe3O4的部分工艺流程如下所示。
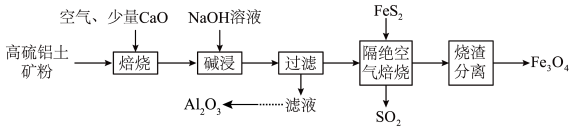
(1)加入少量CaO的主要作用为_____________ 。
(2)配平“焙烧”过程中发生反应的化学方程式:______________ 。




(3)向“过滤”得到的滤液中通入过量CO2,含金属元素的阴离子发生反应的离子方程式为___________________________ 。
(4)“隔绝空气焙烧”过程生成Fe3O4和SO2,发生反应的化学方程式为____________ 。
(5)“烧渣分离”若采取物理方法可以使用___________ (填物质名称)分离。
(6)纯度检验:将少量产品溶于稀硫酸中,再滴入酸性KMnO4溶液,若酸性KMnO4溶液褪色,___________ (填“能”或“不能”)说明产品中含有FeO,理由是________________________________________ 。
(7)“焙烧”的过程中采用多层逆流焙烧,优点是_____________ (任答一点)。

(1)加入少量CaO的主要作用为
(2)配平“焙烧”过程中发生反应的化学方程式:




(3)向“过滤”得到的滤液中通入过量CO2,含金属元素的阴离子发生反应的离子方程式为
(4)“隔绝空气焙烧”过程生成Fe3O4和SO2,发生反应的化学方程式为
(5)“烧渣分离”若采取物理方法可以使用
(6)纯度检验:将少量产品溶于稀硫酸中,再滴入酸性KMnO4溶液,若酸性KMnO4溶液褪色,
(7)“焙烧”的过程中采用多层逆流焙烧,优点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(Ⅰ)某小组同学依据性质差异,采用比较的方法设计实验鉴别Na2CO3和NaHCO3。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中_______ (填“放出”或“吸收”)热量,可判断固体b为Na2CO3。
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。分别向两支试管中滴加2滴酚酞,_______ 试管中红色较浅。
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因_______ 。
(Ⅱ)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(4)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为_______ mol。
(5)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①配料中属于两性氧化物的是_______
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O= Na2Al2Si2O8↓+4NaOH ,“赤泥”的主要成分为Na2Al2Si2O8和_______ (写出化学式)。
③ “酸化”时,通入过量CO2与之反应,生成滤液的主要成分是_______ (写化学式)。
实验I | 实验Ⅱ | 实验Ⅲ |
 |  |  |
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。分别向两支试管中滴加2滴酚酞,
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因
(Ⅱ)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(4)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为
(5)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①配料中属于两性氧化物的是
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O= Na2Al2Si2O8↓+4NaOH ,“赤泥”的主要成分为Na2Al2Si2O8和
③ “酸化”时,通入过量CO2与之反应,生成滤液的主要成分是
您最近一年使用:0次



