《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_________________ 。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
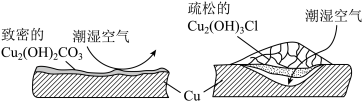
青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu2(OH)3Cl的原理示意图为:
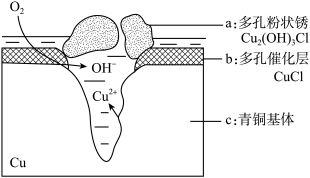
写出正极的电极反应式____________ ;若生成2.145 g Cu2(OH)3Cl,理论上消耗标准状况下氧气的体积为________ L。
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:

①过程Ⅰ的正极反应物是___________ 。
②过程Ⅰ负极的电极反应式是__________________________________ 。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:
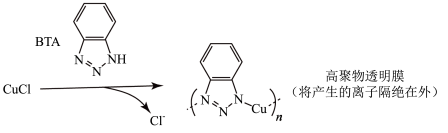
请回答下列问题:
①写出碳酸钠法的离子方程式________________________________________________ 。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________ 。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:

青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu2(OH)3Cl的原理示意图为:

写出正极的电极反应式
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:

①过程Ⅰ的正极反应物是
②过程Ⅰ负极的电极反应式是
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:

请回答下列问题:
①写出碳酸钠法的离子方程式
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
更新时间:2020-10-25 18:28:53
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】碘化亚铜(CuI)是一种不溶于水也不溶于酸的白色固体,用途很广泛,可用作有机合成催化剂、树脂改性剂、人工降雨剂、阳极射线管覆盖物,以及加碘盐中的碘来源。下图是工业上利用冰铜制备无水碘化亚铜的流程。
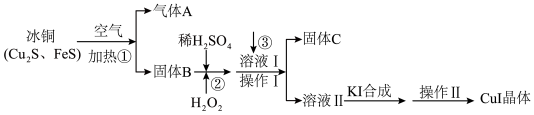
(1)步骤①中Cu2S被转化为Cu,同时有大气污染物A生成,此反应化学方程式为_____ ,固体B的主要成分为黑色磁性物质,其化学式为______ 。
(2)步骤②中H2O2的作用是_______ 。
(3)溶液I中含少量Fe3+,步骤③加入氨水加以除去,已知室温下Fe(OH)3的Ksp=8.0×10−38,据此分析,室温下除去Fe3+应调节pH不小于_____ 。(已知lg2≈0.3)
(4)操作II为先水洗后乙醇洗,用乙醇洗涤的好处是______ 。
(5)写出合成步发生反应的离子方程式______ 。
(6)产物纯度测定:称产物agCuI样品,加足量的FeCl3溶液,发生2CuI+4Fe3+=2Cu2++4Fe2++I2,待样品完全反应后,用bmol/L酸性K2Cr2O7溶液滴定Fe2+,消耗标准液的体积平均值为cmL。样品中CuI的质量分数的计算表达式为____ (请用含a、b、c的式子表示)。如果滴定前,锥形瓶用待测液润洗,CuI的质量分数_____ (填“偏低”、“偏高”或“无影响”)。

(1)步骤①中Cu2S被转化为Cu,同时有大气污染物A生成,此反应化学方程式为
(2)步骤②中H2O2的作用是
(3)溶液I中含少量Fe3+,步骤③加入氨水加以除去,已知室温下Fe(OH)3的Ksp=8.0×10−38,据此分析,室温下除去Fe3+应调节pH不小于
(4)操作II为先水洗后乙醇洗,用乙醇洗涤的好处是
(5)写出合成步发生反应的离子方程式
(6)产物纯度测定:称产物agCuI样品,加足量的FeCl3溶液,发生2CuI+4Fe3+=2Cu2++4Fe2++I2,待样品完全反应后,用bmol/L酸性K2Cr2O7溶液滴定Fe2+,消耗标准液的体积平均值为cmL。样品中CuI的质量分数的计算表达式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣小组发现实验室有多件表面呈灰绿色的金属制品, 经了解其来源并查阅相关资料(如下表),初步确认为铜制品。
针对铜制品表面的灰绿色物质究竟是什么,同学们提出了多种猜想并展开实验探究。
【猜想假设】
(1)小吴同学认为可能是纯铜制品表面涂上了灰绿色的油漆;
小周同学认为可能是青铜(铜锡合金),因为常见的青铜是灰绿色的;
小黄同学认为是纯铜制品,只是表面长出了铜绿[ Cu2(OH)2CO3];
除上述猜想外,其他合理的猜想是____________________ (只写一个)。
【实验验证】三位同学为了验证各自上述的猜想,进行了以下探究:
(2)小吴刮下部分灰绿色物质放入燃烧匙中进行灼烧,发现该物质不能燃烧,证明灰绿色物质不是油漆。 其判断依据是________________________ 。
(3)小周刮下足量的灰绿色物质投入盐酸溶液中,观察到有气体产生,实验表明该气体不能燃烧。将表面刮净后的铜制品也投入盐酸中,并无气体产生。由此证明该铜制品不是青铜,理由是__________________ 。
(4)根据上述实验,小黄认为灰绿色物质可能是铜绿[ Cu2(OH)2CO3]。于是按图5所示装置进行实验。
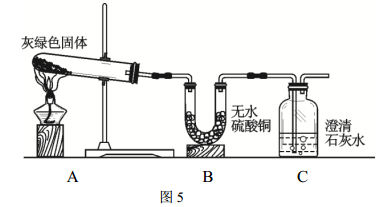
实验证明小黄的猜测是正确的,因为在A中观察到灰绿色物质变黑,B中观察到了___________ 的现象, C中观察到了_____________ 的现象。B中所发生反应的化学方程式为:__________________ 。
如果将实验装置中的B和C进行调换,将无法得出灰绿色物质是铜绿的结论,原因是______________ 。
【实验拓展】
(5)小黄同学还从网上找到了利用氨水擦拭去除铜绿的方法,其原理是氨水与碱式碳酸铜反应生成铜氨络离子[Cu(NH3)42+],其离子方程式可表示为:___________________________ 。
| 紫铜 | 青铜 | 铜绿 | |
| 主要成分 | 纯铜 | 铜锡合金 | Cu2(OH)2CO3 |
| 性质与用途 | 紫红色, 质软,导电性能良好;主要用作电线电缆。 | 多呈灰绿色, 熔点低、硬度大、 可塑性强;可铸造成各种器具。 | 不溶于水的灰绿色粉末,溶于酸, 加热易分解;可作颜料、杀虫剂。 |
针对铜制品表面的灰绿色物质究竟是什么,同学们提出了多种猜想并展开实验探究。
【猜想假设】
(1)小吴同学认为可能是纯铜制品表面涂上了灰绿色的油漆;
小周同学认为可能是青铜(铜锡合金),因为常见的青铜是灰绿色的;
小黄同学认为是纯铜制品,只是表面长出了铜绿[ Cu2(OH)2CO3];
除上述猜想外,其他合理的猜想是
【实验验证】三位同学为了验证各自上述的猜想,进行了以下探究:
(2)小吴刮下部分灰绿色物质放入燃烧匙中进行灼烧,发现该物质不能燃烧,证明灰绿色物质不是油漆。 其判断依据是
(3)小周刮下足量的灰绿色物质投入盐酸溶液中,观察到有气体产生,实验表明该气体不能燃烧。将表面刮净后的铜制品也投入盐酸中,并无气体产生。由此证明该铜制品不是青铜,理由是
(4)根据上述实验,小黄认为灰绿色物质可能是铜绿[ Cu2(OH)2CO3]。于是按图5所示装置进行实验。

实验证明小黄的猜测是正确的,因为在A中观察到灰绿色物质变黑,B中观察到了
如果将实验装置中的B和C进行调换,将无法得出灰绿色物质是铜绿的结论,原因是
【实验拓展】
(5)小黄同学还从网上找到了利用氨水擦拭去除铜绿的方法,其原理是氨水与碱式碳酸铜反应生成铜氨络离子[Cu(NH3)42+],其离子方程式可表示为:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】以硅孔雀石[主要成分为CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如下:
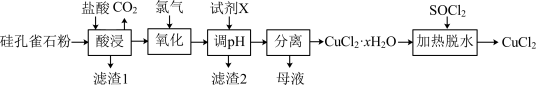
已知:①SOCl2+H2O SO2↑+2HCl↑
SO2↑+2HCl↑
②Ksp[Fe(OH)3]=4.0×10-38 Ksp[Fe(OH)2]=8.0×10-16 Ksp[Cu(OH)2]=2.2×10-20
(1)“酸浸”时盐酸与CuCO3•Cu(OH)2反应的化学方程式为__________________________ 。
(2)引用相关数据和物质性质说明“氧化”步骤在该流程中的必要性__________________________________________________ 。
(3)“调pH”步骤的目的是除去Fe3+,试剂X可以选择_____________ (填化学式,写出一种即可);若此时溶液中c(Cu2+)=2.2mol•L-1,则调节后溶液pH不得高于_____________ 。
(4)“加热脱水”时,加入SOCl2的作用是__________________________________________ 。

已知:①SOCl2+H2O
 SO2↑+2HCl↑
SO2↑+2HCl↑②Ksp[Fe(OH)3]=4.0×10-38 Ksp[Fe(OH)2]=8.0×10-16 Ksp[Cu(OH)2]=2.2×10-20
(1)“酸浸”时盐酸与CuCO3•Cu(OH)2反应的化学方程式为
(2)引用相关数据和物质性质说明“氧化”步骤在该流程中的必要性
(3)“调pH”步骤的目的是除去Fe3+,试剂X可以选择
(4)“加热脱水”时,加入SOCl2的作用是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】已知辉铜矿、软锰矿的主要成分如下表所示:
某化工厂拟以这两种矿石为原料采用湿法冶炼铜,工艺如下:
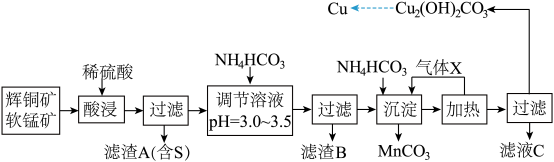
回答下列问题:
(1)气体 X 遇浓硝酸产生“白烟”,写出气体 X 的电子式:______________________________ 。
(2)提高“酸浸”速率的措施有______________________________ (填两条)。
(3)用离子方程式表示“酸浸”中 MnO2的作用:______________________________ ,被氧化的元素是______________________________ (填元素符号)。
(4)已知 CH3COONH4溶液呈中性,则常温下,NH4HCO3溶液 pH______________________________ (填“>”、“<”或“=”)7,理由是__________ 。
(5)从滤液 C 中可以提取一种化学肥料,它的化学式为_____________________________ 。
(6) 从溶液中析出的碱式碳酸铜可能带有结晶水,设其通式为 Cu2(OH)2CO3·xH2O。准确称取a g 样品,灼烧至恒重,称得 CuO 的质量,固体质量减轻 b g,则 x 为______________________________ 。
| 矿石 | 辉铜矿 | 软锰矿 |
| 主要成分 | Cu2S、Fe2O3、SiO2 | MnO2、SiO2 |
某化工厂拟以这两种矿石为原料采用湿法冶炼铜,工艺如下:

回答下列问题:
(1)气体 X 遇浓硝酸产生“白烟”,写出气体 X 的电子式:
(2)提高“酸浸”速率的措施有
(3)用离子方程式表示“酸浸”中 MnO2的作用:
(4)已知 CH3COONH4溶液呈中性,则常温下,NH4HCO3溶液 pH
(5)从滤液 C 中可以提取一种化学肥料,它的化学式为
(6) 从溶液中析出的碱式碳酸铜可能带有结晶水,设其通式为 Cu2(OH)2CO3·xH2O。准确称取a g 样品,灼烧至恒重,称得 CuO 的质量,固体质量减轻 b g,则 x 为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】氯碱工业中惰性电极电解饱和的食盐水的原理示意图如图所示:
(1)溶液A的溶质是_________________ 。(填化学式)
(2)电解饱和食盐水的离子方程式是________________________ 。
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用:___________________________ 。
(4)电解所用的盐水需要精制,去除有影响的的Ca 2+ 、Mg 2+ 、NH 4+和SO 42- [c(SO 42-)>c(Ca 2+ )]。精致流程如下(淡盐水和溶液A来电解池):
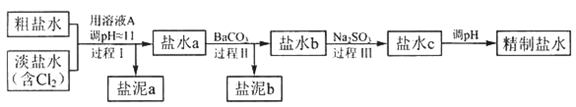
①盐泥a除泥沙外,还含有的物质是_________________ 。(填化学式)
②过程Ⅰ中将NH4+转化为N2的离子方程式是____________________ 。
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有_________________ 。(填离子符号)
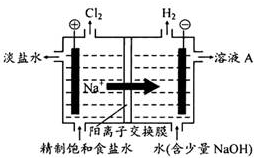
(1)溶液A的溶质是
(2)电解饱和食盐水的离子方程式是
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用:
(4)电解所用的盐水需要精制,去除有影响的的Ca 2+ 、Mg 2+ 、NH 4+和SO 42- [c(SO 42-)>c(Ca 2+ )]。精致流程如下(淡盐水和溶液A来电解池):

①盐泥a除泥沙外,还含有的物质是
②过程Ⅰ中将NH4+转化为N2的离子方程式是
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】电解含CH3COOH的有机废水也可获得清洁能源H2,原理如图所示。
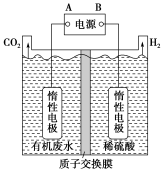
(1)B为电源_______ 极,电解时阳极的电极反应式为_______ 。
(2)下列物质的核磁共振氢谱不止一个吸收峰的是_______ (填序号)
①新戊烷 ②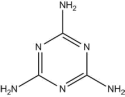 ③
③ ④金刚烷
④金刚烷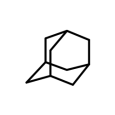
(3)写出丙酮的同分异构体中,核磁共振氢谱有三组峰,且峰面积之比为3:2:1的结构简式_______ 。

(1)B为电源
(2)下列物质的核磁共振氢谱不止一个吸收峰的是
①新戊烷 ②
 ③
③ ④金刚烷
④金刚烷
(3)写出丙酮的同分异构体中,核磁共振氢谱有三组峰,且峰面积之比为3:2:1的结构简式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某小组同学利用下图装置对电解氯化铜实验进行了研究。
(1)甲认为电解过程中阳极产生的_________ 是溶液变绿的原因。
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2++ 4Cl- [CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:
[CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:________________ 。
(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依据是________ ,否定乙的依据是________________ 。
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]-,[CuCl2]-掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]-的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]-掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]-的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是__________________ 。
② 写出b中生成[CuCl2]-的离子方程式:____________________ 。
③ 补充c中必要的操作及现象:____________________ 。
丙据此得出结论:电解时阴极附近生成[CuCl2]-是导致溶液变绿的原因。
| 装置 | 现象 |
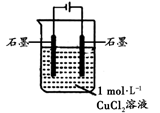 | 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,烧杯壁变热,溶液由蓝色变为绿色 |
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2++ 4Cl-
 [CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:
[CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
| 装置 | 现象 |
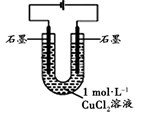 | 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色;U形管变热,冷却后阴极附近溶液仍为绿色 |
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]-,[CuCl2]-掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]-的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]-掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]-的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是
② 写出b中生成[CuCl2]-的离子方程式:
③ 补充c中必要的操作及现象:
丙据此得出结论:电解时阴极附近生成[CuCl2]-是导致溶液变绿的原因。
您最近一年使用:0次



