某反应在催化剂的作用下按以下两步进行:第一步为X+Y=Z;第二步为Y+Z=M+N+X。此反应的总的化学方程式是___ ,反应的催化剂是___ 。
更新时间:2020-11-10 05:55:31
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)已知25℃、101 kPa时:
①2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197 kJ/mol;
②H2O(g)=H2O(l) ΔH2=-44 kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式为__________ 。
(2)已知:温度过高时,WO2(s)转变为WO2(g):
①WO2(s)+2H2(g)⇌W(s)+2H2O(g) ΔH1=+66.0 kJ·mol-1
②WO2(g)+2H2(g)⇌W(s)+2H2O(g) ΔH2=-137.9 kJ·mol-1
则WO2(s)⇌WO2(g)的ΔH=__________ 。
①2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197 kJ/mol;
②H2O(g)=H2O(l) ΔH2=-44 kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式为
(2)已知:温度过高时,WO2(s)转变为WO2(g):
①WO2(s)+2H2(g)⇌W(s)+2H2O(g) ΔH1=+66.0 kJ·mol-1
②WO2(g)+2H2(g)⇌W(s)+2H2O(g) ΔH2=-137.9 kJ·mol-1
则WO2(s)⇌WO2(g)的ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】NO可直接用活性铁粉转化为N2,已知:N2(g)+O2(g)=2NO(g)ΔH1,4Fe(s)+3O2(g)=2Fe2O3(s) ΔH2,则6NO(g)+4Fe(s)=2Fe2O3(s)+3N2(g)ΔH=_____ (用“ΔH1”、“ΔH2”表示)。
您最近一年使用:0次
【推荐3】煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后再使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为
a.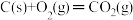 ΔH=E1①
ΔH=E1①
b.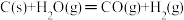 ΔH=E2②
ΔH=E2②
 ΔH=E3③
ΔH=E3③
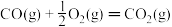 ΔH=E4④
ΔH=E4④
(1)上述四个热化学方程式中哪个反应的ΔH>0?______ (填序号)。
(2)等质量的煤分别通过以上两种不同的途径产生的可利用的总能量关系正确的是____ (填字母)。
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为E1=__________________ 。
(4)已知:①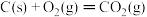 ΔH1=-393.5kJ/mol
ΔH1=-393.5kJ/mol
②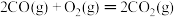 ΔH2=-566kJ/mol
ΔH2=-566kJ/mol
③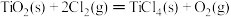 ΔH3=+141kJ/mol
ΔH3=+141kJ/mol
则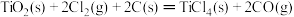 的ΔH=
的ΔH=_____________________ 。
a.
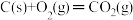 ΔH=E1①
ΔH=E1①b.
 ΔH=E2②
ΔH=E2② ΔH=E3③
ΔH=E3③ 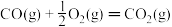 ΔH=E4④
ΔH=E4④(1)上述四个热化学方程式中哪个反应的ΔH>0?
(2)等质量的煤分别通过以上两种不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为E1=
(4)已知:①
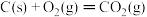 ΔH1=-393.5kJ/mol
ΔH1=-393.5kJ/mol②
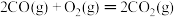 ΔH2=-566kJ/mol
ΔH2=-566kJ/mol③
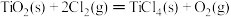 ΔH3=+141kJ/mol
ΔH3=+141kJ/mol 则
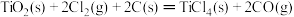 的ΔH=
的ΔH=
您最近一年使用:0次



