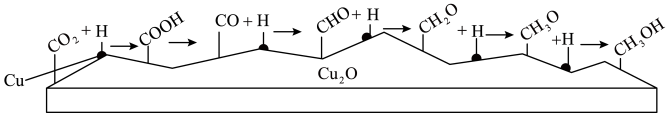
CO2加氢制CH4的一种催化机理如图,下列说法正确的是( )
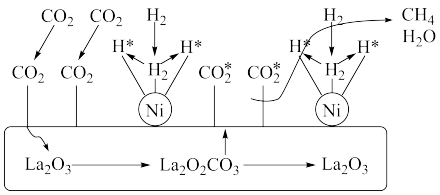

| A.催化过程使用的催化剂为La2O3和La2O2CO3 |
| B.La2O2CO3可以释放出CO2*(活化分子) |
| C.H2经过Ni活性中心裂解产生活化态H*的过程为放热过程 |
| D.CO2加氢制CH4的过程只需要La2O3催化即可完成 |
更新时间:2020-11-17 15:16:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组依据反应AsO43-+2H++2I- AsO33-+I2+H2O设计左下图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如右下图,下列有关叙述错误的是
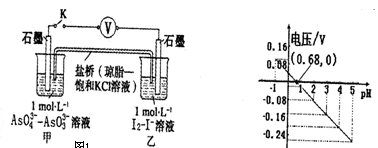

| A.pH>0.68时,甲烧杯中石墨为负极 |
| B.pH=0.68时,反应处于平衡状态 |
| C.pH>0.68时,氧化性I2>AsO43- |
| D.pH=5时,负极电极反应式为2I--2e-=I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于各图象的解释或得出结论正确的是






| A.图1表示0.10 mol·L−1 NaOH溶液滴定20.00 mL 0.10 mol·L−1醋酸溶液的滴定曲线 |
| B.用0.1 mol·L−1NaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸溶液,图2中实线表示的是滴定醋酸的曲线 |
| C.根据图3所示可知:N2O(g)+NO(g)===N2(g)+NO2(g) ΔH=+139 kJ·mol−1 |
| D.图4表示某温度时,BaSO4在水中的沉淀溶解平衡曲线,蒸发水可使溶液由b点变到a点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.1molH2与0.5molO2反应放出的热量就是H2的燃烧热 |
| B.已知含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)= CH3COONa(aq)+H2O(l)△H=-57.4 kJ·mol-1 |
| C.已知2C(s)+2O2=(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
| D.使用氢气作燃料有助于控制温室效应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知 和
和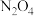 存在平衡:
存在平衡:
 。下列分析正确的是
。下列分析正确的是
 和
和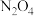 存在平衡:
存在平衡:
 。下列分析正确的是
。下列分析正确的是A. 平衡混合气体中含 平衡混合气体中含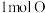 原子 原子 |
| B.恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
| C.恒容时,水浴加热`该平衡正向移动,气体颜色变浅 |
D.断裂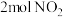 中的共价键所需能量小于断裂 中的共价键所需能量小于断裂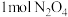 中的共价键所需能量 中的共价键所需能量 |
您最近一年使用:0次
【推荐3】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜催化剂上的反应机理和能量图如图:下列说法正确的是
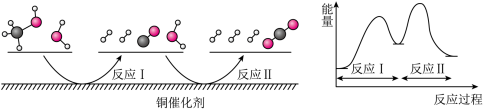

| A.选择优良的催化剂降低反应I和II的活化能,有利于减少过程中的能耗 |
| B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量 |
| C.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
| D.反应II的热化学方程式为CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=+akJ/mol(a>0) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列有关叙述正确的是( )
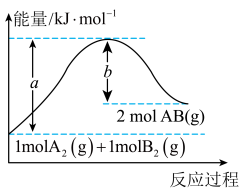

| A.每生成2molAB(g)吸收bkJ热量 |
| B.该反应中反应物的总能量高于生成物的总能量 |
| C.反应热ΔH=+(a-b)kJ/mol |
| D.形成1molA-A键和1molB-B键,吸收akJ能量 |
您最近一年使用:0次
【推荐2】键能是气态原子形成1mol化学键释放的最低能量。键能的大小可以衡量化学键的强弱,也可以用于计算化学反应的反应热。下表是一些化学键的键能:
根据键能数据计算每消耗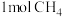 时,反应
时,反应 的
的 为
为
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ/mol) | 414 | 489 | 565 | 155 |
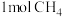 时,反应
时,反应 的
的 为
为| A.-1940kJ∙mol-1 | B.+1940 kJ∙mol-1 | C.-485 kJ∙mol-1 | D.+485 kJ∙mol-1 |
您最近一年使用:0次

 2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率以及H2的平衡转化率均增大
2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率以及H2的平衡转化率均增大 ,在水溶液中用H原子将
,在水溶液中用H原子将 高效还原为甲醇的反应机理如图所示。下列说法错误的是
高效还原为甲醇的反应机理如图所示。下列说法错误的是