按要求填空:
(1)制备Fe(OH)3胶体的化学反应方程式:_________ 。
(2)制备Fe(OH)3胶体的实验具体操作_____________
(3)工业制备漂白粉化学方程式___________
(4)漂白粉失效化学方程式______________
(5)写出下列反应离子方程式
①Ba(OH)2+H2SO4_________
②醋酸与一水合氨_________
③Na+H2O_________
④CO2+NaOH_________
⑤CaCO3+HCl_________
⑥CH3COONa+H2SO4_________
⑦Ca(HCO3)2+NaOH(少量)_________
(6)写出下列电解质在水中的电离方程式
①碳酸_________
②一水合氨_________
③硫酸_________
④硫酸氢钠_________
⑤碳酸氢钠_________
⑥硫酸钡_________
⑦醋酸_________
(1)制备Fe(OH)3胶体的化学反应方程式:
(2)制备Fe(OH)3胶体的实验具体操作
(3)工业制备漂白粉化学方程式
(4)漂白粉失效化学方程式
(5)写出下列反应离子方程式
①Ba(OH)2+H2SO4
②醋酸与一水合氨
③Na+H2O
④CO2+NaOH
⑤CaCO3+HCl
⑥CH3COONa+H2SO4
⑦Ca(HCO3)2+NaOH(少量)
(6)写出下列电解质在水中的电离方程式
①碳酸
②一水合氨
③硫酸
④硫酸氢钠
⑤碳酸氢钠
⑥硫酸钡
⑦醋酸
更新时间:2020-11-10 13:54:27
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列物质在水溶液中的电离方程式
(1)CuSO4:_____________ 。
(2)FeCl3:__________ 。
(3)(NH4)2CO3:____________ 。
(4)NaHSO4:___________ 。
(1)CuSO4:
(2)FeCl3:
(3)(NH4)2CO3:
(4)NaHSO4:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列10种物质:①铁 ②蔗糖固体 ③盐酸 ④熔融CaO ⑤NaHCO3溶液 ⑥CO2 ⑦熔融NaOH ⑧氢氧化铁胶体 ⑨无水酒精 ⑩FeCl3固体
(1)上述物质属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(2)NaHSO4在水溶液中的电离方程式:_______ 。
(3)少量CO2通入澄清石灰水反应的离子方程式:_______ 。
(4)NaHCO3与NaHSO4溶液反应的离子方程式:_______ 。
(5)实验室制备氢氧化铁胶体的化学方程式:_______ 。
(1)上述物质属于电解质的有
(2)NaHSO4在水溶液中的电离方程式:
(3)少量CO2通入澄清石灰水反应的离子方程式:
(4)NaHCO3与NaHSO4溶液反应的离子方程式:
(5)实验室制备氢氧化铁胶体的化学方程式:
您最近一年使用:0次
【推荐3】回答下列问题:
(1)已知乙醇能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O。Cr2O 和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
①写出Cr2(SO4)3的电离方程式:___ 。
②该反应___ (填“是”或“不是”)氧化还原反应,判断的依据是___ 。
③这一反应可用来检测司机是否酒后驾,简述其原理:___ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是___ ;若反应中转移了0.3mol电子,则氧化产物的质量是___ g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱顺序为___ 。足量Cl2通入FeBr2溶液中发生反应的离子方程式为___ 。
(1)已知乙醇能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O。Cr2O
 和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+在溶液中分别显橙色和绿色,回答下列问题:①写出Cr2(SO4)3的电离方程式:
②该反应
③这一反应可用来检测司机是否酒后驾,简述其原理:
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有_______
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)请写出一个既属于离子反应、置换反应又属于氧化还原反应的反应方程式_______ 。
(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在有
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)请写出一个既属于离子反应、置换反应又属于氧化还原反应的反应方程式
(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)写出下列化学反应的离子方程式
①氢氧化钡溶液和硫酸溶液反应_______
②碳酸钙和足量稀盐酸反应_______
(2)根据下列离子方程式,各写一个符合条件的化学方程式
①Zn+2H+=Zn2++H2↑_______
②HCO + H+=CO2↑+ H2O
+ H+=CO2↑+ H2O _______
①氢氧化钡溶液和硫酸溶液反应
②碳酸钙和足量稀盐酸反应
(2)根据下列离子方程式,各写一个符合条件的化学方程式
①Zn+2H+=Zn2++H2↑
②HCO
 + H+=CO2↑+ H2O
+ H+=CO2↑+ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是___________ 。
(2)属于电解质的是___________ 。
(3)属于非电解质的是___________ 。
(4)②在水溶液中的电离方程式为___________ ,①与②在溶液中反应使溶液呈中性的离子方程式为___________ 。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是___________ 。
II.该反应中氧化剂与还原剂的数目比为___________ 。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)②在水溶液中的电离方程式为
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是
II.该反应中氧化剂与还原剂的数目比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填“SiO2”或“Si”)
(2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用。已知“84”消毒液的制备原理为Cl2 + 2NaOH=NaCl+NaClO + H2O,则“84”消毒液的有效成分为___________ (填“NaCl”或“NaClO”)
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO N2 +2
N2 +2 ___________ 。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用。已知“84”消毒液的制备原理为Cl2 + 2NaOH=NaCl+NaClO + H2O,则“84”消毒液的有效成分为
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO
 N2 +2
N2 +2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式___________ 。
(2)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式___________ 。
②下列收集Cl2的正确装置是___________ 。
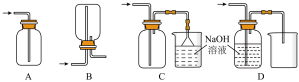
③将灼热的铜丝伸入盛有氯气的集气瓶中,反应的方程式为___________ 。将反应后的产物溶于水配成饱和溶液,向溶液中加入一小块金属钠,发生反应的离子方程式为________ 、_________ 。
④某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:
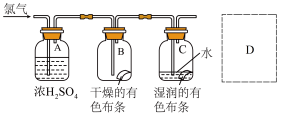
i.浓H2SO4的作用是___________ 。
ii.与研究目的直接相关的实验现象是___________ 。
iii.该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入烧碱溶液以除去多余的氯气,该反应的离子方程式为___________ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式
(2)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式
②下列收集Cl2的正确装置是

③将灼热的铜丝伸入盛有氯气的集气瓶中,反应的方程式为
④某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

i.浓H2SO4的作用是
ii.与研究目的直接相关的实验现象是
iii.该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入烧碱溶液以除去多余的氯气,该反应的离子方程式为
您最近一年使用:0次



