图中,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请根据图示回答下列问题:

(1)写出反应①的离子方程式:_________ 。
(2)写出反应②的化学方程式:_________ 。
(3)实验室制取A的离子反应方程式为__________ 。A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是_____________ (用化学方程式表示)。

(1)写出反应①的离子方程式:
(2)写出反应②的化学方程式:
(3)实验室制取A的离子反应方程式为
更新时间:2020-11-11 09:46:11
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C三种常见单质,其有关反应如图所示:
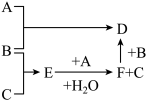
已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血红色。
(1)写出B与水反应的离子方程式_______________________________
(2)A+B→D反应化学方程式___________________________________
(3)F→D的离子方程式是:____________________________________

已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血红色。
(1)写出B与水反应的离子方程式
(2)A+B→D反应化学方程式
(3)F→D的离子方程式是:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色试验均为黄色。
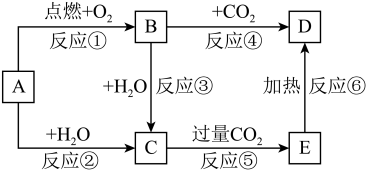
请填写下列空白:
(1)写出下列化学式:B_______ ,C_______ ,E_______ 。
(2)反应②③⑤⑥中_______ (填序号)属于氧化还原反应。
(3)完成下列方程式。
①写出反应②的离子方程式:_______ 。
②写出反应④的化学方程式:_______ 。

请填写下列空白:
(1)写出下列化学式:B
(2)反应②③⑤⑥中
(3)完成下列方程式。
①写出反应②的离子方程式:
②写出反应④的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E五种物质均为中学化学中常见的化合物,已知A、B、C、D、 E五种物质里含有相同的一种金属元素。并且A、B、C、D都可与物质M反应生成E;N是气体,物质之间按箭头方向都可通过一步反应实现转化。实验室通常用碱B检验 CO2,回答下列问题:
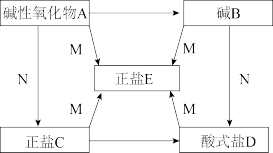
(1)写出物质的化学式A_______ B_______ C _______ D _______
(2)选择用“酸、碱、盐、酸性氧化物或碱性氧化物”填空,M属于_______ ,N属于_______
(3)向碱B的澄清溶液中逐渐通入N,最终转化为酸式盐D的过程中,发生反应的离子方程式_______

(1)写出物质的化学式A
(2)选择用“酸、碱、盐、酸性氧化物或碱性氧化物”填空,M属于
(3)向碱B的澄清溶液中逐渐通入N,最终转化为酸式盐D的过程中,发生反应的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】在实验室制取氯气的实验中:
(1)制法反应原理(方程式)为__________________ ;
(2)实验装置如图所示
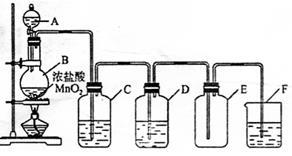
指出下列装置中所盛试剂及其作用:
C.____________ ______________________________
D.____________ ____________________________
F.____________ ___________________________
(1)制法反应原理(方程式)为
(2)实验装置如图所示

指出下列装置中所盛试剂及其作用:
C.
D.
F.
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为了“探究铁及其化合物的氧化性或还原性”,某同学甲设计了如下的实验方案。
(1)实验前甲同学预测:Fe2+肯定既有还原性又有氧化性。你认为甲同学预测的依据是______ 。
(2)甲同学欲用实验证明他的预测。实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1 mol·L-1 FeCl2溶液、KSCN溶液、新制氯水。
①若甲同学计划在0.1 mol·L-1 FeCl2溶液中滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是___________ (写化学方程式),现象是:溶液由浅绿色变__ 色。
②实验中,甲同学发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据。你认为可选上述试剂中的___ 滴入甲同学所得的混合液中,出现_______ 现象,证明甲同学的观点和实验方案都是正确的。
③对于证明Fe2+具有氧化性,甲同学认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小,由此说明三种金属的还原性由强至弱的顺序为_____ 。
(1)实验前甲同学预测:Fe2+肯定既有还原性又有氧化性。你认为甲同学预测的依据是
(2)甲同学欲用实验证明他的预测。实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1 mol·L-1 FeCl2溶液、KSCN溶液、新制氯水。
①若甲同学计划在0.1 mol·L-1 FeCl2溶液中滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是
②实验中,甲同学发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据。你认为可选上述试剂中的
③对于证明Fe2+具有氧化性,甲同学认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小,由此说明三种金属的还原性由强至弱的顺序为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】碳酸亚铁(FeCO3)是生产补血剂的重要原料,制取碳酸亚铁的过程中涉及以下探究实验。
实验一:
为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如图实验。
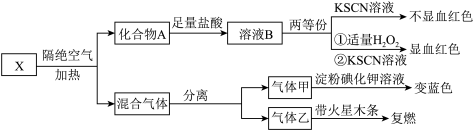
已知:气体甲、气体乙均为单质。
请回答:
(1)气体甲与碘化钾溶液反应的离子方程式为____ 。
(2)化合物X含有的元素为____ (写元素符号)。
(3)化合物A的化学式为____ 。
实验二:
如图装置,利用实验一所得溶液B制取FeCO3(白色固体,难溶于水):
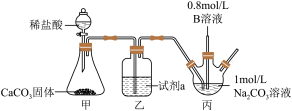
装置丙中,先向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,再滴加一定量B溶液产生白色沉淀和无色气体(离子方程式为Fe2++2HCO =FeCO3↓+CO2↑+H2O),过滤、洗涤、干燥,得到FeCO3固体。
=FeCO3↓+CO2↑+H2O),过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(4)乙装置中的试剂a是____ ,作用是____ 。
(5)向Na2CO3溶液通入的CO2目的是____ 。
(6)不可用酸性高锰酸钾溶液检验溶液B中的金属正离子的原因是:____ 。
(7)100mL0.8mol/LB溶液完全反应,最终得到5.568gFeCO3固体,则产率为____ 。
实验一:
为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如图实验。

已知:气体甲、气体乙均为单质。
请回答:
(1)气体甲与碘化钾溶液反应的离子方程式为
(2)化合物X含有的元素为
(3)化合物A的化学式为
实验二:
如图装置,利用实验一所得溶液B制取FeCO3(白色固体,难溶于水):

装置丙中,先向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,再滴加一定量B溶液产生白色沉淀和无色气体(离子方程式为Fe2++2HCO
 =FeCO3↓+CO2↑+H2O),过滤、洗涤、干燥,得到FeCO3固体。
=FeCO3↓+CO2↑+H2O),过滤、洗涤、干燥,得到FeCO3固体。请回答:
(4)乙装置中的试剂a是
(5)向Na2CO3溶液通入的CO2目的是
(6)不可用酸性高锰酸钾溶液检验溶液B中的金属正离子的原因是:
(7)100mL0.8mol/LB溶液完全反应,最终得到5.568gFeCO3固体,则产率为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,G为黄绿色气体单质,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,它们之间的相互转化关系如图,其他与题无关的生成物均已略去。请回答下列问题:
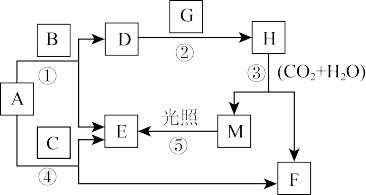
(1)写出D、G的化学式D:_________ ,G:_________ 。
(2)H是“84”消毒液的主要成分,写出反应③的化学方程式_________ 。
(3)A→E的转化在实际中的应用是_________ 。
(4)在滴入几滴无色酚酞的F溶液中逐滴加入 溶液,观察到的现象是
溶液,观察到的现象是_________ 。
(5)写出反应⑤的化学方程式_________ ,由此得出M的保存方法为_________ 。

(1)写出D、G的化学式D:
(2)H是“84”消毒液的主要成分,写出反应③的化学方程式
(3)A→E的转化在实际中的应用是
(4)在滴入几滴无色酚酞的F溶液中逐滴加入
 溶液,观察到的现象是
溶液,观察到的现象是(5)写出反应⑤的化学方程式
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】为抑制新冠病毒传播,含氯消毒剂被广泛使用。常见的含氯消毒剂有次氯酸盐、ClO2、有机氯化物等。用NaCl电解法生成ClO2的工艺原理示意图如图,发生器内电解生成ClO2。
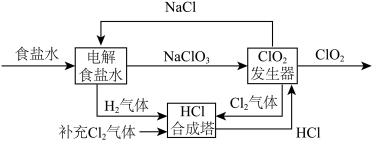
完成下列填空:
(1)Cl原子的最外层电子层上具有_____ 种不同能量的电子;HClO的电子式是_________ ;
(2)Cl2性质活泼,易形成多种化合物。请说明NaCl的熔沸点比HCl高的原因:_________________________
(3)根据示意图,补充并配平ClO2发生器中发生的化学反应方程式:_____ 。
_____NaClO3+_____HCl =_____+_____H2O
若反应中有2mol电子发生转移,则生成ClO2_____ mol。
(4)某兴趣小组通过实验测定不同pH环境中,相同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
①NaClO溶液呈碱性的原因是_________________________ (用离子方程式表示)。
②调节NaClO溶液pH时不能选用盐酸的原因为________________ 。
③由表中数据可推断,该实验得到的结论是_____________________
④家用消毒常用84消毒液而不采用次氯酸,说明其理由。_______________

完成下列填空:
(1)Cl原子的最外层电子层上具有
(2)Cl2性质活泼,易形成多种化合物。请说明NaCl的熔沸点比HCl高的原因:
(3)根据示意图,补充并配平ClO2发生器中发生的化学反应方程式:
_____NaClO3+_____HCl =_____+_____H2O
若反应中有2mol电子发生转移,则生成ClO2
(4)某兴趣小组通过实验测定不同pH环境中,相同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
NaClO溶液浓度/ (mg·L-1) | 不同pH下的细菌杀灭率/% | ||
pH=4.0 | pH=6.5 | pH=9.0 | |
250 | 98.90 | 77.90 | 53.90 |
①NaClO溶液呈碱性的原因是
②调节NaClO溶液pH时不能选用盐酸的原因为
③由表中数据可推断,该实验得到的结论是
④家用消毒常用84消毒液而不采用次氯酸,说明其理由。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持已略),实验装置如图:

回答下列问题:
(1)①装置A中是用 和浓盐酸反应制备
和浓盐酸反应制备 ,写出其化学反应方程式(并用双线桥标出电子转移的方向与数目):
,写出其化学反应方程式(并用双线桥标出电子转移的方向与数目):_______ 。
②若反应产生标准状况下4.48L ,则方程式中转移的电子数为
,则方程式中转移的电子数为_______ 。
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出C发生堵塞时B中的现象:____ 。
(3)设置装置C的实验目的是验证氯气是否具有漂白性,为此C中的I、II、III依次应放入_______ (从下表a、b、c、d中选择)。
(4)装置G有_______ 作用,发生的离子方程式是_______ 。
(5)装置E中潮湿的 与
与 以等物质的量反应,生成
以等物质的量反应,生成 、气体
、气体 和另一种盐,试写出该反应化学方程式:
和另一种盐,试写出该反应化学方程式:_______ 。
(6)某同学设计实验探究84消毒液的漂白性。
I.在2mL 84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.在2mL 84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱,ORP值越大,氧化性越强。
①实验I、II现象不同的原因是为_______ 。
②实验III中,随时间的变化ORP值不同的原因可能是_______ 。

回答下列问题:
(1)①装置A中是用
 和浓盐酸反应制备
和浓盐酸反应制备 ,写出其化学反应方程式(并用双线桥标出电子转移的方向与数目):
,写出其化学反应方程式(并用双线桥标出电子转移的方向与数目):②若反应产生标准状况下4.48L
 ,则方程式中转移的电子数为
,则方程式中转移的电子数为(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出C发生堵塞时B中的现象:
(3)设置装置C的实验目的是验证氯气是否具有漂白性,为此C中的I、II、III依次应放入
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)装置E中潮湿的
 与
与 以等物质的量反应,生成
以等物质的量反应,生成 、气体
、气体 和另一种盐,试写出该反应化学方程式:
和另一种盐,试写出该反应化学方程式:(6)某同学设计实验探究84消毒液的漂白性。
I.在2mL 84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.在2mL 84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱,ORP值越大,氧化性越强。
①实验I、II现象不同的原因是为
②实验III中,随时间的变化ORP值不同的原因可能是
您最近半年使用:0次
【推荐1】如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质,试推出各物质的化学式,并写出B→C、A→D反应的化学方程式。
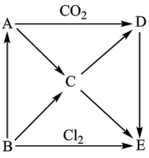
(1)各物质的化学式:A___ ,D___ 。
(2)写出B→C、A→D反应的化学方程式:
B→C:____ 。
A→D:____ 。
(3)将3.9 g A投入到足量的水中充分反应,生成的气体在标准状况下的体积为___ L,将反应后的溶液配成1000 mL溶液,所得溶液的物质的量浓度为___ 。

(1)各物质的化学式:A
(2)写出B→C、A→D反应的化学方程式:
B→C:
A→D:
(3)将3.9 g A投入到足量的水中充分反应,生成的气体在标准状况下的体积为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某些资料认为NO不能与Na2O2反应。有同学提出质疑,他认为NO易与O2发生反应,应该更容易被Na2O2氧化。
查阅资料:a.2NO+Na2O2=2NaNO2
b.6NaNO2+3H2SO4(稀)=3Na2SO4+2HNO3+4NO↑+2H2O
c.酸性条件下,NO能被MnO4-氧化成NO3-
该同学利用如图中装置来探究NO与Na2O2的反应(装置可重复使用)。
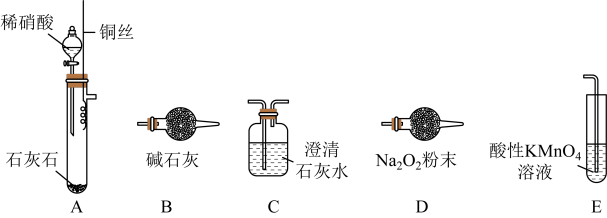
(1)装置连接的顺序为A→_______________ ,A中生成NO的化学方程式____________ ;
(2)装置C的作用是_________________ ;
(3)装置E的作用是_________________ ,发生反应的离子方程式为______________ ;
(4)充分反应后,检验D装置中是否生成了NaNO2的实验操作是______________________ 。
查阅资料:a.2NO+Na2O2=2NaNO2
b.6NaNO2+3H2SO4(稀)=3Na2SO4+2HNO3+4NO↑+2H2O
c.酸性条件下,NO能被MnO4-氧化成NO3-
该同学利用如图中装置来探究NO与Na2O2的反应(装置可重复使用)。
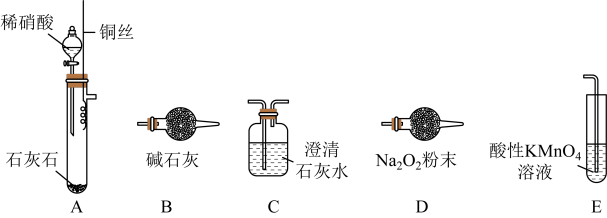
(1)装置连接的顺序为A→
(2)装置C的作用是
(3)装置E的作用是
(4)充分反应后,检验D装置中是否生成了NaNO2的实验操作是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
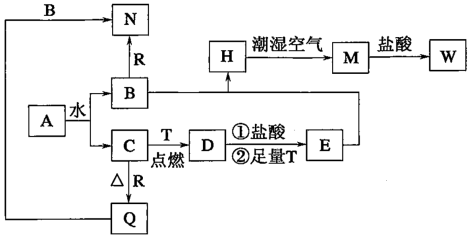
(1)写出下列物质的化学式:A:_______ ,D:_______ ,R:_______ 。
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式:_______ ;
B和R反应生成N的离子方程式:_______ ;
D与盐酸反应的离子方程式:_______ 。
(3)向W溶液中加入一定量T后,为检验所得溶液中金属阳离子,甲、乙两位同学做了如下实验:甲同学取出少量反应后溶液,加入少量H2O2,再滴加几滴KSCN溶液,发现溶液显血红色,由此得出结论有Fe2+;乙同学取出少量反应后溶液,加入少量酸性KMnO4溶液,发现酸性KMnO4溶液褪色,由此得出结论有Fe2+。丙同学看了实验过程后认为甲、乙同学的结论都有问题,你觉得丙同学判断甲、乙同学结论的依据是:
甲同学:_______ ;
乙同学:_______ 。

(1)写出下列物质的化学式:A:
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式:
B和R反应生成N的离子方程式:
D与盐酸反应的离子方程式:
(3)向W溶液中加入一定量T后,为检验所得溶液中金属阳离子,甲、乙两位同学做了如下实验:甲同学取出少量反应后溶液,加入少量H2O2,再滴加几滴KSCN溶液,发现溶液显血红色,由此得出结论有Fe2+;乙同学取出少量反应后溶液,加入少量酸性KMnO4溶液,发现酸性KMnO4溶液褪色,由此得出结论有Fe2+。丙同学看了实验过程后认为甲、乙同学的结论都有问题,你觉得丙同学判断甲、乙同学结论的依据是:
甲同学:
乙同学:
您最近半年使用:0次



