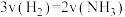一定能增加反应物分子中活化分子的百分数的是( )
| A.降低温度 | B.增大压强 |
| C.使用催化剂 | D.增加浓度 |
9-10高二·吉林长春·阶段练习 查看更多[14]
天津市第九十五中学益中学校2023-2024学年高二上学期12月月考化学试题天津市西青区杨柳青第一中学2021-2022高二上学期期中考试化学试题甘肃省兰州市第一中学2020-2021学年高二上学期期中考试化学(理)试题(已下线)2.1.2 活化能(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)吉林省油田第十一中学2019-2020学年高二上学期第一次月考化学试题【全国百强校】贵州省遵义市第四中学2018-2019学年高二上学期第一次月考化学试题2【全国百强校】贵州省遵义市第四中学2018-2019学年高二上学期第一次月考化学试题1宁夏育才中学2017-2018学年高二上学期期中考试化学试题宁夏育才中学2017-2018学年高二上学期期中化学试题(已下线)2010-2011学年浙江省兰溪一中高二下学期期中考试化学试卷2016-2017学年陕西省宝鸡市岐山县高二上期中理化学卷2016-2017学年陕西省宝鸡中学高二上月考一化学卷)(已下线)2010年青海省青海师大附中高二上学期期中考试化学试卷(已下线)吉林省长春外国语学校2010-2011学年高二第一次月考化学试题
更新时间:2020-11-12 17:46:34
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
| A.相同规格的Fe和Mg分别与0.1mol•L-1的盐酸反应,反应速率相同 |
| B.0.1mol•L-1的盐酸与0.1mol•L-1CH3COOH分别与大小、形状相同的大理石反应,反应速率相同 |
| C.催化剂能降低分子活化时所需能量,使活化分子百分数大大增加 |
| D.100mL2mol•L-1的盐酸与锌片反应,加入适量的NaCl固体,反应速率增大 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.活化分子具有的能量叫做活化能 |
| B.活化分子之间发生的碰撞一定为有效碰撞 |
| C.若反应的活化能接近零,当反应物接触时瞬间完成反应 |
| D.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积)或者升高温度,可增加活化分子的百分数,从而使反应速率增大 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关说法正确的是
| A.氨气催化氧化制硝酸属于氮的固定 |
| B.将食品放入冰箱保存,降低了体系的活化分子百分数 |
| C.铝热反应需要在高温下进行,故该反应为吸热反应 |
| D.测量中和反应反应热时,盐酸与氢氧化钠溶液应分多次加入量热计中 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】近日,大连理工大学在《ACS Catal》发文称:合成了一种B/N共掺杂多孔碳纳米管负载的Mo单原子位点(Mo/BCN),该材料在室温下能将 高效电还原为
高效电还原为 。相关机理如图2所示(图1为碳纳米管):
。相关机理如图2所示(图1为碳纳米管):

下列叙述正确的是
 高效电还原为
高效电还原为 。相关机理如图2所示(图1为碳纳米管):
。相关机理如图2所示(图1为碳纳米管):
下列叙述正确的是
| A.碳纳米管是一种新型高分子化合物材料 | B.碳纳米管参杂B、N的过程属于物理变化 |
C.该材料能降低 成为活化分子所需要的能量 成为活化分子所需要的能量 | D.该过程属于氮的固定中的自然固氮 |
您最近半年使用:0次

 ,发生反应
,发生反应
 ,下列说法正确的是
,下列说法正确的是