在一定条件下,用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又可以经此反应的逆反应,生成颗粒很细的铁粉。某校化学小组利用下图所列装置进行铁与水反应的实验,并利用产物进一步与四氧化三铁反应制取铁粉。(装置中的铁架台、铁夹等必要的夹持仪器在图中均已略去)
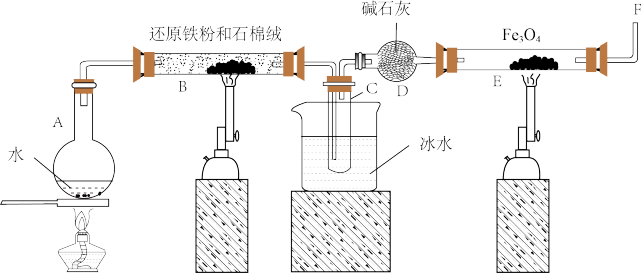
(1)烧瓶A中常加入碎瓷片,其作用是___________________ ,小试管C的作用是______________________________ 。
(2)为了安全,在E管中的反应发生前,在F出口处必须_________________ ,E管中的反应开始后,在F出口处应______________________ 。
(3)反应3Fe+4H2O(g) Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释_____________________ 。
(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象______________________ 。
(5)若E管中反应按以下两步进行:Fe3O4+H2 3FeO+H2O,FeO+H2
3FeO+H2O,FeO+H2 Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为
Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为________ (填序号)
①Fe ②Fe和Fe3O4 ③FeO和Fe3O4④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉________ g。(不考虑空气中的成分参与反应)

(1)烧瓶A中常加入碎瓷片,其作用是
(2)为了安全,在E管中的反应发生前,在F出口处必须
(3)反应3Fe+4H2O(g)
 Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象
(5)若E管中反应按以下两步进行:Fe3O4+H2
 3FeO+H2O,FeO+H2
3FeO+H2O,FeO+H2 Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为
Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为①Fe ②Fe和Fe3O4 ③FeO和Fe3O4④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉
更新时间:2020-11-19 15:04:23
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】为测定铝热反应实验所得“铁块”的成分,某学生兴趣小组设计实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
(1)取溶解操作得到的溶液,向其中滴加KSCN溶液,发现溶液变血红色。出现这种现象的原因,除了可能混有没反应完的氧化铁外,还有一个原因是_______________ 。
(2)沉铁操作应调节溶液pH的范围的为________ ,试剂B 选择______ 。(填序号)
a.稀盐酸 b.氧化铁 c.MgCO3固体 d.氨水
(3)已知常温下Fe(OH)3的Ksp=1.1×10-36,则铁完全沉淀时溶液中c(Fe3+)=_____ mol/L。
(4)根据流程得到的固体M质量_____ (填“能”或“不能”)计算出铁块中金属铁的质量,原因是________________ 。
(5)另有小组采用滴定的方式测定“铁块”中铁的含量(铁元素只存在Fe和Fe2O3),测定方式如下:
I.取10g“铁块”粉碎,加入足量氢氧化钠溶液充分反应,过滤、洗涤、干燥,得到8.88g固体。将固体加入足量盐酸溶解,获得200mL溶液A;
II.取出10mL 溶液A 于锥形瓶,先加入足量的SnCl2溶液,将Fe3+全部转化为Fe2+,除去过量的Sn2+;
III.加入一定量的硫酸和磷酸,并滴加指示剂。再向锥形瓶中滴加0.1000mol/LK2Cr2O7溶液,恰好完全反应时,共消耗12.50mL K2Cr2O7溶液。发生反应:Cr2O72-+6Fe2++14H+==2Cr3++6Fe3++7H2O
①步骤I中加入足量氢氧化钠溶液的作用为________________________ 。
②请计算样品中Fe单质的质量分数__________ (写出计算过程)。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
(2)沉铁操作应调节溶液pH的范围的为
a.稀盐酸 b.氧化铁 c.MgCO3固体 d.氨水
(3)已知常温下Fe(OH)3的Ksp=1.1×10-36,则铁完全沉淀时溶液中c(Fe3+)=
(4)根据流程得到的固体M质量
(5)另有小组采用滴定的方式测定“铁块”中铁的含量(铁元素只存在Fe和Fe2O3),测定方式如下:
I.取10g“铁块”粉碎,加入足量氢氧化钠溶液充分反应,过滤、洗涤、干燥,得到8.88g固体。将固体加入足量盐酸溶解,获得200mL溶液A;
II.取出10mL 溶液A 于锥形瓶,先加入足量的SnCl2溶液,将Fe3+全部转化为Fe2+,除去过量的Sn2+;
III.加入一定量的硫酸和磷酸,并滴加指示剂。再向锥形瓶中滴加0.1000mol/LK2Cr2O7溶液,恰好完全反应时,共消耗12.50mL K2Cr2O7溶液。发生反应:Cr2O72-+6Fe2++14H+==2Cr3++6Fe3++7H2O
①步骤I中加入足量氢氧化钠溶液的作用为
②请计算样品中Fe单质的质量分数
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】从铬锰矿渣(主要成分为 、MnO,杂质为
、MnO,杂质为 、
、 、
、 )中分离铬、锰的一种工艺流程如图所示:
)中分离铬、锰的一种工艺流程如图所示:
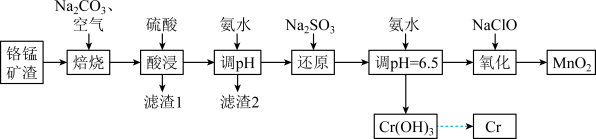
该工艺中,部分氢氧化物开始沉淀时和完全沉淀时的pH见下表:
回答下列问题:
(1)“焙烧”时空气是从焙烧炉下部进入,而矿渣粉是从上部投入的,这样做的优点是___________ 。
(2)“焙烧”中氧化产物只有 ,则相应反应中消耗的氧化剂与还原剂的物质的量之比为
,则相应反应中消耗的氧化剂与还原剂的物质的量之比为___________ ,“焙烧”中有___________ (填化学式)气体生成。
(3)第一次“调pH”时,理论上pH的最佳值是___________ 。“氧化”反应的离子方程式为___________ 。
(4)由 制备Cr的主要过程是灼烧
制备Cr的主要过程是灼烧 得到
得到 ,然后用铝热法还原
,然后用铝热法还原 得到Cr,则铝热法制备Cr的化学方程式为
得到Cr,则铝热法制备Cr的化学方程式为___________ 。
 、MnO,杂质为
、MnO,杂质为 、
、 、
、 )中分离铬、锰的一种工艺流程如图所示:
)中分离铬、锰的一种工艺流程如图所示:
该工艺中,部分氢氧化物开始沉淀时和完全沉淀时的pH见下表:
| 沉淀物 |  |  |  |  |
| 开始沉淀时的pH | 2.7 | 4.2 | 4.5 | 8.1 |
| 完全沉淀时的pH | 3.5 | 5.2 | 6.2 | 10.1 |
(1)“焙烧”时空气是从焙烧炉下部进入,而矿渣粉是从上部投入的,这样做的优点是
(2)“焙烧”中氧化产物只有
 ,则相应反应中消耗的氧化剂与还原剂的物质的量之比为
,则相应反应中消耗的氧化剂与还原剂的物质的量之比为(3)第一次“调pH”时,理论上pH的最佳值是
(4)由
 制备Cr的主要过程是灼烧
制备Cr的主要过程是灼烧 得到
得到 ,然后用铝热法还原
,然后用铝热法还原 得到Cr,则铝热法制备Cr的化学方程式为
得到Cr,则铝热法制备Cr的化学方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】I.天宫二号空间实验室已于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是___________ (填化学式),该物质的类别属于_______ (填“碱性氧化物”或“酸性氧化物”),实验室中不能用玻璃塞的试剂瓶盛放KOH溶液,原因是___________________ (用离子方程式表示)。
(2)太阳能电池帆板是“天宫二号”空间运行的动力。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光太阳能电池,该电池的核心材料是_______ ,其能量转化方式为____________________ 。
II.铝和氢氧化钾都是重要的工业产品。
请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是____________________ 。
(2)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有____________ (填序号)。
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,________ (填“能”或“不能”)说明固体混合物中无Fe2O3,若能,则不用填写理由,若不能,理由是(用离子方程式说明)___________________ 。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)太阳能电池帆板是“天宫二号”空间运行的动力。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光太阳能电池,该电池的核心材料是
II.铝和氢氧化钾都是重要的工业产品。
请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是
(2)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】已知在温度低于570℃ 时,还原铁粉与水蒸气反应的产物是FeO;高于570℃ 时,生成Fe3O4。老师用下图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
试回答下列问题:
(1)湿棉花的作用是______________ 。
(2)写出高于570℃ 时,Fe 与水蒸气反应的化学方程式:___________ 。
(3)乙同学认为加入KSCN 溶液没有出现血红色的原因可能是固体中没有Fe3O4,也有可能是因为___ (填物质名称)过量造成的。该物质过量时,溶液中还会发生反应,导致加入KSCN 溶液时没有出现血红色,该反应的离子方程式是______________ 。
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH 溶液后,观察到的实验现象为___ 。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
| 实验编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末放入试管中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
② | 向试管中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
(1)湿棉花的作用是
(2)写出高于570℃ 时,Fe 与水蒸气反应的化学方程式:
(3)乙同学认为加入KSCN 溶液没有出现血红色的原因可能是固体中没有Fe3O4,也有可能是因为
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH 溶液后,观察到的实验现象为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系。据此判断:
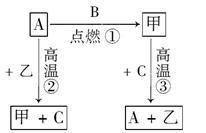
(1)元素A有可变化合价,则单质A是________ ,化合物甲是________ 。
(2)写出反应①②③的化学方程式

(1)元素A有可变化合价,则单质A是
(2)写出反应①②③的化学方程式
①
②
③
您最近半年使用:0次
【推荐3】铁是人类较早使用的金属之一,铁及其化合物应用广泛。请运用所学知识,回答下列问题。
Ⅰ.某化学学习小组想利用FeCl3腐蚀铜后所得的废液回收铜,并同时使FeCl3溶液再生,设计了如下实验:
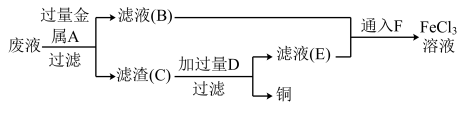
(1)通入F气体时发生反应的离子方程式为__________________
(2)若取少量滤液B于试管中,加入适量氢氧化钠溶液,振荡试管,再放置几分钟,可以观察到试管内的现象为________________ ,涉及的化学反应方程式为_________________________ 。
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,进行了如图实验。
(3)若所用铁粉中含有少量杂质铝,可以用_________ 除去铝(填序号),
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
(4)实验Ⅰ中反应的化学方程式为_________________________________
(5)甲同学观察到实验Ⅰ中持续产生肥皂泡,一段时间后,取少量实验Ⅰ中反应后的固体进行实验Ⅱ。如果实验Ⅱ中的溶液b呈现红色,则说明溶液a中一定含有____ 离子(写离子符号),但甲同学发现实验Ⅱ中的溶液b并没有呈现红色,请你分析溶液b未呈现红色的原因为:__ 。
Ⅰ.某化学学习小组想利用FeCl3腐蚀铜后所得的废液回收铜,并同时使FeCl3溶液再生,设计了如下实验:

(1)通入F气体时发生反应的离子方程式为
(2)若取少量滤液B于试管中,加入适量氢氧化钠溶液,振荡试管,再放置几分钟,可以观察到试管内的现象为
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,进行了如图实验。
| 实验Ⅰ | 实验Ⅱ |
 |  |
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
(4)实验Ⅰ中反应的化学方程式为
(5)甲同学观察到实验Ⅰ中持续产生肥皂泡,一段时间后,取少量实验Ⅰ中反应后的固体进行实验Ⅱ。如果实验Ⅱ中的溶液b呈现红色,则说明溶液a中一定含有
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室用下图装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。
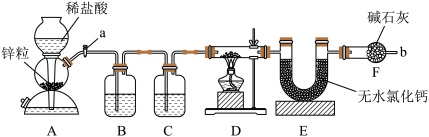
(1)为了安全,在点燃D处的酒精灯之前,在b处必须________________ 。
(2)装置B的作用是_______________ ,装置C中盛装的液体是________________ 。
(3)在硬质双通玻璃管中发生的化学反应方程式是________________________________ 、__________________________ 。
(4)若为FeO和Fe2O3物质的量之比1∶1的固体混合物,反应完全后,U形管的质量增加7.2 g,则混合物中Fe2O3的质量为______________ 。
(5)U形管E右边连接干燥管F的目的是________________ ,若无干燥管F,测得Fe2O3的质量将_____________ (填“偏大”“偏小”或“无影响”)。
(6)铁的化合物的固体或溶液中常常混有需要除去的杂质,试对下列物质(括号内为杂质),使用合适的试剂或分离方法除杂。
①Fe2O3[Fe(OH)3]___________________________________ ;
②FeCl3溶液(FeCl2)___________________________________ ;
③FeCl2溶液(FeCl3)___________________ 。

(1)为了安全,在点燃D处的酒精灯之前,在b处必须
(2)装置B的作用是
(3)在硬质双通玻璃管中发生的化学反应方程式是
(4)若为FeO和Fe2O3物质的量之比1∶1的固体混合物,反应完全后,U形管的质量增加7.2 g,则混合物中Fe2O3的质量为
(5)U形管E右边连接干燥管F的目的是
(6)铁的化合物的固体或溶液中常常混有需要除去的杂质,试对下列物质(括号内为杂质),使用合适的试剂或分离方法除杂。
①Fe2O3[Fe(OH)3]
②FeCl3溶液(FeCl2)
③FeCl2溶液(FeCl3)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用如图装置测定 和
和 固体混合物中
固体混合物中 的质量,装置D中硬质双通玻璃管中的固体物质是
的质量,装置D中硬质双通玻璃管中的固体物质是 和
和 的混合物。
的混合物。
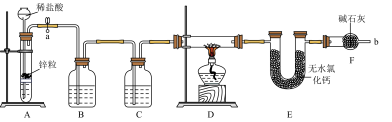
(1)为了安全,在点燃D处的酒精灯之前,必须_____ 。
(2)装置F的作用是_____ 。
(3)检验装置A气密性的方法是_____ 。
(4)若 和
和 固体混合物的质量为
固体混合物的质量为 ,反应完全后U形管的质量增加
,反应完全后U形管的质量增加 ,则混合物中
,则混合物中 的质量为
的质量为_____ g。
(5)若装置中无干燥管F,则测得的 质量将
质量将_____ (填“偏大”“偏小”或“无影响”,下同),若反应后得到的残留固体中还有少量 ,则测得的
,则测得的 质量将
质量将_____ 。
 和
和 固体混合物中
固体混合物中 的质量,装置D中硬质双通玻璃管中的固体物质是
的质量,装置D中硬质双通玻璃管中的固体物质是 和
和 的混合物。
的混合物。
(1)为了安全,在点燃D处的酒精灯之前,必须
(2)装置F的作用是
(3)检验装置A气密性的方法是
(4)若
 和
和 固体混合物的质量为
固体混合物的质量为 ,反应完全后U形管的质量增加
,反应完全后U形管的质量增加 ,则混合物中
,则混合物中 的质量为
的质量为(5)若装置中无干燥管F,则测得的
 质量将
质量将 ,则测得的
,则测得的 质量将
质量将
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,按要求填空
(1)①~⑧元素中金属性最强的元素是___________ (写元素符号),画出⑨的原子结构示意图___________ 。
(2)①~⑧元素中,最高价氧化物水化物酸性最强的物质是___________ (写化学式)。
(3)⑤⑥⑦⑧四种元素中,离子半径最小的是___________ (填离子符号)。
(4)⑧的一种含氧酸具有强氧化性,常用于杀菌、消毒、漂白,请用写出该化合物的电子式___________ 。
(5)将54.4 g铁粉和氧化铁的混合物中加入200 mL的稀硫酸,恰好完全反应,放出氢气4.48 L(标准状况)反应后的溶液中滴加KSCN不显红色。求:
I. 混合物中氧化铁是___________ g。
II. 原稀硫酸的物质的量浓度___________ mol·L-1。
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)①~⑧元素中,最高价氧化物水化物酸性最强的物质是
(3)⑤⑥⑦⑧四种元素中,离子半径最小的是
(4)⑧的一种含氧酸具有强氧化性,常用于杀菌、消毒、漂白,请用写出该化合物的电子式
(5)将54.4 g铁粉和氧化铁的混合物中加入200 mL的稀硫酸,恰好完全反应,放出氢气4.48 L(标准状况)反应后的溶液中滴加KSCN不显红色。求:
I. 混合物中氧化铁是
II. 原稀硫酸的物质的量浓度
您最近半年使用:0次



