现有① ②
② ③
③ ④
④ ⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
(1)甲中有________ ;乙中有________ 。(填序号)
(2)由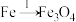 ,
,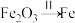 可知,欲实现I反应过程应从
可知,欲实现I反应过程应从________ (填“甲”或“乙”,下同)中找物质,欲实现Ⅱ反应过程应从________ 中找物质。
(3)请将下列6种物质: 、
、 、
、 、
、 、
、 、
、 (提示:能按
(提示:能按 ________+________→________+________+
________+________→________+________+ 形式反生化学反应)写出该反应对应的离子方式
形式反生化学反应)写出该反应对应的离子方式_______ ;并在离子方程式上标出电子转移的方向和数目______ 。
(4)一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为: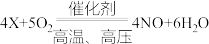 ,请推出X的化学式为
,请推出X的化学式为_____ 。
 ②
② ③
③ ④
④ ⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:(1)甲中有
(2)由
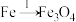 ,
,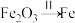 可知,欲实现I反应过程应从
可知,欲实现I反应过程应从(3)请将下列6种物质:
 、
、 、
、 、
、 、
、 、
、 (提示:能按
(提示:能按 ________+________→________+________+
________+________→________+________+ 形式反生化学反应)写出该反应对应的离子方式
形式反生化学反应)写出该反应对应的离子方式(4)一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
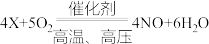 ,请推出X的化学式为
,请推出X的化学式为
更新时间:2020-11-29 10:47:22
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】根据反应 MnO2+4HCl(浓)== MnCl2+Cl2↑+2H2O,回答下列问题:
①还原剂是________ ,还原产物是________ .
②氧化剂是________ ,氧化产物是________ .
③在标准状况下有44、8L Cl2生成时,被氧化的物质是________ mol
①还原剂是
②氧化剂是
③在标准状况下有44、8L Cl2生成时,被氧化的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,___________ 元素被氧化,___________ 元素被还原;氧化剂是___________ ,氧化产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目_________________________________ 。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:(1)上述反应中,
(2)用“双线桥法”表示反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角。
(1)在氧化还原反应中,氧化剂______ 电子,发生______ 反应。
(2)理论上,处于最低价态的元素通常具有______ 性,在氧化还原反应中常作_____ 剂。
(3)下列物质在氧化还原反应中,常作还原剂的有______ (均填序号,下同);常作氧化剂的有______ 。
①KMnO4 ②铝 ③氧气 ④FeCl3 ⑤一氧化碳
(4)已知钠与冷水剧烈反应,反应方程式是2Na+2H2O=2NaOH+H2↑,铁与水蒸气发生反应:3Fe+4H2O(g) Fe3O4+4H2,钠与水反应中,若消耗0.2 mol钠,则转移的电子为
Fe3O4+4H2,钠与水反应中,若消耗0.2 mol钠,则转移的电子为______ mol。事实证明,钠的还原性比铁的还原性______ (填“强”或“弱”)。
(1)在氧化还原反应中,氧化剂
(2)理论上,处于最低价态的元素通常具有
(3)下列物质在氧化还原反应中,常作还原剂的有
①KMnO4 ②铝 ③氧气 ④FeCl3 ⑤一氧化碳
(4)已知钠与冷水剧烈反应,反应方程式是2Na+2H2O=2NaOH+H2↑,铁与水蒸气发生反应:3Fe+4H2O(g)
 Fe3O4+4H2,钠与水反应中,若消耗0.2 mol钠,则转移的电子为
Fe3O4+4H2,钠与水反应中,若消耗0.2 mol钠,则转移的电子为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】请填写以下空白。
(1)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是_______ 。
A.Fe B.Fe2+ C.Fe3+
(2)曾多次出现因误食NaNO2而中毒事件,其原因是NaNO2把人体内的Fe2+转化为 Fe3+而失去与O2结合的能力,这说明NaNO2具有_______ 性。(“氧化” 或“还原”)。下列不能实现上述转化的物质是_______ 。
A.Cl2 B.O2 C.FeCl3
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 +3C =K2S +N2↑+ 3CO2↑。在该反应中还原剂是_______ ,氧化剂是_______ 。
(1)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)曾多次出现因误食NaNO2而中毒事件,其原因是NaNO2把人体内的Fe2+转化为 Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 +3C =K2S +N2↑+ 3CO2↑。在该反应中还原剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】我国是最早记载丹砂的药用价值和炼制方法的,为了使人民重视丹砂,我国曾发行面值为10分的丹砂邮票。汞单质及其化合物在工业生产和科学研究上有着广泛用途。丹砂炼汞的反应原理包括以下两个反应:
反应I:HgS+O2 Hg+SO2
Hg+SO2
反应II:4HgS+4CaO 4Hg+3CaS+CaSO4
4Hg+3CaS+CaSO4
(1)反应I中,还原产物是_______ ,每生成1个SO2分子,转移电子数为_______ 。
(2)反应II中,HgS是_______ (填“氧化剂”、“还原剂”或“氧化剂和还原剂”),用双线桥法标出反应II中电子转移的方向和数目_______ 。
4HgS+4CaO 4Hg+3CaS+CaSO4
4Hg+3CaS+CaSO4
反应I:HgS+O2
 Hg+SO2
Hg+SO2反应II:4HgS+4CaO
 4Hg+3CaS+CaSO4
4Hg+3CaS+CaSO4(1)反应I中,还原产物是
(2)反应II中,HgS是
4HgS+4CaO
 4Hg+3CaS+CaSO4
4Hg+3CaS+CaSO4
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】双氧水、84消毒液、 都可做消毒剂。
都可做消毒剂。
Ⅰ.某学习小组为探究 的电离情况,用
的电离情况,用 计测定25℃时不同浓度次氯酸的
计测定25℃时不同浓度次氯酸的 ,结果如下:
,结果如下:
(1)根据表中数据可知 是
是_______ 电解质(填“强”或“弱”),得出此结论的依据是_______ 。
(2)从表中数据,还可以得出另一结论:随着次氯酸溶液浓度的减小,次氯酸的电离程度_______ (填“增大”、“减小”或“不变”)。
Ⅱ.2016年巴西奥运会期间,工作人员将84消毒液与双氧水两种消毒剂混用,导致泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 。
。
(3)①该反应说明氧化性:
_______  (填“>”或“<”)。
(填“>”或“<”)。
②当有 生成时,转移电子
生成时,转移电子_______  。
。
(4)已知: 不稳定,为防止存储过程中失效,通常要在84消毒液中残余少量
不稳定,为防止存储过程中失效,通常要在84消毒液中残余少量 ,请运用平衡移动原理解释
,请运用平衡移动原理解释 的作用:
的作用:_______ 。
(5)双氧水是二元弱酸,298K时,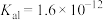 ,
,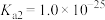 ,双氧水电离方程式为
,双氧水电离方程式为_______ ;298K时 双氧水溶液的
双氧水溶液的
_______ 。(已知: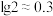 )
)
 都可做消毒剂。
都可做消毒剂。Ⅰ.某学习小组为探究
 的电离情况,用
的电离情况,用 计测定25℃时不同浓度次氯酸的
计测定25℃时不同浓度次氯酸的 ,结果如下:
,结果如下:浓度/( ) ) | 0.2000 | 0.1000 | 0.0100 |
 | 2.83 | 2.88 | 3.38 |
 是
是(2)从表中数据,还可以得出另一结论:随着次氯酸溶液浓度的减小,次氯酸的电离程度
Ⅱ.2016年巴西奥运会期间,工作人员将84消毒液与双氧水两种消毒剂混用,导致泳池藻类快速生长,池水变绿。一种可能的原因是
 与
与 反应产生
反应产生 。
。(3)①该反应说明氧化性:

 (填“>”或“<”)。
(填“>”或“<”)。②当有
 生成时,转移电子
生成时,转移电子 。
。(4)已知:
 不稳定,为防止存储过程中失效,通常要在84消毒液中残余少量
不稳定,为防止存储过程中失效,通常要在84消毒液中残余少量 ,请运用平衡移动原理解释
,请运用平衡移动原理解释 的作用:
的作用:(5)双氧水是二元弱酸,298K时,
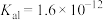 ,
,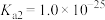 ,双氧水电离方程式为
,双氧水电离方程式为 双氧水溶液的
双氧水溶液的
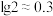 )
)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】H2O2在实验、医疗、化工等方面有广泛的应用。
(1)H2O2中O的化合价为___________ ,具有___________ (填“氧化性”“还原性”或“氧化性和还原性”)。
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是H2O2+KMnO4+H2SO4=K2SO4+MnSO4+O2↑+H2O。已知:稀MnSO4溶液几乎无色。
①配平该化学反应方程式___________ 。
②上述反应中的还原剂为___________ (填化学式),被还原的元素是___________ (填元素符号)。
③高锰酸钾溶液呈___________ 色,向酸性KMnO4溶液中滴入双氧水,观察到的现象是___________ ,反应后溶液的pH___________ (填“增大”“减小”或“不变”)。
④2个KMnO4参加上述反应,转移电子___________ 个。
(1)H2O2中O的化合价为
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是H2O2+KMnO4+H2SO4=K2SO4+MnSO4+O2↑+H2O。已知:稀MnSO4溶液几乎无色。
①配平该化学反应方程式
②上述反应中的还原剂为
③高锰酸钾溶液呈
④2个KMnO4参加上述反应,转移电子
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如图为氯及其化合物的“价—类”二维图。

(1)二维图中 A 的类别为___________ ;B的名称为___________ 。
(2)已知氯的某氧化物(ClmOn)中,氯、氧元素的质量比为 71∶64,此氧化物的化学式为___________ ,该物质可用于自来水的消毒,是因为该物质具有_____ 性。
(3)已知 HClO4是一元强酸,写出 HClO4的电离方程式_________ 。
(4)某同学研究 HCl 性质,进行如下预测:
①从物质类别上看,HCl属于酸,能与大理石反应,反应的离子方程式为_____ 。
②从化合价角度看,Cl-具有_____ 性,能与_____ 发生反应(填标号)。
A.NaClO B.Fe C.KMnO4 D.NaOH

(1)二维图中 A 的类别为
(2)已知氯的某氧化物(ClmOn)中,氯、氧元素的质量比为 71∶64,此氧化物的化学式为
(3)已知 HClO4是一元强酸,写出 HClO4的电离方程式
(4)某同学研究 HCl 性质,进行如下预测:
①从物质类别上看,HCl属于酸,能与大理石反应,反应的离子方程式为
②从化合价角度看,Cl-具有
A.NaClO B.Fe C.KMnO4 D.NaOH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为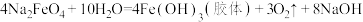 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。回答下列问题:
(1)高铁酸钠( )属于
)属于_________ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为_________ 价。
(2)Fe(OH)3胶体能使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是__________ nm。
(3)该反应中NaOH____________ (填“是氧化产物”、“是还原产物”或“既不是氧化产物又不是还原产物”,下同),
_________ 。
II.一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁,服用维生素C,可使食物中的Fe3+转化成Fe2+,有利于人体吸收。
(4)在人体中进行Fe2+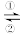 Fe3+的转化时,①反应中的Fe2+发生
Fe3+的转化时,①反应中的Fe2+发生______ (填“氧化”或“还原”,下同)反应,②反应中的Fe3+被______ 。
(5)“服用维生素C,可使食物中的Fe3+转化成Fe2+”这句话说明,维生素C具有______ 性。
 )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为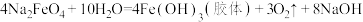 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。回答下列问题:(1)高铁酸钠(
 )属于
)属于(2)Fe(OH)3胶体能使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是
(3)该反应中NaOH

II.一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁,服用维生素C,可使食物中的Fe3+转化成Fe2+,有利于人体吸收。
(4)在人体中进行Fe2+
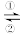 Fe3+的转化时,①反应中的Fe2+发生
Fe3+的转化时,①反应中的Fe2+发生(5)“服用维生素C,可使食物中的Fe3+转化成Fe2+”这句话说明,维生素C具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnC12、SnC14、FeSO4、Fe2(SO4)3,反应前在溶液中滴加KSCN溶液显红色,反应后红色消失。
(1)该反应的氧化剂是____________ 。
(2)在该反应中,发生氧化反应的过程是___________ →___________ 。
(3)写出并配平该反应的化学方程式,并标出电子转移的方向和数目:_____________ 。
(4)SnC14与SnC12可用Hg2+来鉴别,HgC12与SnC12反应的产物是SnC14和Hg2C12(白色沉淀),该反应中还原剂与氧化剂的物质的量之比为___________ 。
(1)该反应的氧化剂是
(2)在该反应中,发生氧化反应的过程是
(3)写出并配平该反应的化学方程式,并标出电子转移的方向和数目:
(4)SnC14与SnC12可用Hg2+来鉴别,HgC12与SnC12反应的产物是SnC14和Hg2C12(白色沉淀),该反应中还原剂与氧化剂的物质的量之比为
您最近一年使用:0次

 H2S +
H2S + 

