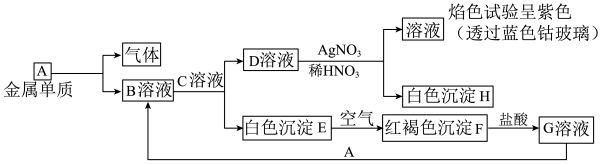
某研究性学习小组请你参与“研究铁与水蒸气反应所得固体物质的成分、性质及再利用”实验探究,并回答下列问题:
【查阅资料】含有Fe3+的盐溶液遇到KSCN溶液时变成红色,含有Fe2+的盐溶液遇到KSCN溶液时不变色。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。
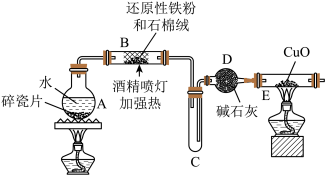
(1)硬质玻璃管B中发生反应的化学方程式为:________
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分(已知酸性KMnO4溶液能与盐酸发生反应生成氯气)。
(2)待硬质玻璃管B冷却后,取少许其中的固体继续进行如下实验:

①试剂A是_____ ,现象2为___ 。
②若现象1中溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:_______ 。
【查阅资料】含有Fe3+的盐溶液遇到KSCN溶液时变成红色,含有Fe2+的盐溶液遇到KSCN溶液时不变色。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为:
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分(已知酸性KMnO4溶液能与盐酸发生反应生成氯气)。
(2)待硬质玻璃管B冷却后,取少许其中的固体继续进行如下实验:

①试剂A是
②若现象1中溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:
更新时间:2020-11-29 21:23:21
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】按如图所示装置进行铁和水蒸气反应的实验。
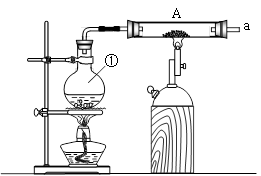
(1)请指出仪器①的名称:________________ ;
(2)铁粉与水蒸气反应的化学方程式是:__________________ ;
(3)为检验生成的气体产物,请将下列三套装置进行合理组合,其正确的连接顺序为(用接口字母表示)a—____________ ,能证明该气体产物的实验现象为________________ ;
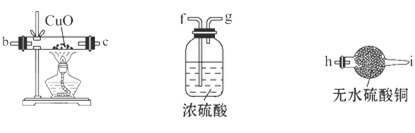
(4)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应,过滤。简述检验所得滤液中是否含Fe3+的操作方法:________________ ;
(5)某同学在实验室欲制取白色的Fe(OH)2沉淀。
①向上述滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。沉淀由白色变为红褐色的化学方程式是:_________________ ;
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,该同学设计如下图所示的装置。通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中不正确的是________ (填序号)。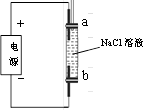
A.a端必须用铁作电极
B.a端发生的反应是2Cl--2e-=Cl2↑
C.b端发生的反应是2H++2e-=H2↑

(1)请指出仪器①的名称:
(2)铁粉与水蒸气反应的化学方程式是:
(3)为检验生成的气体产物,请将下列三套装置进行合理组合,其正确的连接顺序为(用接口字母表示)a—

(4)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应,过滤。简述检验所得滤液中是否含Fe3+的操作方法:
(5)某同学在实验室欲制取白色的Fe(OH)2沉淀。
①向上述滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。沉淀由白色变为红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,该同学设计如下图所示的装置。通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中不正确的是

A.a端必须用铁作电极
B.a端发生的反应是2Cl--2e-=Cl2↑
C.b端发生的反应是2H++2e-=H2↑
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:

(1)A装置的作用是___ 。
(2)装置B中发生反应的化学方程式是___ 。
(3)D的作用是___ 。E中的实验现象是___ 。
(4)同学们经过分析讨论,认为此实验装置设计还不完整,原因是___ 。

(1)A装置的作用是
(2)装置B中发生反应的化学方程式是
(3)D的作用是
(4)同学们经过分析讨论,认为此实验装置设计还不完整,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】烧碱在保存过程会部分变质(杂质主要为Na2CO3)。
Ⅰ、定性检验
取少量烧碱样品于试管,加蒸馏水使其完全溶解。向所得溶液滴加几滴BaCl2溶液,若出现白色沉淀,则说明已变质,反之则未变质
Ⅱ、定量测定
准确称取5.0g样品配制成250mL溶液,各取配制好的烧碱溶液20.00mL于三个锥形瓶中,分别加入过量的BaCl2溶液(使Na2CO3完全转变成BaCO3沉淀),并向锥形瓶中各加入1∼2滴指示剂(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1∼4.4②甲基红4.4∼6.2③酚酞8.2∼10),用浓度为0.2000mol·L−1的盐酸标准液进行滴定。相关数据记录如下:
试回答:
(1)如何确定BaCl2溶液是否滴加过量?__________________
(2)向混有BaCO3沉淀的NaOH溶液中滴入盐酸,应选用_______________ 做指示剂,理由是____________ ;判断到达滴定终点的实验现象是___________________ .
(3)滴定时的正确操作是____________________________________ .依据表中数据,计算出烧碱样品中含NaOH(M=40g/mol)的质量分数为________________ %.(小数点后保留两位数字)
(4)下列操作会导致烧碱样品中NaOH含量测定值偏高的是_________________
A. 锥形瓶用蒸馏水洗后未用待测液润洗 B. 酸式滴定管用蒸馏水洗后未用标准液润洗
C. 在滴定前有气泡,滴定后气泡消失 D. 滴定前平视读数,滴定结束俯视读数。
Ⅰ、定性检验
取少量烧碱样品于试管,加蒸馏水使其完全溶解。向所得溶液滴加几滴BaCl2溶液,若出现白色沉淀,则说明已变质,反之则未变质
Ⅱ、定量测定
准确称取5.0g样品配制成250mL溶液,各取配制好的烧碱溶液20.00mL于三个锥形瓶中,分别加入过量的BaCl2溶液(使Na2CO3完全转变成BaCO3沉淀),并向锥形瓶中各加入1∼2滴指示剂(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1∼4.4②甲基红4.4∼6.2③酚酞8.2∼10),用浓度为0.2000mol·L−1的盐酸标准液进行滴定。相关数据记录如下:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.50 | 31.50 |
| 2 | 20.00 | 1.00 | 32.04 |
| 3 | 20.00 | 1.10 | 32.18 |
试回答:
(1)如何确定BaCl2溶液是否滴加过量?
(2)向混有BaCO3沉淀的NaOH溶液中滴入盐酸,应选用
(3)滴定时的正确操作是
(4)下列操作会导致烧碱样品中NaOH含量测定值偏高的是
A. 锥形瓶用蒸馏水洗后未用待测液润洗 B. 酸式滴定管用蒸馏水洗后未用标准液润洗
C. 在滴定前有气泡,滴定后气泡消失 D. 滴定前平视读数,滴定结束俯视读数。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】实验室有五瓶失去标签的未知溶液,只知道它们由Na2CO3、 、CuCl2、K2SO4、HCl五种溶液组成,为了将它们一一鉴别出来,某兴趣小组在不用其他试剂的条件下,做了以下实验。
、CuCl2、K2SO4、HCl五种溶液组成,为了将它们一一鉴别出来,某兴趣小组在不用其他试剂的条件下,做了以下实验。
①将五瓶溶液随机标记为A、B、C、D、E;
②经观察,发现只有D溶液呈蓝色,另外四瓶溶液无色;
③将A、B、C、E四种溶液分别彼此相互滴加,发现B可与E产生沉淀,与C产生气体。
根据实验现象回答下列问题。
(1)由此可推断A、D的化学式分别为:A___________ D___________
(2)写出向B中滴加少盘C溶液的离子方程式:___________
(3)将含相同物质的量C、D、E的溶液混合,混合后溶液中存在的离子有:___________ ;且各离子的物质的量之比为:___________
(4)请你设计实验,进一步检验A溶液中的阴离子。___________ (实验仪器和药品任选,必须包含实验步骤、现象、结论)
 、CuCl2、K2SO4、HCl五种溶液组成,为了将它们一一鉴别出来,某兴趣小组在不用其他试剂的条件下,做了以下实验。
、CuCl2、K2SO4、HCl五种溶液组成,为了将它们一一鉴别出来,某兴趣小组在不用其他试剂的条件下,做了以下实验。①将五瓶溶液随机标记为A、B、C、D、E;
②经观察,发现只有D溶液呈蓝色,另外四瓶溶液无色;
③将A、B、C、E四种溶液分别彼此相互滴加,发现B可与E产生沉淀,与C产生气体。
根据实验现象回答下列问题。
(1)由此可推断A、D的化学式分别为:A
(2)写出向B中滴加少盘C溶液的离子方程式:
(3)将含相同物质的量C、D、E的溶液混合,混合后溶液中存在的离子有:
(4)请你设计实验,进一步检验A溶液中的阴离子。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】“84消毒液”为含氯消毒剂的代表被广泛使用,化学小组用如下方法测定某“84消毒液”中有效氯的含量。
I.准确量取2.00mL消毒液稀释成100.0mL溶液;
II.取1.00mL上述稀释后溶液,依次加入3mol·L-1硫酸溶液15mL、15.00mL一定浓度的Fe2+溶液,加盖振摇混匀后,室温静置反应10min;
III.用0.0010mol·L-1的标准K2Cr2O7溶液滴定II中反应后溶液,记录消耗的体积为VmL;
IV.另取与II中相同的15.00mL一定浓度的Fe2+溶液,依次加入1.00mL蒸馏水、3mol·L-1硫酸溶液15mL,加盖振摇混匀;
V.用0.0010mol·L-1的标准K2Cr2O7溶液滴定IV中溶液,记录消耗的体积为V0mL。
(1)工业上制取“84消毒液”反应的化学方程式为_______ 。
(2)Ⅰ中稀释溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和______ 。
(3)用KSCN溶液检测到II反应后溶液中含有Fe3+的现象是______ ,Ⅱ中反应的离子方程式为______ 。
(4)Ⅲ中发生反应的离子方程式是_____ (Cr2O 转化为Cr3+,此条件下不氧化Cl-)。
转化为Cr3+,此条件下不氧化Cl-)。
(5)该“84消毒液”中有效氯的含量为_____ g/100mL。(有效氯以NaClO质量计,NaClO摩尔质量:74.5g·mol-1)
(6)由于Fe2+具有_____ 性,II、IV中实验须在密闭容器中进行。
I.准确量取2.00mL消毒液稀释成100.0mL溶液;
II.取1.00mL上述稀释后溶液,依次加入3mol·L-1硫酸溶液15mL、15.00mL一定浓度的Fe2+溶液,加盖振摇混匀后,室温静置反应10min;
III.用0.0010mol·L-1的标准K2Cr2O7溶液滴定II中反应后溶液,记录消耗的体积为VmL;
IV.另取与II中相同的15.00mL一定浓度的Fe2+溶液,依次加入1.00mL蒸馏水、3mol·L-1硫酸溶液15mL,加盖振摇混匀;
V.用0.0010mol·L-1的标准K2Cr2O7溶液滴定IV中溶液,记录消耗的体积为V0mL。
(1)工业上制取“84消毒液”反应的化学方程式为
(2)Ⅰ中稀释溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(3)用KSCN溶液检测到II反应后溶液中含有Fe3+的现象是
(4)Ⅲ中发生反应的离子方程式是
 转化为Cr3+,此条件下不氧化Cl-)。
转化为Cr3+,此条件下不氧化Cl-)。(5)该“84消毒液”中有效氯的含量为
(6)由于Fe2+具有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
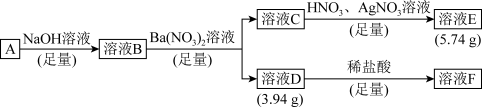
【推荐2】Ⅰ.由三种短周期元素组成的化合物A,按如下流程进行实验。已知相同条件下气态A物质的密度为氢气密度的49.5倍。
请回答:
(1)组成A的三种元素为__________ ,A的化学式为__________ 。
(2)A与足量NaOH溶液反应的化学方程式为__________ 。
(3)A与足量氨气在一定条件下可以反应生成2种常见的氮肥,该反应的化学方程式为________ 。
Ⅱ.二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于 10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(4)在处理废水时,ClO2可将废水中的CN-氧化成CO2和N2,写出该反应的离子方程式为____________ 。
(5)某小组按照文献中制备ClO2的方法,设计了如图所示的实验装置,用于制备ClO2并验证其某些性质。
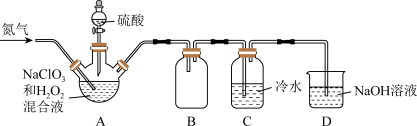
①通入氮气的主要作用有 2 个,一是可以起到搅拌作用,二是____________________ ;
②关于该实验,以下说法正确的是______________ 。
A.装置 A 用适量 H2O2制取 ClO2气体,其反应的化学方程式为2NaClO3+3H2O2+H2SO4=2ClO2↑+Na2SO4+2O2↑+4H2O
B.装置 B 用来收集二氧化氯气体
C.当看到装置 C 中导管液面上升时应加大氮气的通入量
D.二氧化氯能杀菌消毒,但不会与有机物发生取代反应

请回答:
(1)组成A的三种元素为
(2)A与足量NaOH溶液反应的化学方程式为
(3)A与足量氨气在一定条件下可以反应生成2种常见的氮肥,该反应的化学方程式为
Ⅱ.二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于 10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(4)在处理废水时,ClO2可将废水中的CN-氧化成CO2和N2,写出该反应的离子方程式为
(5)某小组按照文献中制备ClO2的方法,设计了如图所示的实验装置,用于制备ClO2并验证其某些性质。

①通入氮气的主要作用有 2 个,一是可以起到搅拌作用,二是
②关于该实验,以下说法正确的是
A.装置 A 用适量 H2O2制取 ClO2气体,其反应的化学方程式为2NaClO3+3H2O2+H2SO4=2ClO2↑+Na2SO4+2O2↑+4H2O
B.装置 B 用来收集二氧化氯气体
C.当看到装置 C 中导管液面上升时应加大氮气的通入量
D.二氧化氯能杀菌消毒,但不会与有机物发生取代反应
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学小组用下列装置制备氨基甲酸铵(NH2COONH4),其反应原理为:2NH3(g) + CO2(g) = NH2COONH4(s) △H<0。已知:氨基甲酸铵难溶于四氯化碳;易水解生成碳酸氢铵,受热分解可生成尿素。

试回答下列问题:
(1)C装置中橡皮管的作用是___________ ;试剂x可以是___________ 。
(2)用上述装置制取氨基甲酸铵,以上所有装置的正确连接顺序是:___________→___________→E←___________←___________←___________。 (填大写字母)___________
(3)反应时,为了提高氨基甲酸铵的产量,三颈烧瓶应放置在___________ (填“热水浴’或“冷水浴”)中:装置E中浸有稀H2SO4的棉花作用是___________ 。
(4)反应在CCl4的液体中进行的原因是___________ 。
(5)实验制备过程中为了提高氨基甲酸铵纯度,请提出合理措施___________ 。

试回答下列问题:
(1)C装置中橡皮管的作用是
(2)用上述装置制取氨基甲酸铵,以上所有装置的正确连接顺序是:___________→___________→E←___________←___________←___________。 (填大写字母)
(3)反应时,为了提高氨基甲酸铵的产量,三颈烧瓶应放置在
(4)反应在CCl4的液体中进行的原因是
(5)实验制备过程中为了提高氨基甲酸铵纯度,请提出合理措施
您最近一年使用:0次