已知有以下物质相互转化:
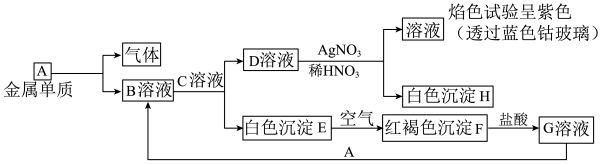
试回答:
(1)写出下列物质化学式:B_______ D_______ F_______ 。
(2)金属单质A与水蒸气反应的化学方程式为_______ ;此反应中消耗3mol单质A,电子转移数目为_______ 个。
(3)写出由E转变成F的化学方程式_______ 。
(4)用KSCN鉴别G溶液的现象_______ ;向G溶液加入A的有关离子反应方程式_______ 。

试回答:
(1)写出下列物质化学式:B
(2)金属单质A与水蒸气反应的化学方程式为
(3)写出由E转变成F的化学方程式
(4)用KSCN鉴别G溶液的现象
更新时间:2022-02-18 16:15:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】M是一种单质,A、B、C、D、E、F、G都是含有同一种元素的物质,这七种物质相互转变的关系如图所示:

(1)写出下列物质的颜色:M_______ F_______ ,
(2)写出下列变化的化学方程式
A→B:_______ 该反应中每消耗0.3 mol的A,可转移电子_______ mol。
E→G_______ ;
D→C_______ 。
(3)上述反应中,属于氧化还原反应的有_______ 个

(1)写出下列物质的颜色:M
(2)写出下列变化的化学方程式
A→B:
E→G
D→C
(3)上述反应中,属于氧化还原反应的有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】盐A是由三种元素组成的化合物,某研究小组按图流程探究其组成:

请回答下列问题:
(1)写出红棕色固体C的化学式___________ 。
(2)写出A受热分解的化学方程式___________ 。
(3)写出气体B与溶液E的离子方程式___________ 。

请回答下列问题:
(1)写出红棕色固体C的化学式
(2)写出A受热分解的化学方程式
(3)写出气体B与溶液E的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】 、
、 、
、 、
、 四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8,
四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8, 元素原子的
元素原子的 层电子数与
层电子数与 、
、 层电子数之和相等,
层电子数之和相等, 元素原子的
元素原子的 、
、 层电子数之和等于电子总数的一半。试回答下列问题。
层电子数之和等于电子总数的一半。试回答下列问题。
(1)四种元素的符号依次是
______ ,
______ ,
______ ,
______ ;它们的原子半径由大到小的顺序是______ (用元素符号表示)。
(2)试写出四种元素的离子结构示意图:
______ ,
______ ,
______ ,
______ 。它们的离子半径由大到小的顺序是______ (用离子符号表示)。
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:______ 。
(4)分别写出 、
、 两元素的气态氢化物的化学式:
两元素的气态氢化物的化学式:______ 。
 、
、 、
、 、
、 四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8,
四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8, 元素原子的
元素原子的 层电子数与
层电子数与 、
、 层电子数之和相等,
层电子数之和相等, 元素原子的
元素原子的 、
、 层电子数之和等于电子总数的一半。试回答下列问题。
层电子数之和等于电子总数的一半。试回答下列问题。(1)四种元素的符号依次是




(2)试写出四种元素的离子结构示意图:




(3)分别写出四种元素的最高价氧化物对应水化物的化学式:
(4)分别写出
 、
、 两元素的气态氢化物的化学式:
两元素的气态氢化物的化学式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某校化学小组学生利用如图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体。(图中夹持及尾气处理装置均已略去)
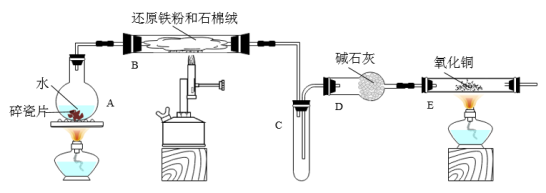
已知:3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)。请回答:
Fe3O4(s)+4H2(g)。请回答:
(1)装置A的作用是_______ 。
(2)仪器D的名称是_______ ,装置E中的现象是_______ 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出Fe3O4与稀盐酸反应的化学方程式:_______ 。
(4)该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如图所示:
滤液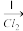 FeCl3溶液
FeCl3溶液 FeCl3·6H2O晶体
FeCl3·6H2O晶体
①步骤I中通入Cl2的作用是_______ ,写出反应的离子方程式_______ 。
②简述检验滤液中Fe3+的操作方法_______ 。
③步骤Ⅱ从FeCl3稀溶液中得到FeCl3•6H2O晶体的主要操作包括:_______ 。

已知:3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g)。请回答:
Fe3O4(s)+4H2(g)。请回答:(1)装置A的作用是
(2)仪器D的名称是
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出Fe3O4与稀盐酸反应的化学方程式:
(4)该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如图所示:
滤液
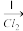 FeCl3溶液
FeCl3溶液 FeCl3·6H2O晶体
FeCl3·6H2O晶体①步骤I中通入Cl2的作用是
②简述检验滤液中Fe3+的操作方法
③步骤Ⅱ从FeCl3稀溶液中得到FeCl3•6H2O晶体的主要操作包括:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】铁不能与冷、热水反应,但是能与水蒸气反应。实验装置如图所示。在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。 请回答:
(1)写出该反应的化学方程式___________ 。
(2)实验前必须对整套装置进行的操作是______ ,实验开始时应先点燃______ (填“酒精灯”或“酒精喷灯”),实验结束时应先熄灭____ (填“酒精灯”或“酒精喷灯”)。
(3)圆底烧瓶中盛有水,该装置受热后的主要作用是_____ ;烧瓶里应事先放置______ ,其作用是_____ ;干燥管中盛装的物质是_____ 。
(4)待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B,取少量溶液B滴加_____ 溶液,若_____ (填实验现象),则说明溶液B中含有Fe3+。

(1)写出该反应的化学方程式
(2)实验前必须对整套装置进行的操作是
(3)圆底烧瓶中盛有水,该装置受热后的主要作用是
(4)待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B,取少量溶液B滴加

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质均为常见物质或它们的溶液,其中A为淡黄色固体,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱.根据它们之间的转化关系(如图),用化学用语回答问题。(部分产物已省略)
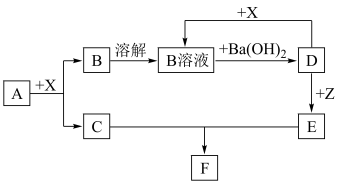
(1)写出下列物质的化学式:A____ D ____ 。
(2)物质E转化为物质F的现象为____ ,化学方程式为 ____ 。
(3)写出向B溶液中通入X气体的离子方程式_________________________ 。
(4)电子工业上,常使用向Z溶液中通入一定量的Cl2后所得溶液来刻蚀印刷电路板铜箔,写出刻蚀印刷电路板铜箔的离子方程式_________________________________ 。
(5)向含10gD的溶液中通入一定里的X,完全反应后,在低温条件下蒸发结晶,最终得到14.8g固体。所得固体中含有的物质及其物质的量之比为____ 。 (表达示例:n(A)︰n(B)=a︰b);简述蒸发结晶在低温条件下进行的理由: ____ (用必要文字回答)。

(1)写出下列物质的化学式:A
(2)物质E转化为物质F的现象为
(3)写出向B溶液中通入X气体的离子方程式
(4)电子工业上,常使用向Z溶液中通入一定量的Cl2后所得溶液来刻蚀印刷电路板铜箔,写出刻蚀印刷电路板铜箔的离子方程式
(5)向含10gD的溶液中通入一定里的X,完全反应后,在低温条件下蒸发结晶,最终得到14.8g固体。所得固体中含有的物质及其物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】研究小组为了探究无机盐X(仅含三种元素)的组成和性质,设计并完成如图实验。

已知:气体甲、固体甲均为纯净物。
请回答:
(1)X含有的元素是___ (填元素符号);白色沉淀2的化学式是___ 。
(2)隔绝空气加热X的化学方程式为___ 。
(3)一定条件下,气体甲与固体甲能发生氧化还原反应,写出一个可能的化学方程式___ 。

已知:气体甲、固体甲均为纯净物。
请回答:
(1)X含有的元素是
(2)隔绝空气加热X的化学方程式为
(3)一定条件下,气体甲与固体甲能发生氧化还原反应,写出一个可能的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C为三种单质(其中A为固体,B、C为气体),D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如下图:

填写下列空白:
(1)物质A是________ ,B是________ ,C是________ .
(2)F中加入NaOH溶液,并在空气中放置的化学方程式是__________________________ ,______________________________________________ 。

填写下列空白:
(1)物质A是
(2)F中加入NaOH溶液,并在空气中放置的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:

(1)将黄铜矿粉碎的目的是___________ 。
(2)高温焙烧时发生的反应方程式为 ,1molO2参加反应时,反应中转移电子
,1molO2参加反应时,反应中转移电子___________ mol。
(3)操作a使用的玻璃仪器为___________ 。
(4)向滤液A中通入Cl2的目的是___________ 。
(5)向溶液B中通入NH3时反应的离子方程式为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
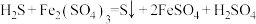 ,
,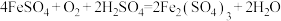
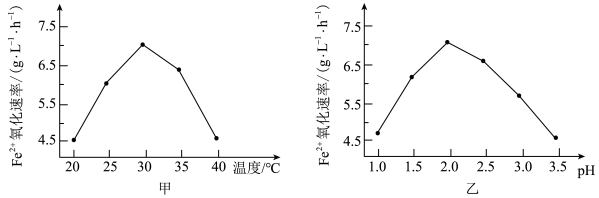
由图甲和图乙判断使用硫杆菌的最佳条件为___________

(1)将黄铜矿粉碎的目的是
(2)高温焙烧时发生的反应方程式为
 ,1molO2参加反应时,反应中转移电子
,1molO2参加反应时,反应中转移电子(3)操作a使用的玻璃仪器为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3时反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
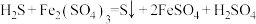 ,
,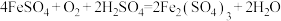
由图甲和图乙判断使用硫杆菌的最佳条件为___________

| A.温度为20℃,pH=2.0 |
| B.温度为30℃,pH=2.0 |
| C.温度为30℃,pH=1.0 |
| D.温度为40℃,pH=2.0 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】白色固体碘化亚铜( )可用作树脂改性剂,不溶于水,能被
)可用作树脂改性剂,不溶于水,能被 氧化,见光易分解。实验室制备
氧化,见光易分解。实验室制备 的方法是向
的方法是向 和
和 混合溶液中通入足量
混合溶液中通入足量 ,实验装置如图所示(部分装置已省略)。请回答下列问题:
,实验装置如图所示(部分装置已省略)。请回答下列问题:
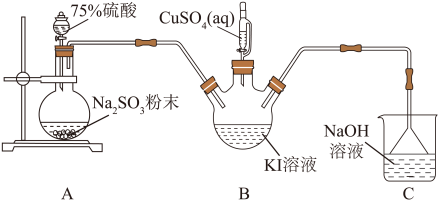
(1)装置A中发生反应的化学方程式为_______ 。
(2)装置B中发生反应的离子方程式是_______ 。
(3)盛放 溶液的仪器是
溶液的仪器是_______ ,C装置的作用是_______ 。
(4)实验结束后,装置B中物质经_______ 、洗涤、干燥,得到 固体,洗涤时用
固体,洗涤时用 溶液洗涤
溶液洗涤 的目的是
的目的是_______ ,再用无水乙醇洗涤。
(5)碘化亚铜能用于检测空气中的汞蒸气,其反应为 (玫瑰红)
(玫瑰红) 。产物
。产物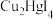 中,
中, 元素显
元素显_______ 价。当有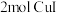 参与反应时,转移电子
参与反应时,转移电子_______ mol。
 )可用作树脂改性剂,不溶于水,能被
)可用作树脂改性剂,不溶于水,能被 氧化,见光易分解。实验室制备
氧化,见光易分解。实验室制备 的方法是向
的方法是向 和
和 混合溶液中通入足量
混合溶液中通入足量 ,实验装置如图所示(部分装置已省略)。请回答下列问题:
,实验装置如图所示(部分装置已省略)。请回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)装置B中发生反应的离子方程式是
(3)盛放
 溶液的仪器是
溶液的仪器是(4)实验结束后,装置B中物质经
 固体,洗涤时用
固体,洗涤时用 溶液洗涤
溶液洗涤 的目的是
的目的是(5)碘化亚铜能用于检测空气中的汞蒸气,其反应为
 (玫瑰红)
(玫瑰红) 。产物
。产物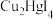 中,
中, 元素显
元素显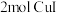 参与反应时,转移电子
参与反应时,转移电子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】各物质间的转化关系如图所示,请回答下列问题。

(1)写出B和D的化学式:B___________ ;D___________ 。
(2)写出E转变成F的化学方程式:___________ ;向G溶液加入A的离子方程式:___________ ,将饱和的G溶液加入到沸水中制备胶体的化学方程式。___________ 。
(3)工业上利用G溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀。请运用氧化还原反应的规律进行分析并写出反应的化学方程式:___________ ;每转移___________  电子腐蚀96g铜。
电子腐蚀96g铜。

(1)写出B和D的化学式:B
(2)写出E转变成F的化学方程式:
(3)工业上利用G溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀。请运用氧化还原反应的规律进行分析并写出反应的化学方程式:
 电子腐蚀96g铜。
电子腐蚀96g铜。
您最近一年使用:0次




