在Al2O3催化剂和加热的条件下,丁烷发生完全裂解:C4H10→C2H6+C2H4,C4H10→CH4+C3H6,某实验小组通过如图实验装置进行定性、定量测定丁烷裂解产物及其含量。
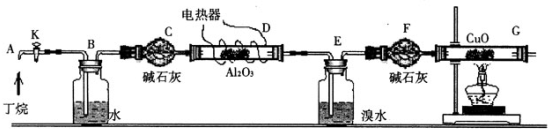
(1)C和F玻璃仪器的名称是________ 。
(2)参考装置图,连接好各仪器,________ ,加入各试剂,排除装置中的空气,加热D和G装置,B装置所起的作用是________ 。
(3)E装置中的实验现象是________ ;写出G装置中的反应的化学方程式_______ 。(写出一个即可)
(4)E和F装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷的摩尔分数是x=_____ %
(提示1:x= ×100%;提示2:假定流经D、G装置中的气体能完全反应)
×100%;提示2:假定流经D、G装置中的气体能完全反应)
(5)对E装置中的混合物再按以下流程实验:
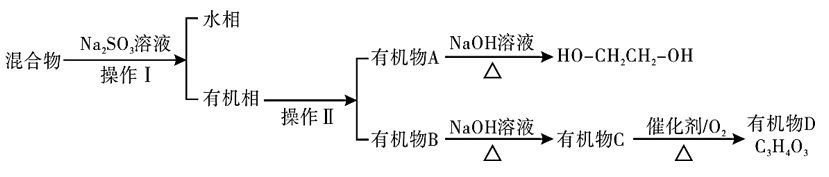
①Na2SO3溶液的作用是(用离子方程式表示)____ ,分离操作I、Ⅱ名称分别是____ 和______ 。
②有机物B的一种同系物E的分子式为C6H12Br2,其中有三个甲基的同分异构体有____ 种。

(1)C和F玻璃仪器的名称是
(2)参考装置图,连接好各仪器,
(3)E装置中的实验现象是
(4)E和F装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷的摩尔分数是x=
(提示1:x=
 ×100%;提示2:假定流经D、G装置中的气体能完全反应)
×100%;提示2:假定流经D、G装置中的气体能完全反应)(5)对E装置中的混合物再按以下流程实验:

①Na2SO3溶液的作用是(用离子方程式表示)
②有机物B的一种同系物E的分子式为C6H12Br2,其中有三个甲基的同分异构体有
更新时间:2020-12-02 16:42:30
|
相似题推荐
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
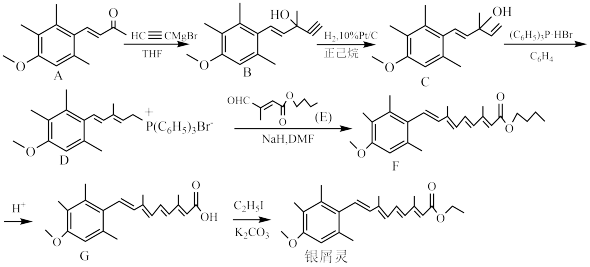
【推荐1】银屑灵是抗牛皮癣药,其一种合成路线如下。
(1)银屑灵中含氧官能团有_______ (填名称)。
(2)B→C的反应类型是_______ 。G→银屑灵中 的作用是
的作用是_______ 。
(3)设计实验证明E中含碳碳双键:_______ 。
(4)在镍、加热条件下,1 mol G最多能与_______ mol  反应。
反应。
(5)T是A的同系物,T的相对分子质量比A的小28.在T的同分异构体中,同时满足下列条件的结构有_______ 种(不包括立体异构体)。
①只含一种官能团且与苯环直接连接;②0.5 mol有机物与足量银氨溶液反应最多生成2.0 mol Ag;③苯环上只有3个取代基。
其中,在核磁共振氢谱上有4组峰的结构简式为_______ (写一种)。
(6)设计以一溴环己烷、 为原料合成
为原料合成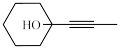 的合成路线:
的合成路线:_______ (其他无机试剂任选)。
(1)银屑灵中含氧官能团有
(2)B→C的反应类型是
 的作用是
的作用是(3)设计实验证明E中含碳碳双键:
(4)在镍、加热条件下,1 mol G最多能与
 反应。
反应。(5)T是A的同系物,T的相对分子质量比A的小28.在T的同分异构体中,同时满足下列条件的结构有
①只含一种官能团且与苯环直接连接;②0.5 mol有机物与足量银氨溶液反应最多生成2.0 mol Ag;③苯环上只有3个取代基。
其中,在核磁共振氢谱上有4组峰的结构简式为
(6)设计以一溴环己烷、
 为原料合成
为原料合成 的合成路线:
的合成路线:
您最近半年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐2】有机物H是合成雌酮激素的中间体,其合成路线如下:

已知:I.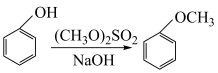
Ⅱ. (其中R为烃基)
(其中R为烃基)
请回答:
(1)B的分子式是___________ 。
(2)C中含氧官能团的名称为硝基、___________ 。
(3)下列说法正确的是___________。
(4)写出B→C的化学方程式___________ 。
(5)E的同分异构体中,同时满足下列条件的有___________ 种(不含立体异构),其中核磁共振氢谱有5组峰,且峰面积之比为6∶2∶2∶1∶1的结构简式为___________ 。
①苯环上有2个取代基;②能与 溶液发生显色反应;③能发生银镜和水解反应。
溶液发生显色反应;③能发生银镜和水解反应。
(6)参照上述合成路线,设计由甲苯为起始原料制备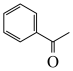 的合成路线
的合成路线________ (无机试剂任选)。

已知:I.

Ⅱ.
 (其中R为烃基)
(其中R为烃基)请回答:
(1)B的分子式是
(2)C中含氧官能团的名称为硝基、
(3)下列说法正确的是___________。
| A.A分子中所有原子肯定处于同一平面 |
| B.化合物B具有碱性 |
| C.D→E的反应类型为加成反应 |
D.F的结构简式为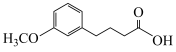 |
(4)写出B→C的化学方程式
(5)E的同分异构体中,同时满足下列条件的有
①苯环上有2个取代基;②能与
 溶液发生显色反应;③能发生银镜和水解反应。
溶液发生显色反应;③能发生银镜和水解反应。(6)参照上述合成路线,设计由甲苯为起始原料制备
 的合成路线
的合成路线
您最近半年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐3】化合物Ⅰ是合成抗HIV病毒活性药物的一种中间体,其合成路线如下:
(1)A→B加入稍过量 ,化学方程式为
,化学方程式为_________ ;A与 反应的目的是
反应的目的是_______ 。
(2)B的同分异构体中,含苯环且能发生水解反应,但不能发生银镜反应的有______ 种。
(3)C中不对称碳原子的个数为_____ ;试剂X的结构简式为_______ ;D中含氧官能团的名称为_______ 。
(4)G→H的反应类型为___________ ;Ⅰ中含有两个五元环,其结构简式为______ 。
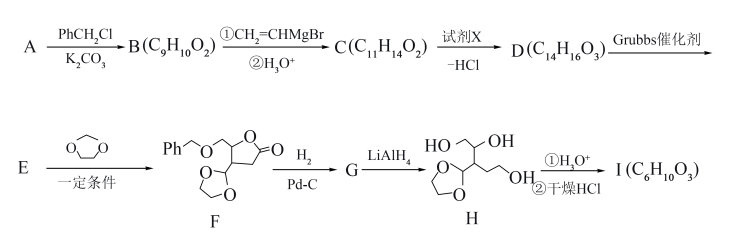
Ⅰ.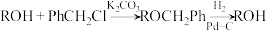
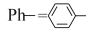
Ⅱ.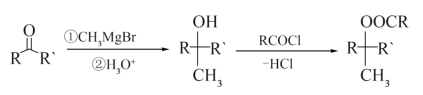 R,R'=H,羟基
R,R'=H,羟基
Ⅲ.
 ,
,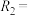 羟基
羟基
Ⅳ.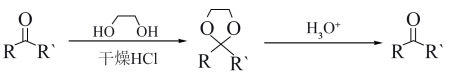
(1)A→B加入稍过量
 ,化学方程式为
,化学方程式为 反应的目的是
反应的目的是(2)B的同分异构体中,含苯环且能发生水解反应,但不能发生银镜反应的有
(3)C中不对称碳原子的个数为
(4)G→H的反应类型为
您最近半年使用:0次
解答题-有机推断题
|
较难
(0.4)
真题
解题方法
【推荐1】A、B、C、D1、D2、E、F、G、H均为有机化合物,请根据下列图示回答问题。
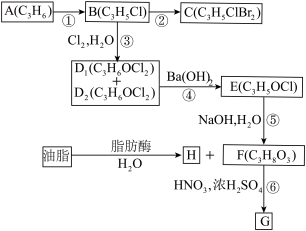 (1)直链有机化合物A的结构简式是
(1)直链有机化合物A的结构简式是_________________________ ;
(2)①的反应试剂和反应条件是____________________ ;
(3)③的反应类型是_______________________________ ;
(4)B生成C的化学方程式是_______________________________ ;
D1或D2生成E的化学方程式是_____________________________ ;
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是_____________ 。
 (1)直链有机化合物A的结构简式是
(1)直链有机化合物A的结构简式是(2)①的反应试剂和反应条件是
(3)③的反应类型是
(4)B生成C的化学方程式是
D1或D2生成E的化学方程式是
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是
您最近半年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】德国化学家Vogel于1979年合成了化合物F,它具有轮烯[10]的骨架,具有芳香性。B的氢谱有2个峰,峰面积之比为2:1;D的分子式为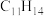 ,E有二重对称轴。
,E有二重对称轴。
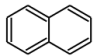
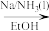 B
B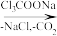 C
C D
D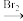 E
E F
F
(1)根据以上信息,写出B~F的结构简式:B____ C____ D____ E____ F____
(2)写出三氯乙酸钠分解后中间体的结构____ ,给出碳原子的价电子数____ 。
(3)E到F反应过程中,三元环开环的动力是____ 。
(4)解释F为什么具有芳香性,而轮烯[10]没有芳香性____ 。
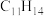 ,E有二重对称轴。
,E有二重对称轴。
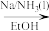 B
B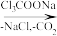 C
C D
D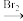 E
E F
F(1)根据以上信息,写出B~F的结构简式:B
(2)写出三氯乙酸钠分解后中间体的结构
(3)E到F反应过程中,三元环开环的动力是
(4)解释F为什么具有芳香性,而轮烯[10]没有芳香性
您最近半年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
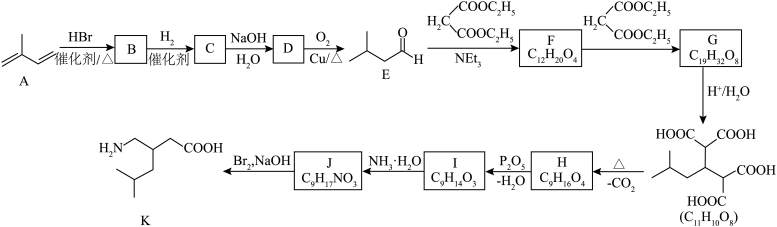
【推荐3】普瑞巴林(K)是一种作抗癫痫药物,可用异戊二烯(A)为原料来合成,路线如下图。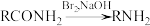
(1)A的官能团名称是__________ 。
(2)C的结构简式为__________ 。
(3)D→E的化学方程式是__________ 。
(4)F→G的反应类型为__________ 。
(5)I中含有一个六元环,H生成I的化学方程式是__________ 。
(6)将K中的碳原子编号标记为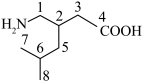 ,其中由
,其中由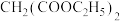 提供的碳原子的编号为
提供的碳原子的编号为__________ 。(填字母序号)。
a.1,2,3,4 b.1,3,4 c.2,3,4 d.1,2,3
ⅰ.
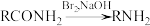
(1)A的官能团名称是
(2)C的结构简式为
(3)D→E的化学方程式是
(4)F→G的反应类型为
(5)I中含有一个六元环,H生成I的化学方程式是
(6)将K中的碳原子编号标记为
 ,其中由
,其中由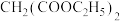 提供的碳原子的编号为
提供的碳原子的编号为a.1,2,3,4 b.1,3,4 c.2,3,4 d.1,2,3
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】三氯化硼(BC13,沸点为12.5℃,熔点为-107.3℃)可用作有机合成催化剂,某化学兴趣小组利用氯气和单质硼反应制备三氯化硼。已知三氯化硼遇水剧烈反应,生成硼酸(H3BO3为一元弱酸)和盐酸。该兴趣小组利用如图所示的部分装置(可重复选用)进行实验。
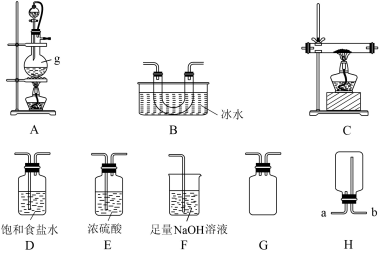
(1)仪器g的名称是___________ ,若用装置H收集氯气,气体应从___________ (填“a”或“b”)进入。
(2)装置的连接顺序依次为______ ,A→______→______→______→_____→______→_____→F,装置G的作用是:_______ 。
(3)NaH2BO3的电离方程式为___________ 。
(4)实验完成后,某同学向装置F中(溶液含有0.1mol∙L-1NaClO、0.1mol∙L-1NaCl、0.2mol∙L-1NaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因。
则x=___________ ,由实验得出的结论是___________ 。

(1)仪器g的名称是
(2)装置的连接顺序依次为
(3)NaH2BO3的电离方程式为
(4)实验完成后,某同学向装置F中(溶液含有0.1mol∙L-1NaClO、0.1mol∙L-1NaCl、0.2mol∙L-1NaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因。
| 实验序号 | 0.2mol∙L-1NaClO/mL | 0.2mol∙L-1NaCl/mL | 0.4mol∙L-1NaOH/mL | H2O/mL | 品红溶液 | 现象 |
| I | 0.0 | 15.0 | 15.0 | 0.0 | 4滴 | 不褪色 |
| II | 15.0 | 0.0 | 15.0 | 0.0 | 4滴 | 缓慢褪色 |
| III | 15.0 | 0.0 | 0.0 | x | 4滴 | 较快褪色 |
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
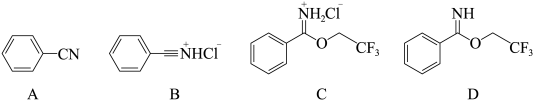
【推荐2】芳基亚胺酯是重要的有机反应中间体,受热易分解,可由腈在酸催化下与醇发生Pinner反应制备,原理如下图所示。
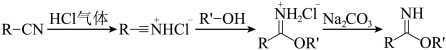
某实验小组以苯甲腈(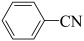 ,
,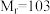 )和三氟乙醇(
)和三氟乙醇(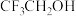 ,
,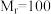 ) 为原料合成苯甲亚胺三氟乙酯。步骤如下:
) 为原料合成苯甲亚胺三氟乙酯。步骤如下:
I.将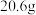 苯甲腈与
苯甲腈与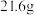 三氟乙醇置于容器中,冰浴降温至
三氟乙醇置于容器中,冰浴降温至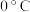 。
。
Ⅱ.向容器中持续通入 气体4小时,密封容器。
气体4小时,密封容器。
Ⅲ.室温下在 氛围中继续搅拌反应液24小时,冷却至
氛围中继续搅拌反应液24小时,冷却至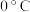 ,抽滤得白色固体,用乙腈洗涤。
,抽滤得白色固体,用乙腈洗涤。
IV.将洗涤后的白色固体加入饱和 溶液中,低温下反应,有机溶剂萃取3次,合并有机相。
溶液中,低温下反应,有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水 ,过滤,蒸去溶剂得产品
,过滤,蒸去溶剂得产品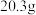 。
。
回答下列问题:
(1)实验室中可用浓盐酸和无水 制备干燥
制备干燥 气体,下列仪器中一定需要的为
气体,下列仪器中一定需要的为__________ (填仪器名称)。
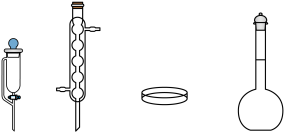
(2)第Ⅱ步通气完毕后,容器密封的原因为__________ 。
(3)第Ⅲ步中得到的白色固体主要成分为__________ 。
(4)第IV步中选择低温的原因为__________ 。
(5)第IV步萃取时可选用的有机溶剂为__________。
(6)第V步中无水 的作用为
的作用为____________________ 。
(7)本实验的产率为__________ 。
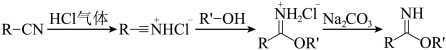
某实验小组以苯甲腈(
 ,
,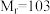 )和三氟乙醇(
)和三氟乙醇(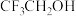 ,
,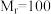 ) 为原料合成苯甲亚胺三氟乙酯。步骤如下:
) 为原料合成苯甲亚胺三氟乙酯。步骤如下:I.将
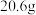 苯甲腈与
苯甲腈与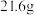 三氟乙醇置于容器中,冰浴降温至
三氟乙醇置于容器中,冰浴降温至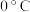 。
。Ⅱ.向容器中持续通入
 气体4小时,密封容器。
气体4小时,密封容器。Ⅲ.室温下在
 氛围中继续搅拌反应液24小时,冷却至
氛围中继续搅拌反应液24小时,冷却至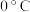 ,抽滤得白色固体,用乙腈洗涤。
,抽滤得白色固体,用乙腈洗涤。IV.将洗涤后的白色固体加入饱和
 溶液中,低温下反应,有机溶剂萃取3次,合并有机相。
溶液中,低温下反应,有机溶剂萃取3次,合并有机相。V.向有机相中加入无水
 ,过滤,蒸去溶剂得产品
,过滤,蒸去溶剂得产品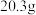 。
。回答下列问题:
(1)实验室中可用浓盐酸和无水
 制备干燥
制备干燥 气体,下列仪器中一定需要的为
气体,下列仪器中一定需要的为
(2)第Ⅱ步通气完毕后,容器密封的原因为
(3)第Ⅲ步中得到的白色固体主要成分为

(4)第IV步中选择低温的原因为
(5)第IV步萃取时可选用的有机溶剂为__________。
| A.丙酮 | B.乙酸 | C.乙酸乙酯 | D.甲醇 |
(6)第V步中无水
 的作用为
的作用为(7)本实验的产率为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】碘化锡(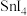 )主要用于制造有机锡配合物。某小组利用单质锡和碘制备碘化锡,其主要实验流程如下(反应装置见下图,夹持仪器略去):
)主要用于制造有机锡配合物。某小组利用单质锡和碘制备碘化锡,其主要实验流程如下(反应装置见下图,夹持仪器略去):
②碘化锡在丙酮和热的石油醚中溶解度较大,在冷的石油醚中溶解度小。
③石油醚的沸点为60~90℃,碘单质的升华温度为45~77℃。
请回答:
(1)反应装置中仪器X的名称是___________ 。
(2)下列说法不正确的是___________。
(3)反应装置中,为使紫色碘蒸气上升不高于冷凝管的中间部位,可采取的措施是___________ 。判断“反应装置”中的反应已完全的实验现象是___________ 。
(4)步骤 ,圆底烧瓶中还附着四碘化锡晶体,处理的方法是
,圆底烧瓶中还附着四碘化锡晶体,处理的方法是___________ 。
(5)产品中的杂质可以进一步采用重结晶法提纯。请从下列选项中选择最佳选项并进行排序。___________
取碘化锡样品放入烧杯中→___________→___________→___________
a.加入适量的热水
b.加入适量的热的石油醚
c.用冷水浴冷却结晶
d.趁热过滤
e.加入适量的冷的石油醚
(6)该小组对制备的碘化锡产品进行性质和组成上的研究。
①取适量的产品溶解在2mL丙酮中配成溶液,再加入1ml蒸馏水,产生白色无定型沉淀,写出反应的化学方程式___________ 。
②本实验可以通过测定某些物理量来确定碘化锡的化学式,需测定的物理量有___________ 。
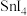 )主要用于制造有机锡配合物。某小组利用单质锡和碘制备碘化锡,其主要实验流程如下(反应装置见下图,夹持仪器略去):
)主要用于制造有机锡配合物。某小组利用单质锡和碘制备碘化锡,其主要实验流程如下(反应装置见下图,夹持仪器略去):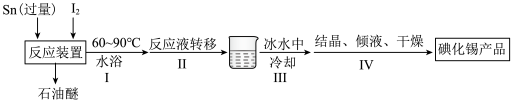
②碘化锡在丙酮和热的石油醚中溶解度较大,在冷的石油醚中溶解度小。
③石油醚的沸点为60~90℃,碘单质的升华温度为45~77℃。
请回答:
(1)反应装置中仪器X的名称是
(2)下列说法不正确的是___________。
| A.将锡片剪成细小碎片、碘磨细的原因是充分反应,同时提高反应速率 |
| B.仪器X的作用是吸收石油醚,防止石油醚扩散到空气中 |
C.步骤 可以不转移反应液,直接在原反应装置(圆底烧瓶)中进行后续操作 可以不转移反应液,直接在原反应装置(圆底烧瓶)中进行后续操作 |
D.步骤 采用蒸发结晶比冷却结晶更好 采用蒸发结晶比冷却结晶更好 |
(3)反应装置中,为使紫色碘蒸气上升不高于冷凝管的中间部位,可采取的措施是
(4)步骤
 ,圆底烧瓶中还附着四碘化锡晶体,处理的方法是
,圆底烧瓶中还附着四碘化锡晶体,处理的方法是(5)产品中的杂质可以进一步采用重结晶法提纯。请从下列选项中选择最佳选项并进行排序。
取碘化锡样品放入烧杯中→___________→___________→___________
a.加入适量的热水
b.加入适量的热的石油醚
c.用冷水浴冷却结晶
d.趁热过滤
e.加入适量的冷的石油醚
(6)该小组对制备的碘化锡产品进行性质和组成上的研究。
①取适量的产品溶解在2mL丙酮中配成溶液,再加入1ml蒸馏水,产生白色无定型沉淀,写出反应的化学方程式
②本实验可以通过测定某些物理量来确定碘化锡的化学式,需测定的物理量有
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】(1)用铜与浓硫酸反应制取硫酸铜,实验装置如图所示。
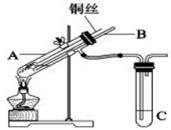
①A中反应体现了浓硫酸的哪些性质?______________________________ ;
②装置中导管B的作用你认为可能是(写出一种)_________________________________ 。
(2)为符合绿色化学的要求,某同学进行如下设计:将铜粉在___________________________ (填仪器名称)中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应,反应后溶液经过_________ 、_________ 、过滤、洗涤、干燥,即可得到产品CuSO4·5H2O晶体,干燥时需要控制温度小于100℃,若温度过高,则会导致___________________________ 。
(3)探究小组用滴定法测定某胆矾晶体中CuSO4的含量。取ag样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol·L-1的EDTA(H2Y2﹣)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应如下:Cu2++H2Y2-=CuY2-+2H+
①写出计算CuSO4质量分数的计算式 =
=________________________ ;
②下列操作会导致CuSO4含量的测定结果偏低的是_______________ 。
a.用样品溶液润洗锥形瓶
b.滴定终点时俯视读数
c.滴定终点时滴定管尖嘴中有气泡
(4)常温下CuSO4溶液中Cu2+水解的离子方程式为_________________ 。已知该反应的平衡常数K=5.0×10-9,则常温下Cu(OH)2的Ksp=_______________________

①A中反应体现了浓硫酸的哪些性质?
②装置中导管B的作用你认为可能是(写出一种)
(2)为符合绿色化学的要求,某同学进行如下设计:将铜粉在
(3)探究小组用滴定法测定某胆矾晶体中CuSO4的含量。取ag样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol·L-1的EDTA(H2Y2﹣)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应如下:Cu2++H2Y2-=CuY2-+2H+
①写出计算CuSO4质量分数的计算式
 =
=②下列操作会导致CuSO4含量的测定结果偏低的是
a.用样品溶液润洗锥形瓶
b.滴定终点时俯视读数
c.滴定终点时滴定管尖嘴中有气泡
(4)常温下CuSO4溶液中Cu2+水解的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】氯化铈常用于石油催化剂、汽车尾气催化剂、中间化合物等行业。为充分利用资源,以废料(主要含 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备氯化铈的工艺流程如图所示:
)为原料制备氯化铈的工艺流程如图所示:
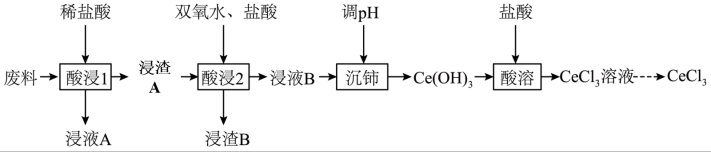
已知: 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。
回答下列问题:
(1)加入过量稀盐酸后“浸渣A”的成分为___________ (填化学式),“浸渣B”的主要用途为___________ (填一种)。
(2)“酸浸2”中发生反应的离子方程式为___________ 。
(3) 及其氧化产物
及其氧化产物 可用于处理硝酸厂烟气中的氮氧化物(
可用于处理硝酸厂烟气中的氮氧化物( ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与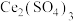 的混合溶液中,其转化过程如下图:
的混合溶液中,其转化过程如下图:

该处理过程中可减少下列环境问题产生___________ (填序号)。
①酸雨 ②光化学烟雾 ③白色污染
(4)取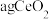 ,经铝热反应可得
,经铝热反应可得 ,该铝热反应的化学方程式为
,该铝热反应的化学方程式为___________ ,该反应中铈的产率为___________ (用含a、b的代数式表示)。
 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备氯化铈的工艺流程如图所示:
)为原料制备氯化铈的工艺流程如图所示:
已知:
 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。回答下列问题:
(1)加入过量稀盐酸后“浸渣A”的成分为
(2)“酸浸2”中发生反应的离子方程式为
(3)
 及其氧化产物
及其氧化产物 可用于处理硝酸厂烟气中的氮氧化物(
可用于处理硝酸厂烟气中的氮氧化物( ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与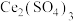 的混合溶液中,其转化过程如下图:
的混合溶液中,其转化过程如下图:
该处理过程中可减少下列环境问题产生
①酸雨 ②光化学烟雾 ③白色污染
(4)取
 ,经铝热反应可得
,经铝热反应可得 ,该铝热反应的化学方程式为
,该铝热反应的化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】碱式碳酸铜在烟火、农药、颜料、杀菌剂等方面应用广泛。一种以辉铜矿(Cu2S,含有SiO2和少量Fe2O3等杂质)为原料制备碱式碳酸铜的流程如图所示:
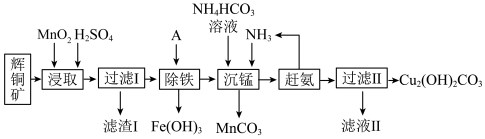
已知:CS2,为无色液体,是硫、磷、硒、溴、碘、樟脑等的良好溶剂,具有挥发性。
回答下列问题:
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有_______ (任写一种)。
(2)滤渣I经CS2提取后可获得一种淡黄色副产品,则滤渣I中的主要成分是_______ (填化学式)。由CS2回收滤渣I中的淡黄色副产品过程中温度控制在50~60℃之间,不宜过高或过低的原因是_______ 。
(3)“除铁”时检验Fe3+是否除尽时常用的化学试剂_______ 。
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式:_______ 。
(5)“赶氨”时,最适宜的操作方法是_______ 。
(6)测定副产品MnSO4·H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的BaCl2溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为_______ (保留到小数点后两位)

已知:CS2,为无色液体,是硫、磷、硒、溴、碘、樟脑等的良好溶剂,具有挥发性。
回答下列问题:
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有
(2)滤渣I经CS2提取后可获得一种淡黄色副产品,则滤渣I中的主要成分是
(3)“除铁”时检验Fe3+是否除尽时常用的化学试剂
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式:
(5)“赶氨”时,最适宜的操作方法是
(6)测定副产品MnSO4·H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的BaCl2溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为
您最近半年使用:0次



