下列有关仪器使用方法或实验操作正确的是
| A.洗净的锥形瓶和容量瓶必须放进烘箱中烘干才能开始实验 |
| B.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 |
| C.酸式滴定管装标准溶液前,必须先用该溶液润洗 |
| D.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差 |
更新时间:2020-12-05 20:53:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作正确的是( )
| A.滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸 |
| B.锥形瓶用蒸馏水洗净后,直接加入未知浓度的NaOH待测液 |
| C.滴定前没有排出滴定管尖嘴处的气泡 |
| D.读数时视线与滴定管内液体的凹液面最底处保持水平 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用标准的盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是
| A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 |
| B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 |
| C.用碱式滴定管取10.00 mLNaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量指示剂进行滴定 |
| D.用酚酞作指示剂滴至红色刚变无色时即停止加盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用酚酞作指示剂,以0.100 mol·L-1的NaOH溶液测定锥形瓶中一定体积的盐酸的物质的量浓度。下列操作将导致测定值高于实际值的是( )
| A.标准液在“0”刻度线以上,未予调整就开始滴定 |
| B.滴定过程中振荡时,锥形瓶中有液滴溅出 |
| C.观察记录滴定管内液面刻度时滴定前俯视,滴定后仰视 |
| D.酚酞指示剂由无色变为红色时立即停止滴定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作会使结果偏小的是
A.用酸式滴定管量取 盐酸,开始时平视,结束时仰视,读取所量液体的体积 盐酸,开始时平视,结束时仰视,读取所量液体的体积 |
B.用玻璃棒蘸取少量氯化钠溶液滴在湿润的 试纸上 试纸上 |
C.中和反应反应热 的测定实验中,测了 的测定实验中,测了 溶液起始温度后的温度计未洗涤,直接测定 溶液起始温度后的温度计未洗涤,直接测定 溶液的温度 溶液的温度 |
| D.用已知浓度的盐酸滴定未知浓度的氢氧化钠时,酸式滴定管刚开始有气泡,读数时,气泡消失 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关实验操作的叙述错误的是( )
| A.测定中和热实验时,用铜丝替代环形玻璃搅拌棒,会使实验所得的ΔH偏高 |
| B.取淀粉的水解液少许,先加入过量的氢氧化钠溶液,再加入新制的氢氧化铜,加热,若产生砖红色沉淀,则证明淀粉的水解产物有还原性。 |
| C.测定醋酸钠溶液的pH可用洁净的玻璃棒蘸取待测液,点在湿润的pH试纸上,与标准比色卡对比读数。 |
| D.用已知浓度的盐酸测定未知浓度的氢氧化钠溶液,当滴定达终点时滴定管尖嘴有悬液,则测定结果偏高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室需要使用240mL0.1000mol·L-1FeCl3溶液,现用FeCl3•6H2O晶体(设摩尔质量为ag·mol-1)配制该溶液,下列有关说法正确的是
| A.需要称取0.024agFeCl3•6H2O晶体 |
| B.需要先加热除去结晶水 |
| C.该实验中玻璃棒的作用为搅拌 |
| D.定容时若俯视刻度线会导致配制的溶液浓度偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某同学在实验报告中记录下列数据,其中正确的是()
| A.用10mL量筒量取7.36mLNaOH溶液 |
| B.用托盘天平称取6.85g食盐 |
| C.实验室配制480ml的碳酸钠溶液需要使用500ml容量瓶 |
| D.用广泛pH试纸测得某溶液pH为5.5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】草酸晶体(H2C2O4⋅2H2O)用途广泛,易溶于水,其制备及纯度测定实验如下。
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为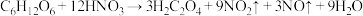 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。
Ⅱ.纯度测定
称取制得的草酸晶体 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为
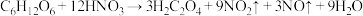 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。Ⅱ.纯度测定
称取制得的草酸晶体
 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是| A.配制溶液时容量瓶底部残留少量水,会导致所配溶液浓度偏低 |
| B.滴加“混酸”速度过快,不影响草酸晶体的产率 |
| C.锥形瓶用草酸溶液润洗,所测产品纯度会偏低 |
| D.滴定终点读数时仰视,所测产品纯度偏高 |
您最近一年使用:0次



