对可逆反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),下列叙述正确的是
| A.达到化学平衡时,6v正(O2)=5v逆(H2O) |
| B.化学反应速率关系是:2v正(NH3)=3v逆(H2O) |
| C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| D.若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 |
更新时间:2020/12/15 17:51:34
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在带有活塞的密闭容器中发生反应: ,采取下列措施不能改变反应速率的是( )
,采取下列措施不能改变反应速率的是( )
 ,采取下列措施不能改变反应速率的是( )
,采取下列措施不能改变反应速率的是( )A.增加 的量 的量 | B.保持容器体积不变,增加 的量 的量 |
C.充入 ,保持容器内压强不变 ,保持容器内压强不变 | D.充入 ,保持容器体积不变 ,保持容器体积不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】H2(g)+I2(g) 2HI(g) △H=-Q(Q>0),下列说法正确的是
2HI(g) △H=-Q(Q>0),下列说法正确的是
 2HI(g) △H=-Q(Q>0),下列说法正确的是
2HI(g) △H=-Q(Q>0),下列说法正确的是| A.温度升高,反应速率增大,产率增大 | B.增大反应物H2的浓度,HI%增大 |
| C.增大压强,浓度增大,平衡不移动 | D.使用催化剂,反应速率增大,I2的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)⇌2Z(g)。该反应达到平衡的标志是:
| A.容器内X、Y、Z的浓度不随时间而变化 |
| B.容器内X、Y、Z的浓度之比为1∶2∶2 |
| C.单位时间里消耗0.1 mol X同时生成0.2 mol Z |
| D.容器内压强不随时间变化,且比反应前压强大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于可逆反应2A(g)+3B(g) 3C(g),在一定条件下,使一定量气体A和气体B反应,达到平衡状态时,具有的关系是
3C(g),在一定条件下,使一定量气体A和气体B反应,达到平衡状态时,具有的关系是
 3C(g),在一定条件下,使一定量气体A和气体B反应,达到平衡状态时,具有的关系是
3C(g),在一定条件下,使一定量气体A和气体B反应,达到平衡状态时,具有的关系是| A.单位时间内,若消耗了amolA物质,则同时也消耗了1.5amolC物质 |
B.平衡混合物体积是反应开始前的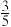 |
| C.平衡混合物中各物质的量浓度相等 |
| D.各物质的量浓度之比为c(A):c(B):c(C)=2:3:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ΔH=-115.6kJ·mol-1。恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是( )
2Cl2(g)+2H2O(g) ΔH=-115.6kJ·mol-1。恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是( )
| A.气体的质量不再改变 |
| B.氯化氢的转化率不再改变 |
| C.断开4molH—Cl键的同时生成4molH—O键 |
| D.n(HCl)∶n(O2)∶n(Cl2)∶n(H2O)=4∶1∶2∶2 |
您最近一年使用:0次
【推荐1】在一定体积的密闭容器中,进行如下化学反应:2X(g)+Y(s) Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
下列叙述不正确的是
 Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表| t℃ | 700 | 800 | 900 | 1000 | 1200 |
| K | 0.6 | 1.0 | 1.3 | 1.8 | 2.7 |
| A.上述反应的正反应是吸热反应 |
B.该反应的化学平衡常数表达式为K=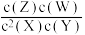 |
| C.若在1L的密闭容器中通入X和Y各0.3mol,5min后温度升高到800℃,此时测得X为0.1mol,该反应达到平衡状态 |
| D.混合气体的密度保持不变可作为该反应达到平衡的标志之一 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在三种不同条件下,分别向容积为2 L的恒容密闭容器中充入2 mol A和 1 mol B,发生反应如下:2A (g) +B(g) 2D(g) ΔH=−Q kJ·mol-1,相关条件和数据见下表。
2D(g) ΔH=−Q kJ·mol-1,相关条件和数据见下表。
下列说法中正确的是
 2D(g) ΔH=−Q kJ·mol-1,相关条件和数据见下表。
2D(g) ΔH=−Q kJ·mol-1,相关条件和数据见下表。| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 反应温度/ ℃ | 800 | 800 | 850 |
| 达平衡时间/min | 40 | 10 | 30 |
| c(D)平衡/mol·L-1 | 0.5 | 0.5 | 0.15 |
| 反应的能量变化/kJ | Q1 | Q2 | Q3 |
| A.可用压强或密度是否发生变化判断上述反应是否达平衡状态 |
| B.实验Ⅱ可能隐含的条件是使用催化剂,实验Ⅲ达平衡时v(D)为0.05 mol·L-1·min-1 |
| C.由表中信息可知Q>0,并且有Q3<Q1=Q2=Q |
| D.实验Ⅰ达平衡后,恒温下再向容器中通入2 mol A和1 mol B,新平衡时c(D)大于1.0 mol·L-1 |
您最近一年使用:0次

 2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是
2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 

