醇是重要的有机化工原料。一定条件下,甲醇可同时发生下面两个反应:
i .2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
ii.2CH3OH(g) C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)
(1)上述反应过程中能量变化如图所示:
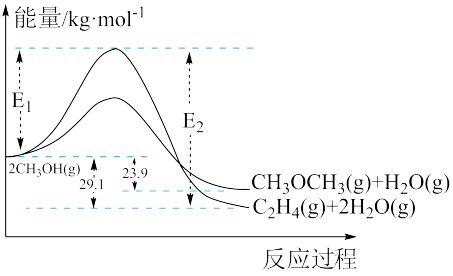
在某密闭容器中,充入一定量CH3OH(g)发生上述两个反应,反应________ (填“i”或“ii”)的速率较大,其原因为___________ 。若在容器中加入催化剂,使ii的反应速率增大,则E1和E2−E1的变化是:E1__________ ;E2−E1___________ (填“增大”、“减小”或“不变”)。
(2)已知:CH3CH2OH(g)=CH3OCH3(g) ΔH =+50.7 kJ∙mol−1。则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的ΔH=______ 。
i .2CH3OH(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)ii.2CH3OH(g)
 C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)(1)上述反应过程中能量变化如图所示:

在某密闭容器中,充入一定量CH3OH(g)发生上述两个反应,反应
(2)已知:CH3CH2OH(g)=CH3OCH3(g) ΔH =+50.7 kJ∙mol−1。则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的ΔH=
更新时间:2020-12-06 20:01:20
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】有些盐的结晶水合物,白天在温度不太高时就能熔化(实质是溶于自身的结晶水中),同时吸收热量;在晚上又可缓慢凝固而释放热量,用以调节室温,称为潜热材料。现有几种盐的水合晶体有关数据如下
(1)上述四种水合晶体盐中最适宜用做潜热材料的两种盐是(用化学式表示)____________________________ ;______________________________ 。
(2)实际应用时最常采用的(由来源和成本考虑)应该是________________________ 。
| Na2S2O3·5H2O | CaCl2·6H2O | Na2SO4·10H2O | Na2HPO4·12H2O | |
| 熔点(℃) | 40.50 | 29.92 | 32.38 | 35.1 |
| 熔化热(kJ/mol) | 49.7 | 37.3 | 77 | 100.1 |
(1)上述四种水合晶体盐中最适宜用做潜热材料的两种盐是(用化学式表示)
(2)实际应用时最常采用的(由来源和成本考虑)应该是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求回答下列问题:
(1)某同学做如下实验,以检验反应中的能量变化。
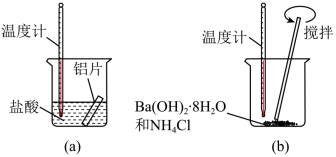
①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是_______ 热反应,(b)中温度降低,由此可以判断(b)中反应是_______ 热反应。
②写出铝与盐酸反应的离子方程式:_______ 。
③根据能量守恒定律,(b)中反应物的总能量应该_______ (填“高于”或“低于”)其生成物的总能量。
(2)如图表示1mol 与1mol
与1mol 反应生成2molHCl的能量变化的理论分析示意图。
反应生成2molHCl的能量变化的理论分析示意图。
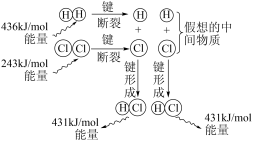
①化学键断裂需要_______ (填“释放”或“吸收”)能量。
②图中共释放的能量为_______ kJ。
③该反应的反应物的总能量_______ (填“大于”、“等于”或“小于”)生成物的总能量,所以该反应是_______ 反应。
(1)某同学做如下实验,以检验反应中的能量变化。

①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
②写出铝与盐酸反应的离子方程式:
③根据能量守恒定律,(b)中反应物的总能量应该
(2)如图表示1mol
 与1mol
与1mol 反应生成2molHCl的能量变化的理论分析示意图。
反应生成2molHCl的能量变化的理论分析示意图。
①化学键断裂需要
②图中共释放的能量为
③该反应的反应物的总能量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】胶状液氢(主要含有H2和CH4)有望用于未来的运载火箭。实验测得298K和101kPa时,氢气和甲烷燃烧热分别为△H氢气=-286 kJ/mol,△H甲烷=-891 kJ/mol
(1)写出CH4的电子式____________ 。
(2)下列热化学方程式书写正确的是_______(单选)
(3)下列有关焓与焓变的说法,正确的是_____。(双选)
(1)写出CH4的电子式
(2)下列热化学方程式书写正确的是_______(单选)
| A.2H2(g)+O2(g)=2H2O(g) △H= +286 kJ mol |
| B.2H2(g)+O2(g)=2H2O(l) △H =- 572 kJ/mol |
| C.2CH4(g)+3O2(g)=2CO(g)+4H2O(1) △H = -1782 kJ/mol |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =- 891 kJ/mol |
| A.系统状态发生变化,焓也随之改变 |
| B.当焓变小于0时,化学反应为吸热反应 |
| C.如果反应是在恒温恒容、只做体积功条件下进行的反应热与焓变相等 |
| D.如果反应是在恒温恒压、只做体积功条件下进行的反应热与焓变相等 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】反应热和焓变
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境_______ 的热量。
(2)焓变
①焓(H):焓是与内能有关的物理量。
②焓变( ):生成物的焓与反应物的焓之差。
):生成物的焓与反应物的焓之差。
③焓变与反应热的关系
等压条件下的反应热等于反应的焓变,常用_______ 表示反应热,常用单位:_______ 。
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境
(2)焓变
①焓(H):焓是与内能有关的物理量。
②焓变(
 ):生成物的焓与反应物的焓之差。
):生成物的焓与反应物的焓之差。③焓变与反应热的关系
等压条件下的反应热等于反应的焓变,常用
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。
(1)该反应为_______ (填“吸热”或“放热”)反应。
(2)当反应达到平衡时,N2和H2的浓度比是_______ ;N2和H2的转化率之比是_______ 。
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_______ ,密度_______ 。(填“增大”“减小”或“不变”)
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将_______ (填“正向”“逆向”或“不”)移动。
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将_______ (填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_______ (填“大于”“小于”或“等于”)原来的2倍。
 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。(1)该反应为
(2)当反应达到平衡时,N2和H2的浓度比是
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】亚硝酰氯(NOCl)是有机合成中的重要试剂。通常条件下,NO和Cl2反应生成NOC1,其能量变化如图所示。
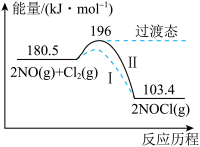
回答下列问题:
(1)曲线Ⅱ中正反应的活化能E1为_______________ ,逆反应的活化能E2为___________ 。 该反应能在通常情况下进行的主要原因是_____________________________ 。
(2)加入催化剂的曲线为_________________ (填“I”或“Ⅱ”)。加入催化剂,能提高化学反应速率的原因是_______________________________________________________ 。
(3)催化剂不能使平衡移动的原因是_________________________________________ 。
(4)上述合成NOCl(g)的热化学方程式为__________________________________ 。

回答下列问题:
(1)曲线Ⅱ中正反应的活化能E1为
(2)加入催化剂的曲线为
(3)催化剂不能使平衡移动的原因是
(4)上述合成NOCl(g)的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】沼气(主要成分是甲烷)是一种廉价的能源,把农村中大量存在的农作物秸秆、杂草、人畜粪便等在沼气池中发酵,便可产生沼气,沼气完全燃烧可以用来点灯、做饭。
(1)在101kPa时,32gCH4燃烧生成CO2和气态H2O,放出1604kJ的热量,写出甲烷燃烧的热化学方程式为__________________________________________________________ 。
(2)120℃,取CH4和过量O2的混合气体共0.4mol,点燃使其充分反应,将燃烧后的气体通过足量的碱石灰(NaOH和CaO的固体混合物)充分吸收,碱石灰增重8g。计算:
①原混合气体中CH4和O2的体积比是多少? ②反应放出多少热量?
___________
(1)在101kPa时,32gCH4燃烧生成CO2和气态H2O,放出1604kJ的热量,写出甲烷燃烧的热化学方程式为
(2)120℃,取CH4和过量O2的混合气体共0.4mol,点燃使其充分反应,将燃烧后的气体通过足量的碱石灰(NaOH和CaO的固体混合物)充分吸收,碱石灰增重8g。计算:
①原混合气体中CH4和O2的体积比是多少? ②反应放出多少热量?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】依据事实,写出下列反应的热化学方程式
(1)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成1molAX5,放出热量123.8kJ。该反应的热化学方程式为_______ 。
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为_______ 。
(3)化学反应N2+3H2=2NH3的能量变化如图所示

试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:_______ 。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是_______ 。
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的热化学方程式为_______ 。
(6)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式_______ 。

(1)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成1molAX5,放出热量123.8kJ。该反应的热化学方程式为
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为
(3)化学反应N2+3H2=2NH3的能量变化如图所示

试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的热化学方程式为
(6)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

您最近一年使用:0次
【推荐1】在环境污染和能源危机日益严重的情况下,氢气作为很有发展前景的新型能源备受青睐,获取氢气的方式有很多。
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
已知:①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+ O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ O2(g)=H2O(g) ΔH3=-242kJ·mol-1
O2(g)=H2O(g) ΔH3=-242kJ·mol-1
计算反应①的ΔH1=______________ 。
(2)如图为两种制备氢气的方法。

①书写系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式__________ 。
②若制得等量H2时,比较两种系统所需能量的大小_____ 。
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
已知:①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+
 O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1③H2(g)+
 O2(g)=H2O(g) ΔH3=-242kJ·mol-1
O2(g)=H2O(g) ΔH3=-242kJ·mol-1计算反应①的ΔH1=
(2)如图为两种制备氢气的方法。

①书写系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式
②若制得等量H2时,比较两种系统所需能量的大小
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
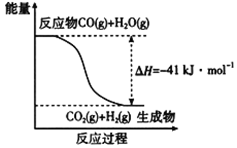
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示,反应的热化学方程式为____________________________________________ 。
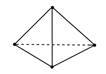
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1 mol N—N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,1mol N4生成N2的ΔH=_________ kJ·mol-1
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。298K时,已知:
①C(s,石墨)+O2(g) CO2(g) ΔH1=a kJ·mol-1
CO2(g) ΔH1=a kJ·mol-1
②2H2(g)+O2(g) 2H2O(l) ΔH2=b kJ·mol-1
2H2O(l) ΔH2=b kJ·mol-1
③2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) ΔH3=c kJ·mol-1
4CO2(g)+2H2O(l) ΔH3=c kJ·mol-1
则反应:2C(s,石墨)+H2(g) C2H2(g) 的焓变ΔH=
C2H2(g) 的焓变ΔH=__________ (用含a、b、c的式子表示)。
(4)已知:铝热反应是放热反应,又知,常温下:
4Al(s)+3O2(g) 2Al2O3(s) ΔH1
2Al2O3(s) ΔH1
4Fe(s)+3O2(g) 2Fe2O3(s) ΔH2
2Fe2O3(s) ΔH2
下面关于ΔH1、ΔH2的比较正确的是____________
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法比较
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示,反应的热化学方程式为

(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1 mol N—N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,1mol N4生成N2的ΔH=

(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。298K时,已知:
①C(s,石墨)+O2(g)
 CO2(g) ΔH1=a kJ·mol-1
CO2(g) ΔH1=a kJ·mol-1②2H2(g)+O2(g)
 2H2O(l) ΔH2=b kJ·mol-1
2H2O(l) ΔH2=b kJ·mol-1③2C2H2(g)+5O2(g)
 4CO2(g)+2H2O(l) ΔH3=c kJ·mol-1
4CO2(g)+2H2O(l) ΔH3=c kJ·mol-1则反应:2C(s,石墨)+H2(g)
 C2H2(g) 的焓变ΔH=
C2H2(g) 的焓变ΔH=(4)已知:铝热反应是放热反应,又知,常温下:
4Al(s)+3O2(g)
 2Al2O3(s) ΔH1
2Al2O3(s) ΔH14Fe(s)+3O2(g)
 2Fe2O3(s) ΔH2
2Fe2O3(s) ΔH2下面关于ΔH1、ΔH2的比较正确的是
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法比较
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】工业上,裂解丁烷可以获得乙烯、丙烯等化工原料。
反应1:C4H10(g,正丁烷) CH4(g)+C3H6(g) △H1
CH4(g)+C3H6(g) △H1
反应2:C4H10(g,正丁烷) C2H6(g)+C2H4(g) △H2
C2H6(g)+C2H4(g) △H2
已知几种烃的燃烧热如下:
回答下列问题:
(1)根据上述数据计算,△H1=___ kJ∙mol−1。
(2)稳定性:正丁烷___ 异丁烷(填“大于”“小于”或“等于”)。
(3)在密闭容器中投入一定量的正丁烷,发生上述反应1和2,测定丁烷的平衡转化率(α)与压强(p)、温度(T)关系如图所示。

①在相同压强下,升高温度,丁烷的平衡转化率增大的原因是___ 。
②比较压强大小:p1___ p2___ p3(填“>”“<”或“=”)。
(4)某温度下,向2L恒容密闭容器中投入2mol正丁烷.假设控制反应条件,只发生反应1,达到平衡时测得CH4的体积分数为 。
。
①下列情况表明上述反应达到平衡的是___ (填字母,双选)。
A.混合气体的密度保持不变 B.甲烷、丙烯的生成速率相等
C.混合气体压强保持不变 D.丙烯体积分数保持不变
②该温度下,反应1的平衡常数K=___ 。
反应1:C4H10(g,正丁烷)
 CH4(g)+C3H6(g) △H1
CH4(g)+C3H6(g) △H1反应2:C4H10(g,正丁烷)
 C2H6(g)+C2H4(g) △H2
C2H6(g)+C2H4(g) △H2已知几种烃的燃烧热如下:
| 烃 | 正丁烷 | 异丁烷 | 甲烷 | 乙烷 | 乙烯 | 丙烯 |
| 燃烧热(△H)/( kJ∙mol−1) | −2878 | −2869 | −890.3 | −1559.8 | −1411 | −2058.3 |
回答下列问题:
(1)根据上述数据计算,△H1=
(2)稳定性:正丁烷
(3)在密闭容器中投入一定量的正丁烷,发生上述反应1和2,测定丁烷的平衡转化率(α)与压强(p)、温度(T)关系如图所示。

①在相同压强下,升高温度,丁烷的平衡转化率增大的原因是
②比较压强大小:p1
(4)某温度下,向2L恒容密闭容器中投入2mol正丁烷.假设控制反应条件,只发生反应1,达到平衡时测得CH4的体积分数为
 。
。①下列情况表明上述反应达到平衡的是
A.混合气体的密度保持不变 B.甲烷、丙烯的生成速率相等
C.混合气体压强保持不变 D.丙烯体积分数保持不变
②该温度下,反应1的平衡常数K=
您最近一年使用:0次

 的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:


