将Fe和Al按一定的质量比组成合金。
(1)取一定量的该合金,向其中加入足量NaOH溶液,生成气体nL(标准状况),则反应的离子方程式是___ ,该反应在转移电子数___________ NA,合金中Al的物质的量是___________ 。
(2)另取相同质量的该合金,向其中加入足量稀硫酸,固体全部溶解,生成气体m L(标准状况),则反应中转移电子的物质的量是____ mol,合金中Fe的质量是___________ 。
(1)取一定量的该合金,向其中加入足量NaOH溶液,生成气体nL(标准状况),则反应的离子方程式是
(2)另取相同质量的该合金,向其中加入足量稀硫酸,固体全部溶解,生成气体m L(标准状况),则反应中转移电子的物质的量是
更新时间:2020-12-28 17:31:47
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】含2molH2SO4的浓硫酸与足量的铜片在加热条件下完全反应,可产生NA个SO2气体分子___
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】酸奶作为世界公认的长寿食品之一正愈来愈受到人们的重视和喜爱。酸奶中的酸味来自乳酸(化学式为C3H6O3)。
(1)乳酸属于哪一类物质:___________ (填“氧化物”、“酸”、“碱”、“盐”),乳酸(C3H6O3)中碳元素的化合价是___________ 价,碳:氢:氧的质量比为:___________
(2)为了测定某品牌酸奶中乳酸的含量,某同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.4%的NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH溶液体积V的变化关系如图所示。计算每100mL酸奶中乳酸的含量为多少克。(已知:乳酸与NaOH溶液反应的化学方程式为NaOH+CH3CH(OH)COOH=CH3CH(OH)COONa+H2O,测定所用NaOH溶液的密度为1.0g/mL,计算结果精确到0.01,无计算过程不给分)。___________

(1)乳酸属于哪一类物质:
(2)为了测定某品牌酸奶中乳酸的含量,某同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.4%的NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH溶液体积V的变化关系如图所示。计算每100mL酸奶中乳酸的含量为多少克。(已知:乳酸与NaOH溶液反应的化学方程式为NaOH+CH3CH(OH)COOH=CH3CH(OH)COONa+H2O,测定所用NaOH溶液的密度为1.0g/mL,计算结果精确到0.01,无计算过程不给分)。

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】向20 mL某浓度的AlCl3溶液中滴加2 mol·L-1的NaOH溶液时,得到Al(OH)3沉淀的质量(g)与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
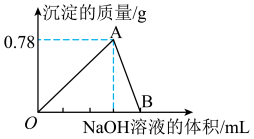
(1)图中A点表示的沉淀是__________ (写化学式),其物质的量为____________ 。
(2)反应至A点时消耗NaOH溶液的体积为______________ 。
(3)图中B点溶液中的溶质有________________ 。
(4)AlCl3溶液的浓度为______________ 。
(5)O点到B点反应的总离子方程式可表示为________________ 。

(1)图中A点表示的沉淀是
(2)反应至A点时消耗NaOH溶液的体积为
(3)图中B点溶液中的溶质有
(4)AlCl3溶液的浓度为
(5)O点到B点反应的总离子方程式可表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)3.01×1024个OH−的物质的量为________ mol,含有电子的数目为________ ,这些OH−和________ gNa+含有的电子数相同。
(2)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为______ ;
(3)实验室为确定一瓶稀盐酸的浓度,用0.1000mol/LNaOH溶液中和25.00mL该盐酸,当酸与碱恰好完全反应时,消耗NaOH溶液24.50mL。该盐酸的物质的量浓度为______ ;
(4)实验室可以用高锰酸钾和浓盐酸反应制备氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥标出电子转移的方向和数目___________ ,该反应中被氧化的元素是________ ,参加反应的氧化剂与还原剂的物质的量之比为________ ,如果该反应过程中转移了5mol电子,生成的氯气在标准状况下体积为__________ L(假设气体全部逸出)。
(2)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为
(3)实验室为确定一瓶稀盐酸的浓度,用0.1000mol/LNaOH溶液中和25.00mL该盐酸,当酸与碱恰好完全反应时,消耗NaOH溶液24.50mL。该盐酸的物质的量浓度为
(4)实验室可以用高锰酸钾和浓盐酸反应制备氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥标出电子转移的方向和数目
您最近一年使用:0次

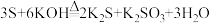 ,据此回答以下问题:
,据此回答以下问题: ,根据以上溶解性,可以用
,根据以上溶解性,可以用

