氧化还原反应是一类重要的化学反应,在生活生产中有重要应用:
(1)过氧化氢(H2O2)俗名双氧水,医疗上可作外科消毒剂。
①向含有酚酞的NaOH溶液中滴加双氧水,此时溶液由红色褪至无色,主要原因是双氧水的___ 性。
②将双氧水加入经酸化的高锰酸钾溶液中,发现溶液的紫红色消退了,此时双氧水表现出___ 性。
(2)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,氧化剂是___ 、还原剂是___ 、氧化产物是___ 、还原产物是___ 。
(3)配平下列氧化还原方程式:
① Fe+ HNO3= Fe(NO3)3+ NO↑+ H2O___ 。
② CO+ Fe2O3= Fe+ CO2___ 。
③ SO2+ Cl2+ H2O= H2SO4+ HCl___ 。
④ K2S+ HNO3= KNO3+ NO↑+ S↓+ H2O___ 。
(1)过氧化氢(H2O2)俗名双氧水,医疗上可作外科消毒剂。
①向含有酚酞的NaOH溶液中滴加双氧水,此时溶液由红色褪至无色,主要原因是双氧水的
②将双氧水加入经酸化的高锰酸钾溶液中,发现溶液的紫红色消退了,此时双氧水表现出
(2)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,氧化剂是
(3)配平下列氧化还原方程式:
① Fe+ HNO3= Fe(NO3)3+ NO↑+ H2O
② CO+ Fe2O3= Fe+ CO2
③ SO2+ Cl2+ H2O= H2SO4+ HCl
④ K2S+ HNO3= KNO3+ NO↑+ S↓+ H2O
更新时间:2020-12-26 22:52:27
|
【知识点】 氧化还原反应方程式的配平解读
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据所学知识回答问题
(1)___________ molH2O中所含有的氧原子数与1.5 molCO2的氧原子数相同。
(2)质量为9.8g的H2SO4物质的量是___________ 。
(3)1.204×1024个H2的物质的量是___________ 。
(4)配制溶液时,称量5.85gNaCl固体,配制480mL溶液,则溶液物质的量浓度是___________ mol/L。
(5)标准状况下16gH2的体积是___________ L。
(6)100mL0.2mol·L-1的Na2SO4溶液中,取出10mL该溶液,c(Na+)=___________ ,将该10mL溶液加水稀释至100mL,则c( )=
)=___________ 。
(7) 的中子数是
的中子数是___________ 。
(8)写出方程式的系数____NaClO+___NaI=____NaIO3+____NaCl___________
(1)
(2)质量为9.8g的H2SO4物质的量是
(3)1.204×1024个H2的物质的量是
(4)配制溶液时,称量5.85gNaCl固体,配制480mL溶液,则溶液物质的量浓度是
(5)标准状况下16gH2的体积是
(6)100mL0.2mol·L-1的Na2SO4溶液中,取出10mL该溶液,c(Na+)=
 )=
)=(7)
 的中子数是
的中子数是(8)写出方程式的系数____NaClO+___NaI=____NaIO3+____NaCl
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国硒含量居世界首位,硒广泛用于冶金、陶瓷、电子、太阳能等领域。工业上常将含硒废料处理得到亚硒酸(H2SeO3)进而制备单质硒。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为___________ 。
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应___________ 。
(3)基态Se原子电子占据最高能级的电子云轮廓图为___________ 形。 号的空间结构为
号的空间结构为___________ 形。
(4)关于硒单质及其化合物说法正确的是___________ (填标号)。
a.硒单质在常温下呈固态 b. 既有氧化性又有还原性
既有氧化性又有还原性
c.键角: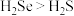 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下, 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:

 的
的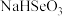 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为___________ ,计算反应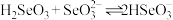 的平衡常数K=
的平衡常数K=___________ 。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应
(3)基态Se原子电子占据最高能级的电子云轮廓图为
 号的空间结构为
号的空间结构为(4)关于硒单质及其化合物说法正确的是
a.硒单质在常温下呈固态 b.
 既有氧化性又有还原性
既有氧化性又有还原性c.键角:
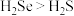 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下,
 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:
 的
的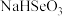 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为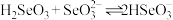 的平衡常数K=
的平衡常数K=
您最近半年使用:0次
填空题
|
适中
(0.64)
【推荐3】铁屑可用于地下水脱氮,其实验室研究步骤如下:
Ⅰ、将铁屑浸泡在0.5 mol/L盐酸中进行预处理。
Ⅱ、30 min后,用去离子水反复冲洗,至冲洗后液体的pH为中性。在N2保护下烘干备用。
Ⅲ、在蒸馏水中加入硝酸钾配制硝酸钾溶液。
Ⅳ、将酸预处理后的铁屑加入硝酸钾溶液中。
请回答:
(1)盐酸溶解Fe2O3的离子方程式是__________ 。
(2)烘干时需要在N2保护下进行的原因是__________ 。
(3)将步骤Ⅱ中冲洗后的溶液在空气中加热蒸发灼烧,最终得到的固体是_________ 。
(4)将酸性条件下,铁与NO3-反应的离子方程式补充完整:________

Ⅰ、将铁屑浸泡在0.5 mol/L盐酸中进行预处理。
Ⅱ、30 min后,用去离子水反复冲洗,至冲洗后液体的pH为中性。在N2保护下烘干备用。
Ⅲ、在蒸馏水中加入硝酸钾配制硝酸钾溶液。
Ⅳ、将酸预处理后的铁屑加入硝酸钾溶液中。
请回答:
(1)盐酸溶解Fe2O3的离子方程式是
(2)烘干时需要在N2保护下进行的原因是
(3)将步骤Ⅱ中冲洗后的溶液在空气中加热蒸发灼烧,最终得到的固体是
(4)将酸性条件下,铁与NO3-反应的离子方程式补充完整:

您最近半年使用:0次



