根据所学知识回答问题
(1)___________ molH2O中所含有的氧原子数与1.5 molCO2的氧原子数相同。
(2)质量为9.8g的H2SO4物质的量是___________ 。
(3)1.204×1024个H2的物质的量是___________ 。
(4)配制溶液时,称量5.85gNaCl固体,配制480mL溶液,则溶液物质的量浓度是___________ mol/L。
(5)标准状况下16gH2的体积是___________ L。
(6)100mL0.2mol·L-1的Na2SO4溶液中,取出10mL该溶液,c(Na+)=___________ ,将该10mL溶液加水稀释至100mL,则c( )=
)=___________ 。
(7) 的中子数是
的中子数是___________ 。
(8)写出方程式的系数____NaClO+___NaI=____NaIO3+____NaCl___________
(1)
(2)质量为9.8g的H2SO4物质的量是
(3)1.204×1024个H2的物质的量是
(4)配制溶液时,称量5.85gNaCl固体,配制480mL溶液,则溶液物质的量浓度是
(5)标准状况下16gH2的体积是
(6)100mL0.2mol·L-1的Na2SO4溶液中,取出10mL该溶液,c(Na+)=
 )=
)=(7)
 的中子数是
的中子数是(8)写出方程式的系数____NaClO+___NaI=____NaIO3+____NaCl
更新时间:2022-12-18 19:57:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.工业生产硝酸的尾气中含有氮氧化物 (假设仅为NO和
(假设仅为NO和 的混合物),影响生态环境。
的混合物),影响生态环境。
(1)氮氧化物 对环境主要影响有两点
对环境主要影响有两点___________ 、___________ 。
Ⅱ.工业上可用氨催化吸收法处理 ,反应原理为:
,反应原理为: 某化学兴趣小组模拟该处理过程的实验装置如图:
某化学兴趣小组模拟该处理过程的实验装置如图:

(2)装置A中发生反应的化学方程式为___________ 。
(3)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是___________ 。
(4)反应 可用于处理
可用于处理 。当转移3.6mol电子时,消耗
。当转移3.6mol电子时,消耗 的物质的量为
的物质的量为___________ mol。
Ⅲ.工业上也常用NaOH溶液吸收法处理 :
:


(5)2240mL(标准状况)NO和 的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是 ___________ 。
 (假设仅为NO和
(假设仅为NO和 的混合物),影响生态环境。
的混合物),影响生态环境。(1)氮氧化物
 对环境主要影响有两点
对环境主要影响有两点Ⅱ.工业上可用氨催化吸收法处理
 ,反应原理为:
,反应原理为: 某化学兴趣小组模拟该处理过程的实验装置如图:
某化学兴趣小组模拟该处理过程的实验装置如图:
(2)装置A中发生反应的化学方程式为
(3)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是
(4)反应
 可用于处理
可用于处理 。当转移3.6mol电子时,消耗
。当转移3.6mol电子时,消耗 的物质的量为
的物质的量为Ⅲ.工业上也常用NaOH溶液吸收法处理
 :
:

(5)2240mL(标准状况)NO和
 的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)等质量的 和
和 ,
, 与
与 的物质的量之比是
的物质的量之比是_______ ,所含氧原子个数之比是_______ ;
(2)等质量的下列四种气体 、
、 、
、 、
、 ,在相同温度和压强条件下,体积最大的是
,在相同温度和压强条件下,体积最大的是_______ ;
(3)标准状况下,体积为 的
的 所含质子数目为
所含质子数目为_______ ;
(4)设 为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为
为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为_______ 
(1)等质量的
 和
和 ,
, 与
与 的物质的量之比是
的物质的量之比是(2)等质量的下列四种气体
 、
、 、
、 、
、 ,在相同温度和压强条件下,体积最大的是
,在相同温度和压强条件下,体积最大的是(3)标准状况下,体积为
 的
的 所含质子数目为
所含质子数目为(4)设
 为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为
为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)3.4克NH3分子中所含氢原子数与_________ 个水分子中所含氢原子数相等。
(2)7克CO与8克O2组成的混合气体,在标准状况下的体积为____ ,1mol这种混合气体的质量是___
(3)已知O2和CO2的混合气体,标准状况下体积为11.2L,质量为18g,则混合气体中O2和CO2的物质的量之比为_____
(4)38g某二价金属氯化物(ACl2)中含有0.8molCl-,则ACl2的摩尔质量是____ ,A的相对原子质量是____
(5)现有下列三种气体:①32g CH4;②约含有6.02×1023个HCl分子的氯化氢气体;③标准状况下33.6LO2.请按物理量由小到大的顺序排列:
a.质量___ (填序号,下同);
b.分子数目___
c.相同状况下气体的体积___ .
(2)7克CO与8克O2组成的混合气体,在标准状况下的体积为
(3)已知O2和CO2的混合气体,标准状况下体积为11.2L,质量为18g,则混合气体中O2和CO2的物质的量之比为
(4)38g某二价金属氯化物(ACl2)中含有0.8molCl-,则ACl2的摩尔质量是
(5)现有下列三种气体:①32g CH4;②约含有6.02×1023个HCl分子的氯化氢气体;③标准状况下33.6LO2.请按物理量由小到大的顺序排列:
a.质量
b.分子数目
c.相同状况下气体的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】定量计算在科学研究中有重要作用。
(1)已知 个X气体分子的质量为32g,则X气体的摩尔质量为
个X气体分子的质量为32g,则X气体的摩尔质量为___________ 。
(2)相同物质的量的H2和CO2,在同温同压下的体积之比___________ ,含分子个数之比为___________ ,所含原子个数的之比为___________ ,质量之比___________ 。
(3)为恰好完全中和 溶液,需要加入
溶液,需要加入___________  稀硫酸。(已知:
稀硫酸。(已知: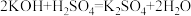 )
)
(1)已知
 个X气体分子的质量为32g,则X气体的摩尔质量为
个X气体分子的质量为32g,则X气体的摩尔质量为(2)相同物质的量的H2和CO2,在同温同压下的体积之比
(3)为恰好完全中和
 溶液,需要加入
溶液,需要加入 稀硫酸。(已知:
稀硫酸。(已知: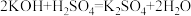 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:①标准状况下,1体积水中最多能溶解500体积的HCl;②饱和NaCl溶液的浓度约为5.00mol/L 。将448L(标准状况下)HCl气体溶于1L水中,所得溶液A的密度为1.20g·cm-3,则溶液A中HCl的物质的量浓度为__________ 。(本题计算结果均取三位有效数字)
(1)若使1L饱和NaCl溶液中的Cl-浓度与溶液A中的Cl-浓度相等,则在1L饱和NaCl溶液中还应溶解__________ L标准状况下的HCl气体(溶液体积变化忽略不计)。
(2)若将10.0mL溶液A稀释成500mL溶液B,则溶液B中HCl的物质的量浓度为__________ 。
(3)在溶液B的配制过程中,使用前必须检查是否漏液的仪器是__________ 。
(1)若使1L饱和NaCl溶液中的Cl-浓度与溶液A中的Cl-浓度相等,则在1L饱和NaCl溶液中还应溶解
(2)若将10.0mL溶液A稀释成500mL溶液B,则溶液B中HCl的物质的量浓度为
(3)在溶液B的配制过程中,使用前必须检查是否漏液的仪器是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列相关问题:
(1)以下物质:① 晶体;②
晶体;② 固体;③NaOH溶液;④熔融NaCl;⑤蔗糖;⑥液氯;⑦
固体;③NaOH溶液;④熔融NaCl;⑤蔗糖;⑥液氯;⑦ 。能导电的是
。能导电的是_______ (填序号,下同);属于电解质的是_______ ;属于碱性氧化物的是_______ 。
(2)实验室用碳酸钙与盐酸反应制取 气体,反应的离子方程式是
气体,反应的离子方程式是_______ 。常用澄清石灰水检验 气体,反应的离子方程式是
气体,反应的离子方程式是_______ 。
(3)某无土栽培用的营养液,要求KCl、 和
和 三种原料的物质的量之比为1∶4∶8。
三种原料的物质的量之比为1∶4∶8。
①配制该营养液后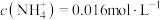 ,溶液中
,溶液中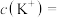
_______  。
。
②若采用 和KCl来配制该营养液,则KCl和
和KCl来配制该营养液,则KCl和 物质的量之比为
物质的量之比为_______ 。
(1)以下物质:①
 晶体;②
晶体;② 固体;③NaOH溶液;④熔融NaCl;⑤蔗糖;⑥液氯;⑦
固体;③NaOH溶液;④熔融NaCl;⑤蔗糖;⑥液氯;⑦ 。能导电的是
。能导电的是(2)实验室用碳酸钙与盐酸反应制取
 气体,反应的离子方程式是
气体,反应的离子方程式是 气体,反应的离子方程式是
气体,反应的离子方程式是(3)某无土栽培用的营养液,要求KCl、
 和
和 三种原料的物质的量之比为1∶4∶8。
三种原料的物质的量之比为1∶4∶8。①配制该营养液后
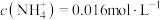 ,溶液中
,溶液中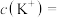
 。
。②若采用
 和KCl来配制该营养液,则KCl和
和KCl来配制该营养液,则KCl和 物质的量之比为
物质的量之比为
您最近一年使用:0次
【推荐1】三氧化二铬(Cr2O3)可用作着色剂、分析试剂、催化剂等。一种利用铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3、SiO2等杂质)清洁生产Cr2O3的工艺流程如下:

已知铬酸酐(CrO3)常用作氧化剂,写出“氧化酸浸”时FeO·Cr2O3反应的化学方程式是_______ 。

已知铬酸酐(CrO3)常用作氧化剂,写出“氧化酸浸”时FeO·Cr2O3反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列物质:①Na2CO3·10H2O晶体,②石墨,③无水乙醇,④小苏打,⑤熔融NaHSO4,⑥醋(乙)酸,⑦液氨,⑧98%浓硫酸,⑨Ba(OH)2固体,⑩Fe(OH)3红褐色胶体
(1)按物质的分类方法,填写表格的空白处(填序号):
(2)配平并用双线桥法表示下列反应,标出转移电子的个数_______ 。
_______NaClO3+_______H2O2+_______H2SO4—_______ClO2↑+_______O2↑+_______Na2SO4+_______H2O
(3)补缺项配平并用单线桥法表示下列反应,标出转移电子的个数_______ 。
_______Cr2O +_______SO
+_______SO +_______——_______Cr3++_______SO
+_______——_______Cr3++_______SO +_______
+_______
(1)按物质的分类方法,填写表格的空白处(填序号):
| 分类标准 | 能导电的物质 | 电解质 | 非电解质 | 强电解质 | 弱电解质 |
| 属于该类的物质 |
(2)配平并用双线桥法表示下列反应,标出转移电子的个数
_______NaClO3+_______H2O2+_______H2SO4—_______ClO2↑+_______O2↑+_______Na2SO4+_______H2O
(3)补缺项配平并用单线桥法表示下列反应,标出转移电子的个数
_______Cr2O
 +_______SO
+_______SO +_______——_______Cr3++_______SO
+_______——_______Cr3++_______SO +_______
+_______
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应在物质制备、能量转化方面有重要的应用。
(1)用单线桥法表示下列反应的电子转移方向和数目。___________

(2)反应 常用于测定溶液中I2的含量。反应的还原剂是
常用于测定溶液中I2的含量。反应的还原剂是___________ ,每生成1moLNaI,反应转移电子___________ mol。
(3)反应 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中氧化剂与还原剂的物质的量之比为___________ 。
(4)高铁酸钾(K2FeO4)可作为高效、多功能水处理剂。用FeCl3与KClO在强碱条件下反应可制取高铁酸钾,完成反应的离子方程式。___________
2Fe3++______ClO-+______OH-=______FeO +3Cl-+______
+3Cl-+______
(1)用单线桥法表示下列反应的电子转移方向和数目。

(2)反应
 常用于测定溶液中I2的含量。反应的还原剂是
常用于测定溶液中I2的含量。反应的还原剂是(3)反应 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中氧化剂与还原剂的物质的量之比为
(4)高铁酸钾(K2FeO4)可作为高效、多功能水处理剂。用FeCl3与KClO在强碱条件下反应可制取高铁酸钾,完成反应的离子方程式。
2Fe3++______ClO-+______OH-=______FeO
 +3Cl-+______
+3Cl-+______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题。
(1)在第三周期元素中,化学性质最不活泼的是_______ ,可用于制半导体材料的元素是_______ ,最高价氧化物的水化物碱性最强的是_______ ,酸性最强的是_______ ,具有两性的是_______ (以上均用化学式填空)。
(2)在C、N、O、F中,原子半径最大的是_______ 。
(3)第32号元素在元素周期表中的位置为_______ 。
(4)由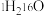 与
与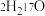 所代表的物质中,共有
所代表的物质中,共有_______ 种元素,_______ 种原子, 、
、 的关系是
的关系是_______ 。
(5)写出钠、铝最高价氧化物的水化物之间反应的化学方程式:_______ 。
(1)在第三周期元素中,化学性质最不活泼的是
(2)在C、N、O、F中,原子半径最大的是
(3)第32号元素在元素周期表中的位置为
(4)由
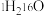 与
与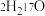 所代表的物质中,共有
所代表的物质中,共有 、
、 的关系是
的关系是(5)写出钠、铝最高价氧化物的水化物之间反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.(1)写出表示含有8个质子、10个中子的原子的化学符号_______ 。
(2)元素周期表中,所含元素超过18种的周期是_______ 。
Ⅱ.有:① 168O、178O、188O ②H2O、D2O ③石墨、金刚石④H、D、T 四组微粒或物质,回答下列问题:
(1)互为同位素的是_______ ;
(2)互为同素异形体的是_______ ;
(3)由①和④中微粒能结合成含三个原子的化合物,这些化合物中分子量最大的是_______ (填化学式)。
(2)元素周期表中,所含元素超过18种的周期是
Ⅱ.有:① 168O、178O、188O ②H2O、D2O ③石墨、金刚石④H、D、T 四组微粒或物质,回答下列问题:
(1)互为同位素的是
(2)互为同素异形体的是
(3)由①和④中微粒能结合成含三个原子的化合物,这些化合物中分子量最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】我国展开“嫦娥探月”工程,向月球发起探索。2020年嫦娥五号一次带回1700多克月壤样本。研究表明,月球上有丰富的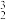 He资源,可开发用作未来的新型能源。
He资源,可开发用作未来的新型能源。
(1)α粒子是带有2个单位正电荷、质量数为4的氦离子,由此推断一个α粒子含有_____ 个电子,它的结构示意图为______ 。
(2)利用核聚变发电,3He是最安全的最清洁的能源,下列说法正确的是______ 。
(3)同温同压下,下列关于氦气和氧气的叙述中,正确的是______ 。
①氦气和氧气所含的分子数相同
②氦分子间的平均距离和氧分子间的平均距离几乎是相等的
③氦分子与氧分子的大小几乎相同
④氦分子和氧分子本身大小对于气体体积影响可以忽略不计
⑤氦气与氧气的密度之比等于32:4
(4)16克氧气含有n个O2分子,则阿伏加德罗常数可表示为______ 。
(5)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,该混合气体的平均分子量为______ ,其中氧气和氦气的分子数之比是_____ 。
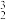 He资源,可开发用作未来的新型能源。
He资源,可开发用作未来的新型能源。(1)α粒子是带有2个单位正电荷、质量数为4的氦离子,由此推断一个α粒子含有
(2)利用核聚变发电,3He是最安全的最清洁的能源,下列说法正确的是
| A.3He、4He的化学性质基本相同 | B.3He、4He具有相同的电子数 |
| C.3He核聚变是化学变化 | D.3He液化是化学变化 |
①氦气和氧气所含的分子数相同
②氦分子间的平均距离和氧分子间的平均距离几乎是相等的
③氦分子与氧分子的大小几乎相同
④氦分子和氧分子本身大小对于气体体积影响可以忽略不计
⑤氦气与氧气的密度之比等于32:4
| A.①② | B.②④ | C.③⑤ | D.②③ |
| A.2n | B. n n | C.16n | D. n n |
您最近一年使用:0次



