应用电化学原理,回答下列问题:
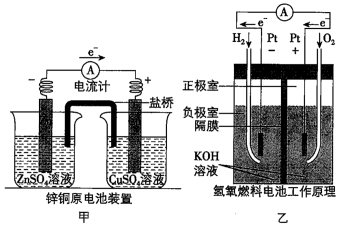
(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是:K+移向_______ ,Cl-移向_______ 。一段时间后,当电路中通过电子为0.5mol时,锌电极质量_______ (填“增加”或“减少”,下同),铜电极质量_______ 了_______ g。
(2)乙中正极反应式为_______ ;若将H2换成CH4,则负极反应式为_______ 。
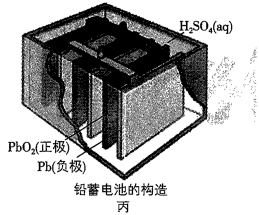
(3)丙中铅蓄电池放电时正极的电极反应式为:_______ ,放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池 _______ 极相连接。


(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是:K+移向
(2)乙中正极反应式为
(3)丙中铅蓄电池放电时正极的电极反应式为:
更新时间:2020-12-20 21:48:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
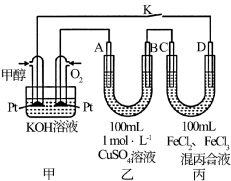
(1)甲中负极的电极反应式为___ 。
(2)乙中A极析出的气体在标准状况下的体积为___ 。

(1)甲中负极的电极反应式为
(2)乙中A极析出的气体在标准状况下的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题:
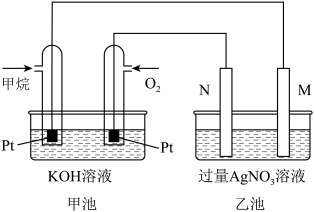
(1)M电极的材料是________ ,其电极反应式为:________ N的电极名称是________ ,电极反应式为:________
(2)通入甲烷的铂电极的电极反应式为________ .
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为________ L(标准状况下)。

(1)M电极的材料是
(2)通入甲烷的铂电极的电极反应式为
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电池和电解池在日常生活中有着广泛的应用。根据所学知识完成下列题目。
Ⅰ.电化学装置如图所示
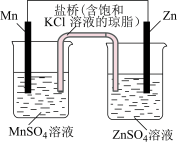
(1)已知金属活泼性: 。若如图装置中负极金属的消耗速率为
。若如图装置中负极金属的消耗速率为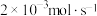 ,则盐桥中
,则盐桥中 流向
流向___________ (填“ ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为___________  。
。
Ⅱ.电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
(2)①电解饱和食盐水的总反应的离子方程式是___________ 。
②在b口加入的物质为___________ (写化学式)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,氨水式燃料电池工作原理如图所示:
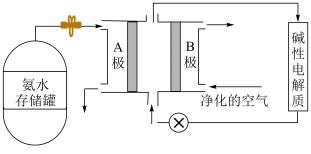
①氨气燃料电池的反应原理是氨气与氧气反应生成一种常见的无毒气体和水,该电池负极上的电极反应式是___________ 。
②“净化的空气”是指在进入电池装置前除去___________ (填化学式)的气体。
Ⅲ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
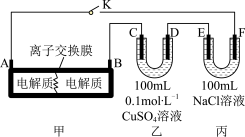
(4)装置甲中A电极为电池的___________ 极,B电极的电极反应式为___________ 。
(5)装置乙中D电极产生的气体是___________ (写化学式),体积为___________  (标准状况)。
(标准状况)。
(6)若将装置丙中的 溶液改换成
溶液改换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是___________ 。

Ⅰ.电化学装置如图所示

(1)已知金属活泼性:
 。若如图装置中负极金属的消耗速率为
。若如图装置中负极金属的消耗速率为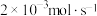 ,则盐桥中
,则盐桥中 流向
流向 ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为 。
。Ⅱ.电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

(2)①电解饱和食盐水的总反应的离子方程式是
②在b口加入的物质为
(3)氨气是一种富氢燃料,可以直接用于燃料电池,氨水式燃料电池工作原理如图所示:

①氨气燃料电池的反应原理是氨气与氧气反应生成一种常见的无毒气体和水,该电池负极上的电极反应式是
②“净化的空气”是指在进入电池装置前除去
Ⅲ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为
 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
(4)装置甲中A电极为电池的
(5)装置乙中D电极产生的气体是
 (标准状况)。
(标准状况)。(6)若将装置丙中的
 溶液改换成
溶液改换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池反应一般是氧化还原反应,但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子,电子通过外电路输送到正极上,氧化剂在正极上得电子,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化。
(1)化学反应 ,
,_______ (填“能”或“不能”)通过原电池原理设计成化学电源,理由是_______ 。
(2)甲醇燃料电池结构简单、能量转化率高,工作原理如图所示。加入的a是_______ (填名称),该电极的名称是_______ (填“正”或“负”)极,其电极反应式为_______ 。
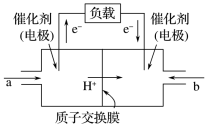
(3)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图所示。

①该电池的电流方向:由_______ (填“左”或“右”,下同)侧电极经过负载流向_______ 侧电极。
②当1mol 参与电极反应时,从
参与电极反应时,从_______ (填“左”或“右”,下同)侧穿过质子交换膜进入_______ 侧的 数目为
数目为_______  。
。
(1)化学反应
 ,
,(2)甲醇燃料电池结构简单、能量转化率高,工作原理如图所示。加入的a是

(3)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图所示。

①该电池的电流方向:由
②当1mol
 参与电极反应时,从
参与电极反应时,从 数目为
数目为 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示三套实验装置,分别回答下列问题。
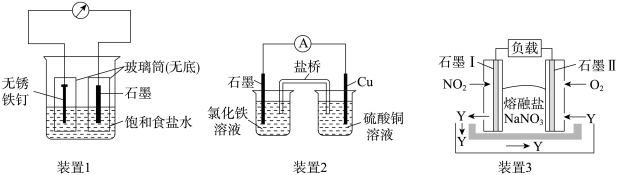
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被___________ (填“氧化”或“还原”);向插入石墨的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应式为___________ 。
(2)装置2中的石墨作___________ (填“正”或“负”)极,该装置发生的总反应的离子方程式为___________ 。
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为___________ (填化学式);石墨II极的电极反应式为:___________ ;当石墨I极中有1molNO2参加反应时,石墨II极消耗的O2的体积___________ (标准状况下)。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被
(2)装置2中的石墨作
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+ O2(g)
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是_____________ (填字母)。
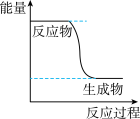
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C=O键断裂,则反应达最大限度
(2)某温度下,将5 mol CH3OH和2 mol O2充入2 L的密闭容器中,经过4 min反应达到平衡,测得c(O2)=0.2 mol·L-1,4 min内平均反应速率v(H2)=_______ ,则CH3OH的转化率为_______ 。
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为_________ ,下列说法正确的是_______ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4 g CH3OH转移1.2 mol电子
(4)已知断开1 mol H—H键吸收的能量为436 kJ,形成1 mol H—N键放出的能量为391 kJ,根据化学方程式N2+3H2 2NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N键需吸收的能量是
2NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N键需吸收的能量是______________ kJ。
Ⅱ.将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15 mol·L-1·min-1。
xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15 mol·L-1·min-1。
(5)x=________ 。
(6)A在5 min末的浓度是________ 。
(7)此时容器内的压强与开始时之比为__________________ 。
(1)已知CH3OH(g)+
 O2(g)
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C=O键断裂,则反应达最大限度
(2)某温度下,将5 mol CH3OH和2 mol O2充入2 L的密闭容器中,经过4 min反应达到平衡,测得c(O2)=0.2 mol·L-1,4 min内平均反应速率v(H2)=
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4 g CH3OH转移1.2 mol电子
(4)已知断开1 mol H—H键吸收的能量为436 kJ,形成1 mol H—N键放出的能量为391 kJ,根据化学方程式N2+3H2
 2NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N键需吸收的能量是
2NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N键需吸收的能量是Ⅱ.将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15 mol·L-1·min-1。
xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15 mol·L-1·min-1。(5)x=
(6)A在5 min末的浓度是
(7)此时容器内的压强与开始时之比为
您最近半年使用:0次



