铁是人体内必需的微量元素,铁的化学性质较活泼,能与很多物质发生反应。完成下列填空:
(1)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(2)写出铁与水蒸气反应的化学方程式_______ 。
(3)写出铁与氯气恰好完全反应的化学方程式_______ 。将产物溶于水,能得到_______ 颜色的溶液,其产物中的阳离子可以用_______ 溶液检验,写出其离子方程式_______ 。
(1)常温下由于浓硫酸能使铁
(2)写出铁与水蒸气反应的化学方程式
(3)写出铁与氯气恰好完全反应的化学方程式
更新时间:2020-12-29 08:42:36
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求回答下列问题。
(1)加碘食盐中含有碘酸钾(KIO3),其中碘的化合价为____ 。
(2)写铁在氧气中燃烧的现象:_____ 。
(3)写出饱和碳酸钠溶液中通入足CO2出现浑浊的离于方程式:_____ 。
(4)用一个化学方程式解释向碳酸钠溶液中滴加少量稀盐酸无明显气泡生成的原因:____ 。
(1)加碘食盐中含有碘酸钾(KIO3),其中碘的化合价为
(2)写铁在氧气中燃烧的现象:
(3)写出饱和碳酸钠溶液中通入足CO2出现浑浊的离于方程式:
(4)用一个化学方程式解释向碳酸钠溶液中滴加少量稀盐酸无明显气泡生成的原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)将金属钠放入硫酸铜溶液中会产生蓝色沉淀,反应的化学方程式 ________________
(2)过氧化钠与水反应的化学方程式:_________
(3)铁在氯气中燃烧反应的化学方程式:____________
(4)氯气和水反应的化学方程式:_____________
(2)过氧化钠与水反应的化学方程式:
(3)铁在氯气中燃烧反应的化学方程式:
(4)氯气和水反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在常温下,Fe与水并不发生反应,但在高温下,Fe与水蒸气可发生反应。应用如图所示装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下Fe与水蒸气反应的实验。
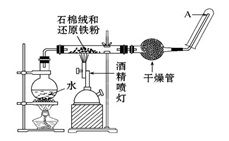
请回答该实验中的问题。
(1)写出Fe与水蒸气反应的化学方程式:____________________________________ 。
(2)实验前必须对整套装置进行的操作是__________________________ 。
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_________________________ 。
(4)干燥管中盛装的物质可以是________________ ,作用是_______________ 。
(5)试管中收集到的气体,若要在A处玻璃管口处点燃该气体,则必须对该气体进行__________ ,目的是:____________ 。

请回答该实验中的问题。
(1)写出Fe与水蒸气反应的化学方程式:
(2)实验前必须对整套装置进行的操作是
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是
(4)干燥管中盛装的物质可以是
(5)试管中收集到的气体,若要在A处玻璃管口处点燃该气体,则必须对该气体进行
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求回答下列问题
(1)氧化钠的化学式___________ ;
(2)制漂白液(离子方程式表示)原理:___________ ;
(3)小苏打用于治疗胃酸过多的离子方程式___________ ;
(4)氢氧化钠加入盐酸的离子方程式___________ ;
(5)铁和水蒸气反应的化学方程式___________ 。
(1)氧化钠的化学式
(2)制漂白液(离子方程式表示)原理:
(3)小苏打用于治疗胃酸过多的离子方程式
(4)氢氧化钠加入盐酸的离子方程式
(5)铁和水蒸气反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】从物质类别和化合价两个角度总结、预测物质的性质是学习化学的重要方法之一。参考铁元素的“价类二维图”,回答下列问题。

Ⅰ相同类别不同价态的物质变化
(1)高铁酸钾是一种常见的水处理剂,可以同时起到杀菌消毒的作用和净水的作用,利用离子方程式表示其原理为______________ ;处理后的废水,调节pH至碱性,通入氯气,可实现水处理剂的循环利用,通入1molCl2理论上可以制备_____ gK2FeO4。
(2)铁氰化钾(K3[Fe(CN)6]),常用于配制铁锈指示剂检验金属的氧化程度,检验Fe2+的现象是___________________ ;工业上可用氯气氧化亚铁氰化钾(K4[Fe(CN)6])制备,离子方程式为______________ 。
Ⅱ不同类别不同价态的物质变化
(3)铁与水蒸气在高温环境下生成黑色固体的方程式:_______________ ;已知黑色固体可以被磁铁吸引,请设计实验,简述如何确定黑色固体的含量________ 。

Ⅰ相同类别不同价态的物质变化
(1)高铁酸钾是一种常见的水处理剂,可以同时起到杀菌消毒的作用和净水的作用,利用离子方程式表示其原理为
(2)铁氰化钾(K3[Fe(CN)6]),常用于配制铁锈指示剂检验金属的氧化程度,检验Fe2+的现象是
Ⅱ不同类别不同价态的物质变化
(3)铁与水蒸气在高温环境下生成黑色固体的方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料 。其主要实验流程如下
。其主要实验流程如下

还原。向“酸浸”后的滤液中加入过量铁粉,使 完全转化为
完全转化为 。“还原”过程中除生成
。“还原”过程中除生成 外,还会生成
外,还会生成___________ (填化学式):检验 是否还原完全的实验操作是
是否还原完全的实验操作是___________ 。
 。其主要实验流程如下
。其主要实验流程如下
还原。向“酸浸”后的滤液中加入过量铁粉,使
 完全转化为
完全转化为 。“还原”过程中除生成
。“还原”过程中除生成 外,还会生成
外,还会生成 是否还原完全的实验操作是
是否还原完全的实验操作是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】钠和铁是两种重要的金属。请回答:
(1)切开的金属钠暴露在空气中,最先发生的化学方程式是____ ,将钠投入水中后,钠熔化成一个小球,根据这一现象得出金属钠的物理性质是_______ ,钠与水反应的离子方程式为____ 。
(2)Fe与Cl2在一定条件下反应,所得产物的化学式是____ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:若向其中一支试管中滴加KSCN溶液,则溶液变成____ 色。向另一支试管中滴加NaOH溶液,反应的离子方程式是____ 。
(1)切开的金属钠暴露在空气中,最先发生的化学方程式是
(2)Fe与Cl2在一定条件下反应,所得产物的化学式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】为了探究AgNO3的氧化性,某化学兴趣小组设计了如下实验。
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验,可选用试剂:KSCN溶液、K3[Fe(CN)6]溶液、氯水。
请完成如表:
【实验结论】Fe的氧化产物为Fe2+和Fe3+。
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验,可选用试剂:KSCN溶液、K3[Fe(CN)6]溶液、氯水。
请完成如表:
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 存在Fe3+ | |
| 取少量除尽Ag+后的溶液于试管中,加入 | 存在Fe2+ |
【实验结论】Fe的氧化产物为Fe2+和Fe3+。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】利用下列实验研究铁与浓硫酸的反应(夹持装置已略去,气密性已检验)。
(1)实验Ⅰ中体现了浓硫酸的_______ (填“氧化性”或“还原性”)。
(2)下列装置中,能用于实验Ⅱ中尾气吸收的是_______ (填序号)。
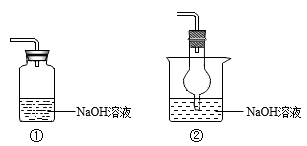
(3)实验Ⅱ中,能够证明生成了SO2的证据是_______ 。
(4)实验Ⅰ和Ⅱ中,实验现象不同的原因是_______ 。
| 实验Ⅰ | 实验Ⅱ |
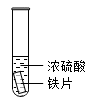 | 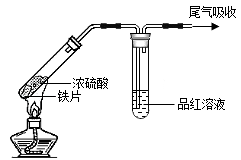 |
| 铁片表面迅速变暗,之后无明显变化 | 加热后产生大量气体,品红溶液褪色 |
(2)下列装置中,能用于实验Ⅱ中尾气吸收的是

(3)实验Ⅱ中,能够证明生成了SO2的证据是
(4)实验Ⅰ和Ⅱ中,实验现象不同的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是_______ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是_______ 。
(3)欲使3 mol VO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少_______ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是_______ (用化学方程式表示)。
(5)下列变化为化学变化的是_______ (填标号)。
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3 mol VO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硝酸的化学性质
(1)酸的通性
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:_________________________ 。
②硝酸和氧化钠反应:_________________________ 。
③硝酸和碳酸钙反应:_________________________ 。
(2)不稳定性:见光或受热易分解,化学方程式为_________________________________ 。
长期存放的浓硝酸呈黄色是因为其分解生成的____ 溶于硝酸中,实验室常将浓硝酸保存在____ 试剂瓶中,并放在____ 处。
(3)强氧化性
①和金属(Cu)反应的实验探究
写出上述反应的化学方程式:_________ ;_________ 。
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而____ ,保护内部金属不再与酸反应,所以可以用____ 制容器或____ 制容器盛放浓硝酸。加热时,铁、铝可以与浓硝酸反应。
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:____ 。
(1)酸的通性
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:
②硝酸和氧化钠反应:
③硝酸和碳酸钙反应:
(2)不稳定性:见光或受热易分解,化学方程式为
长期存放的浓硝酸呈黄色是因为其分解生成的
(3)强氧化性
①和金属(Cu)反应的实验探究
| 实验操作 |  两支试管中分别加入2 mL浓硝酸和稀硝酸 |
| 实验现象 | 浓硝酸反应比较 |
| 实验结论 | 硝酸无论浓、稀都有 |
写出上述反应的化学方程式:
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:
您最近一年使用:0次



