根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是_______ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是_______ 。
(3)欲使3 mol VO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少_______ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是_______ (用化学方程式表示)。
(5)下列变化为化学变化的是_______ (填标号)。
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3 mol VO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
更新时间:2021-03-10 10:35:57
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有下列八种物质:①铝 ② 溶液 ③蔗糖固体 ④稀硫酸 ⑤熔融的
溶液 ③蔗糖固体 ④稀硫酸 ⑤熔融的 ⑥
⑥ 饱和溶液 ⑦
饱和溶液 ⑦ ⑧新制备的氢氧化铁胶体分散系
⑧新制备的氢氧化铁胶体分散系
(1)上述物质属于非电解质的有_________ (填序号)。
(2)上述物质能导电且属于电解质的有_________ (填序号)。
(3)若将⑥滴入下列物质中,能形成⑧的是_________ (填字母代号)。
A. 浓溶液 B.
浓溶液 B. 浓溶液 C.冷水 D.沸水
浓溶液 C.冷水 D.沸水
(4)可利用哪种效应鉴别⑥和⑧:______________________ 。
(5)⑦和足量②反应的离子方程式为______________________ 。
(6)①与⑤的水溶液反应的离子方程式为______________________ 。
 溶液 ③蔗糖固体 ④稀硫酸 ⑤熔融的
溶液 ③蔗糖固体 ④稀硫酸 ⑤熔融的 ⑥
⑥ 饱和溶液 ⑦
饱和溶液 ⑦ ⑧新制备的氢氧化铁胶体分散系
⑧新制备的氢氧化铁胶体分散系(1)上述物质属于非电解质的有
(2)上述物质能导电且属于电解质的有
(3)若将⑥滴入下列物质中,能形成⑧的是
A.
 浓溶液 B.
浓溶液 B. 浓溶液 C.冷水 D.沸水
浓溶液 C.冷水 D.沸水(4)可利用哪种效应鉴别⑥和⑧:
(5)⑦和足量②反应的离子方程式为
(6)①与⑤的水溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氮氧化物种类很多,造成大气污染的主要是一氧化氮(NO)和二氧化氮(NO2)。
(1)汽车尾气中氮氧化物和二氧化硫在形成雾霾时,能观察到丁达尔现象。雾霾小颗粒的直径范围为___________ nm。
(2)SCR技术可有效降低柴油发动机的氮氧化物排放,其原理为:

尿素[CO(NH2)2]水溶液热分解为NH3和CO2.写出SCR催化反应器中NH3还原NO2的化学方程式:___________ 。
(1)汽车尾气中氮氧化物和二氧化硫在形成雾霾时,能观察到丁达尔现象。雾霾小颗粒的直径范围为
(2)SCR技术可有效降低柴油发动机的氮氧化物排放,其原理为:

尿素[CO(NH2)2]水溶液热分解为NH3和CO2.写出SCR催化反应器中NH3还原NO2的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在抗击新冠肺炎疫情的战役中,病毒在不断发生变异,现有疫苗对变异病毒的有效性有待进一步的验证,因此民众的防疫意识不能松懈。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过气溶胶传播。气溶胶属于___________ (填“胶体”或“溶液”);常利用___________ 区分溶液和胶体。
(2)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。请写出实验室制备Cl2的化学方程式___________ 。
(3)2022年10月31日15时37分,搭载空间站梦天实验舱的长征五号B遥四运载火箭在文昌航天发射场成功发射,将梦天实验舱顺利送入轨道。长征系列运载火箭的燃料之一是肼(N2H4)。回答下列问题:
①肼的摩尔质量是___________ 。
②16g肼中含有氮原子的数目为___________ 。
③l6g某物质中含有的分子数为3.01×1023,则该物质的摩尔质量为___________ 。
④在N2H4+O2=N2+2H2O(g)反应中,_____ 是还原剂,1mol还原剂在反应中失去______ mol电子。
⑤标准状况下,等质量的氧气与氮气的体积之比为___________ 。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过气溶胶传播。气溶胶属于
(2)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。请写出实验室制备Cl2的化学方程式
(3)2022年10月31日15时37分,搭载空间站梦天实验舱的长征五号B遥四运载火箭在文昌航天发射场成功发射,将梦天实验舱顺利送入轨道。长征系列运载火箭的燃料之一是肼(N2H4)。回答下列问题:
①肼的摩尔质量是
②16g肼中含有氮原子的数目为
③l6g某物质中含有的分子数为3.01×1023,则该物质的摩尔质量为
④在N2H4+O2=N2+2H2O(g)反应中,
⑤标准状况下,等质量的氧气与氮气的体积之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)氧化剂是___________ ,还原剂是___________ 。
(2)氧化剂与氧化产物的质量比为___________ 。
(3)该反应中发生还原反应的过程表示为Cl2+2e-=2Cl-,则发生氧化反应的过程可表示为___________ 。
(1)氧化剂是
(2)氧化剂与氧化产物的质量比为
(3)该反应中发生还原反应的过程表示为Cl2+2e-=2Cl-,则发生氧化反应的过程可表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2—NO+H2O(未配平)作分析,该反应中,_______ 是还原剂,_______ 还原产物,被还原的物质是_______ 。
(2)在一定条件下,反应2NH3+3CuO 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______(填序号)。
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______(填序号)。
(1)对反应NH3+O2—NO+H2O(未配平)作分析,该反应中,
(2)在一定条件下,反应2NH3+3CuO
 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______(填序号)。
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______(填序号)。| A.该反应是置换反应 |
| B.反应中NH3被氧化为N2 |
| C.在反应中体现了金属铜的还原性 |
| D.在反应中每生成1 mol H2O转移1 mol电子 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在酸性介质中,往MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:2Mn2+ + 5S2O82- + 8H20=2MnO4- + 10SO42- + 16H+。
(1)用单线桥表示上述方程式电子转移方向和数目:____________ 。
(2)该反应中还原剂为:____________________________ 。
(3)该反应常用于检验Mn2+的存在,其现象是:________________________________ 。
(4)若反应中有0.1mol的还原剂参加反应,则转移的电子数目为__________ NA,消耗氧化剂的物质的量为____________ mol。
(1)用单线桥表示上述方程式电子转移方向和数目:
(2)该反应中还原剂为:
(3)该反应常用于检验Mn2+的存在,其现象是:
(4)若反应中有0.1mol的还原剂参加反应,则转移的电子数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中 | ②反应的化学方程式为 |
| 将注射器活塞退回原处并同定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝 聚 |
| 打开K2 | ③ | ④ |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请写出下列反应的化学方程式:
(1)氨气的催化氧化___________ 。
(2)氯化铁溶液制作铜制印刷电路板___________ 。
(3)铜与浓硝酸反应___________ 。
(4)铝与二氧化锰反应冶炼金属锰___________ 。
(1)氨气的催化氧化
(2)氯化铁溶液制作铜制印刷电路板
(3)铜与浓硝酸反应
(4)铝与二氧化锰反应冶炼金属锰
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOX还原成N2,某同学在实验室中,对NH3与NO2反应进行了探究,回答下列问题:
(1)写出NH3和NO2生成N2的化学方程式_______ ,该反应中氧化剂和还原剂的物质的量之比_______ 。生成1molN2转移的电子数为_______ NA.被氧化的物质物质的量为_______ mol
(2)某同学认为铜和浓硝酸在常温下可制得NO2,由此可推测出铁和浓硝酸在常温下也能制得NO2,他的推测正确吗?_______ (“正确”或“不正确”),请说明原因_______ 。
(1)写出NH3和NO2生成N2的化学方程式
(2)某同学认为铜和浓硝酸在常温下可制得NO2,由此可推测出铁和浓硝酸在常温下也能制得NO2,他的推测正确吗?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】根据所学知识,回答下列问题:
(1)《本草纲目》对白酒(俗称烧酒)的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是___ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是___ 。
(3)欲使3molVO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少___ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是___ (用化学方程式表示)。
(5)下列变化为化学变化的是___ (填标号)。
A.CaCl2的潮解
B.钠的焰色反应
C.常温下,Fe遇浓硫酸钝化
(1)《本草纲目》对白酒(俗称烧酒)的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3molVO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解
B.钠的焰色反应
C.常温下,Fe遇浓硫酸钝化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】利用下列实验研究铁与浓硫酸的反应(夹持装置已略去,气密性已检验)。
(1)实验Ⅰ中体现了浓硫酸的_______ (填“氧化性”或“还原性”)。
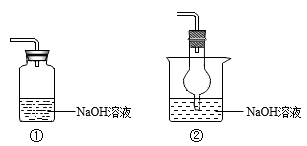
(2)下列装置中,能用于实验Ⅱ中尾气吸收的是_______ (填序号)。
(3)实验Ⅱ中,能够证明生成了SO2的证据是_______ 。
(4)实验Ⅰ和Ⅱ中,实验现象不同的原因是_______ 。
| 实验Ⅰ | 实验Ⅱ |
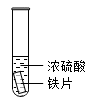 | 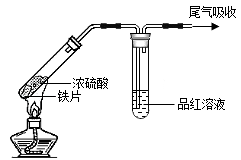 |
| 铁片表面迅速变暗,之后无明显变化 | 加热后产生大量气体,品红溶液褪色 |
(2)下列装置中,能用于实验Ⅱ中尾气吸收的是

(3)实验Ⅱ中,能够证明生成了SO2的证据是
(4)实验Ⅰ和Ⅱ中,实验现象不同的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】铁是人体内必需的微量元素,铁的化学性质较活泼,能与很多物质发生反应。完成下列填空:
(1)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(2)写出铁与水蒸气反应的化学方程式_______ 。
(3)写出铁与氯气恰好完全反应的化学方程式_______ 。将产物溶于水,能得到_______ 颜色的溶液,其产物中的阳离子可以用_______ 溶液检验,写出其离子方程式_______ 。
(1)常温下由于浓硫酸能使铁
(2)写出铁与水蒸气反应的化学方程式
(3)写出铁与氯气恰好完全反应的化学方程式
您最近一年使用:0次



