根据所学知识,回答下列问题:
(1)《本草纲目》对白酒(俗称烧酒)的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是___ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是___ 。
(3)欲使3molVO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少___ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是___ (用化学方程式表示)。
(5)下列变化为化学变化的是___ (填标号)。
A.CaCl2的潮解
B.钠的焰色反应
C.常温下,Fe遇浓硫酸钝化
(1)《本草纲目》对白酒(俗称烧酒)的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3molVO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解
B.钠的焰色反应
C.常温下,Fe遇浓硫酸钝化
更新时间:2021-04-08 16:13:59
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为____________ ,反应中每生成0.1 mol H2,转移电子数为________ NA。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶端分许,名曰发烛。”《资治通鉴》中记载:“陈宣帝太建九年,齐后妃贫苦,至以卖烛为业。”文中的“发烛”就是原始的火柴。已知K2Cr2O7用于工业中制造火柴头。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)___ (填元素名称 )元素被氧化,__ (填化学式 ,下同)是氧化剂。
(2)__ 是氧化产物,__ 发生氧化反应。
(3)参加反应的盐酸,表现了__ 性质。(填“还原性”“氧化性”或“酸性”)
(4)该反应中每生成3分子Cl2转移电子个数为__ 个。
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目___ 。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)
(2)
(3)参加反应的盐酸,表现了
(4)该反应中每生成3分子Cl2转移电子个数为
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氨气是一种无色而具有强烈刺激性的气体,比空气要轻。氨气在工农业生产中有重要应用。
(1)写出氨气的电子式_______ ;写出氨气的一种用途_______ 。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
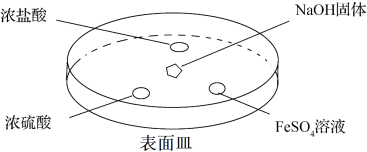
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ 。
② 溶液会出现的现象
溶液会出现的现象_______ 。
(3) 可以转化为其他含氮物质,下图为
可以转化为其他含氮物质,下图为 转化为
转化为 的流程。
的流程。
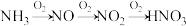
①写出 与
与 反应转化为NO的化学方程式
反应转化为NO的化学方程式_______ 。
② 转化为
转化为 的整个过程中,为提高氮原子的转化率,可采取的措施是
的整个过程中,为提高氮原子的转化率,可采取的措施是_______ 。
(1)写出氨气的电子式
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②
 溶液会出现的现象
溶液会出现的现象(3)
 可以转化为其他含氮物质,下图为
可以转化为其他含氮物质,下图为 转化为
转化为 的流程。
的流程。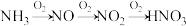
①写出
 与
与 反应转化为NO的化学方程式
反应转化为NO的化学方程式②
 转化为
转化为 的整个过程中,为提高氮原子的转化率,可采取的措施是
的整个过程中,为提高氮原子的转化率,可采取的措施是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】人类农业生产离不开氮肥,科学合理使用氰肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)某小组在实验室模拟以 为原料,制备少量硝态氮肥
为原料,制备少量硝态氮肥 ,转化途径如下(转化所需试剂及条件已略去)。
,转化途径如下(转化所需试剂及条件已略去)。
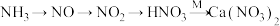
①工业合成氨是制取氮肥的基础。写出工业合成氨的化学反应方程式___________ 。
②写出实验室用NH4Cl和消石灰共热制备氨气的化学反应方程式_________________ 。
③写出NH3发生催化氧化反应生成NO的化学方程式____________________________ 。
向装置中通入4molNH3和2molO2,转移的电子数___________ (大于/小于/等于) 。
。
④工业上为了提高NO的转化率,可以适当增加O2的量,理论上在一定的温度和压强下将2LNO完全转化成HNO3,至少应该通入空气的体积为___________ 。
⑤将HNO3转化为Ca(NO3)2,列举两种不同类别的化合物M___________ (写化学式)。
(2)下列关于氮肥的使用说法正确的是___________。
(1)某小组在实验室模拟以
 为原料,制备少量硝态氮肥
为原料,制备少量硝态氮肥 ,转化途径如下(转化所需试剂及条件已略去)。
,转化途径如下(转化所需试剂及条件已略去)。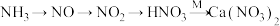
①工业合成氨是制取氮肥的基础。写出工业合成氨的化学反应方程式
②写出实验室用NH4Cl和消石灰共热制备氨气的化学反应方程式
③写出NH3发生催化氧化反应生成NO的化学方程式
向装置中通入4molNH3和2molO2,转移的电子数
 。
。④工业上为了提高NO的转化率,可以适当增加O2的量,理论上在一定的温度和压强下将2LNO完全转化成HNO3,至少应该通入空气的体积为
⑤将HNO3转化为Ca(NO3)2,列举两种不同类别的化合物M
(2)下列关于氮肥的使用说法正确的是___________。
| A.硝酸铵是一种常用的氮肥,在贮存和使用该化肥时不能剧烈撞击 |
| B.过度使用氮肥不会引起土壤和水体污染 |
| C.铵态氮肥和草木灰混合使用可以增强肥效 |
| D.铵态氮肥易与空气反应,因此需要深埋土壤中施用 |
您最近一年使用:0次
填空题
|
较易
(0.85)
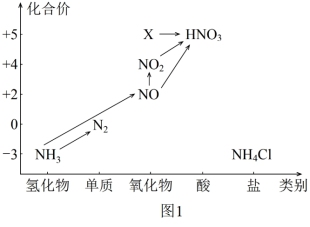
【推荐3】依据图中氮元素及其化合物的转化关系,回答问题:
(1)图1中,X的化学式为____ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_____ 。
②下列试剂能用于干燥NH3的是____ (填字母)。
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.五氧化二磷
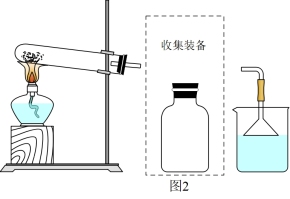
③若要收集一瓶氨气,请将收集装置补充完整,在图2虚框内画出连接图____ 。
④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:____ 。
(3)回答下列关于氮的氧化物的问题:
①将30mL(标准状况下)充满NO2气体的量筒倒置于水中,充分反应后,剩余气体的体积变为____ mL,生成硝酸的物质的量浓度c(HNO3)=____ mol/L。
②NO和NO2按一定比例混合可以被NaOH溶液完全吸收,写出相关化学方程式:____ 。
(1)图1中,X的化学式为

(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.五氧化二磷
③若要收集一瓶氨气,请将收集装置补充完整,在图2虚框内画出连接图

④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
(3)回答下列关于氮的氧化物的问题:
①将30mL(标准状况下)充满NO2气体的量筒倒置于水中,充分反应后,剩余气体的体积变为
②NO和NO2按一定比例混合可以被NaOH溶液完全吸收,写出相关化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
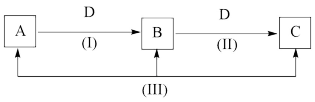
(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为___________ ;D中化学键的类型为___________ (填“离子键”或“共价键”)
②反应Ⅲ的离子方程式是___________ 。
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:___________ 、___________ 。
(3)写出Al(OH)3受热分解的化学方程式:___________ 。

(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为
②反应Ⅲ的离子方程式是
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:
(3)写出Al(OH)3受热分解的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】钠盐在生产和生活中扮演着很重要的角色,如生活中的调味品 NaCl;而钾盐却是是重要的肥料,如 KCl。那么区分这两类物质最简单的方法是:_____ ;此方法属于_________ (填“物理变化”或“化学变化”);具体结论是:_________
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,它们的主要成分如下表。
回答下列问题:
(1)以上主要成分中属于弱电解质的有___ (填序号)。NaCl中所含化学键类型为____________ 。
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是_____________ 。
(3)KAl(SO4)2·12H2O的电离方程式为_______________ 。
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为________ ;
Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为___________ 。
(5)NaHCO3溶液与白醋反应的离子方程式为_________________ 。
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:_______________ 。
商品 | 食盐 | 碱面 | 84消毒液 | 发酵粉 |
主要成分 | ① NaCl | ② Na2CO3 | ③ NaClO | ④ NaHCO3 ⑤KAl(SO4)2·12H2O |
商品 | 料酒 | 白醋 | 洁厕灵 | \ |
主要成分 | ⑥C2H5OH | ⑦CH3COOH | ⑧HCl |
回答下列问题:
(1)以上主要成分中属于弱电解质的有
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是
(3)KAl(SO4)2·12H2O的电离方程式为
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为
Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为
(5)NaHCO3溶液与白醋反应的离子方程式为
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】I.原电池是化学电源的雏形。
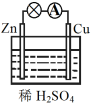
(1)如图连接好装置后,负极材料是_______ (填“Zn”或“Cu”)。
(2)相应原电池的总反应方程式为_______ 。
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是_______ (填序号)。
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2 2CO2 +3H2O
2CO2 +3H2O
II.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极。
(5)若X为银,Y为硝酸银溶液,则X的电极方程式_______
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是_______ 。

(1)如图连接好装置后,负极材料是
(2)相应原电池的总反应方程式为
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2
 2CO2 +3H2O
2CO2 +3H2OII.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
(5)若X为银,Y为硝酸银溶液,则X的电极方程式
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铁是人体内必需的微量元素,铁的化学性质较活泼,能与很多物质发生反应。完成下列填空:
(1)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(2)写出铁与水蒸气反应的化学方程式_______ 。
(3)写出铁与氯气恰好完全反应的化学方程式_______ 。将产物溶于水,能得到_______ 颜色的溶液,其产物中的阳离子可以用_______ 溶液检验,写出其离子方程式_______ 。
(1)常温下由于浓硫酸能使铁
(2)写出铁与水蒸气反应的化学方程式
(3)写出铁与氯气恰好完全反应的化学方程式
您最近一年使用:0次

 B.
B.  C.
C.