根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
⑴氧化剂是_______________ , 还原剂是________________ 。
⑵氧化剂和还原剂的分子个数比___________________________ 。
⑶当有68克氨气参加反应时,被氧化的物质为_____________ 克, 生成还原产物为_________ 克。
⑴氧化剂是
⑵氧化剂和还原剂的分子个数比
⑶当有68克氨气参加反应时,被氧化的物质为
12-13高一·全国·课时练习 查看更多[4]
(已下线)2012年鲁科版高中化学必修1 2.3氧化剂和还原剂练习卷江苏省东台市创新学校2017-2018学年高一10月月考化学试题湖北省荆州市沙市区沙市中学高一上学期化学第二章《化学物质及其变化》过关训练7吉林省舒兰市第十八中学校2022-2023学年高一上学期期中考试化学试题
更新时间:2017/11/07 20:51:46
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)已知下列十种物质①CH3COOH②Cu③NO④干冰⑤硫酸⑥Ba(OH)2⑦Fe(OH)3胶体⑧液氨⑨稀硝酸⑩NaHSO4。根据上述提供的物质,回答下列问题
①属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
②在熔融状态下不导电而在水溶液下导电的电解质是___________ 。
③实验室制备⑦的操作是___________
(2)在2Fe3++2I﹣=I2+2Fe2+反应中,___________ 是氧化剂,___________ 发生氧化反应。
①属于电解质的是
②在熔融状态下不导电而在水溶液下导电的电解质是
③实验室制备⑦的操作是
(2)在2Fe3++2I﹣=I2+2Fe2+反应中,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】SO2从组成和性质看属于酸性氧化物,从化合价来看具有氧化性和还原性,请完成并配平下列化学反应方程式
(1)SO2+H2O_______
(2)SO2+CaO_______
(3)SO2+Ca(OH)2_______
(4)SO2+H2S_______
(5)SO2+H2O2_______
(6)Cl2+SO2+H2O_______
(7)SO2 +H2O+KMnO4_______
从离子角度看,反应(7)中的氧化产物是_______ ,还原产物是________ (均填写离子符号)。
(1)SO2+H2O
(2)SO2+CaO
(3)SO2+Ca(OH)2
(4)SO2+H2S
(5)SO2+H2O2
(6)Cl2+SO2+H2O
(7)SO2 +H2O+KMnO4
从离子角度看,反应(7)中的氧化产物是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氧化还原反应在生产生活中应用十分广泛。回答下列问题:
(1)过氧化氢水溶液俗称双氧水,具有杀菌消毒作用,可用来清洗伤口,还可用作矿业废液消毒剂,H2O2有“绿色氧化剂”的美称。已知下列与H2O2有关的反应:
A、Na2O2+2HCl=2NaCl+H2O2
B、Ag2O+H2O2=2Ag+O2↑+H2O
C、2H2O2 2H2O+O2↑
2H2O+O2↑
D、H2O2+H2S=2H2O+S↓
上述反应中,H2O2仅体现氧化性的是___________ (填序号,下同), H2O2既体现氧化性又体现还原性的是___________ 。
(2)Cl2是一种工业上常用的氧化剂,可以用浓氨水检验输送氯气的管道是否泄漏,原理为:3Cl2+8NH3=6NH4Cl+N2。
①该反应中被氧化的元素是___________ 。
②请用示例中的方法标出该反应中电子转移的方向和数目:___________ 。
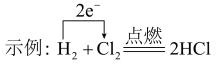
(1)过氧化氢水溶液俗称双氧水,具有杀菌消毒作用,可用来清洗伤口,还可用作矿业废液消毒剂,H2O2有“绿色氧化剂”的美称。已知下列与H2O2有关的反应:
A、Na2O2+2HCl=2NaCl+H2O2
B、Ag2O+H2O2=2Ag+O2↑+H2O
C、2H2O2
 2H2O+O2↑
2H2O+O2↑D、H2O2+H2S=2H2O+S↓
上述反应中,H2O2仅体现氧化性的是
(2)Cl2是一种工业上常用的氧化剂,可以用浓氨水检验输送氯气的管道是否泄漏,原理为:3Cl2+8NH3=6NH4Cl+N2。
①该反应中被氧化的元素是
②请用示例中的方法标出该反应中电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】氧化还原反应在生产、生活中有广泛的应用,回答下列问题:
(1)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下: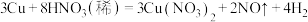
①被氧化的元素是_______ ,被还原的元素是_______ ,氧化剂与还原剂的物质的量之比是_______ 。
②每转移0.3mol电子时,理论上能产生标准状况下气体体积为_______ L。
(2)铀(U)元素在核工业中具有重要作用,工业上可利用钾、钙、镁等金属与铀矿石(主要成分二氧化铀)反应制得铀单质。若要获得等质量的铀单质,钾、钙、镁三种金属中,所耗金属质量最小的是_______ 。
(3) 能与热的经硫酸酸化的
能与热的经硫酸酸化的 溶液反应,生成
溶液反应,生成 和
和 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(1)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:
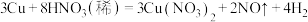
①被氧化的元素是
②每转移0.3mol电子时,理论上能产生标准状况下气体体积为
(2)铀(U)元素在核工业中具有重要作用,工业上可利用钾、钙、镁等金属与铀矿石(主要成分二氧化铀)反应制得铀单质。若要获得等质量的铀单质,钾、钙、镁三种金属中,所耗金属质量最小的是
(3)
 能与热的经硫酸酸化的
能与热的经硫酸酸化的 溶液反应,生成
溶液反应,生成 和
和 ,该反应的离子方程式是
,该反应的离子方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】当Cl2遇到NH3时,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用“双线桥法”表示反应的电子转移方向和数目:___________ ;
(2)参加反应的NH3中,被氧化的N原子与未被氧化的N原子之比:___________ ;
(3)写出NH4Cl在溶液中的电离方程式___________ ,在其溶液中分散质粒子的直径范围为___________ ;
(4)若反应中有6.8g氨发生氧化反应,则反应中有生成氮气的质量为___________ g;请写出N2的一种用途___________ 。
(1)用“双线桥法”表示反应的电子转移方向和数目:
(2)参加反应的NH3中,被氧化的N原子与未被氧化的N原子之比:
(3)写出NH4Cl在溶液中的电离方程式
(4)若反应中有6.8g氨发生氧化反应,则反应中有生成氮气的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】①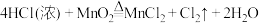
②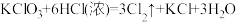
③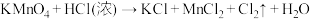 (未配平)
(未配平)
④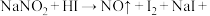 ______(未配平)
______(未配平)
根据以上四个反应,回答下列有关问题:
(1)反应②的离子方程式为______ 。
(2)反应②中,氧化产物与还原产物的质量比为______ 。
(3)请将反应配平: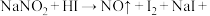
______
(4)若要制得相同质量的氯气,①②③反应中电子转移数目之比为______ 。
(5)已知反应:⑤ ,该反应也能制得氯气,则
,该反应也能制得氯气,则 、
、 、
、 三种物质氧化性由强到弱的顺序为
三种物质氧化性由强到弱的顺序为______ 。
一种有效成分为 、
、 、
、 的“二氧化氯泡腾片”能快速溶于水,放出大量
的“二氧化氯泡腾片”能快速溶于水,放出大量 ,得到
,得到 溶液。生成
溶液。生成 的化学方程式为
的化学方程式为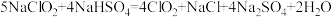 。
。
(6)该反应中氧化剂为______ (填化学式,下同),还原剂为______ 。
(7)用双线桥法表示该反应中电子转移的方向和数目:______ 。
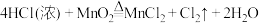
②
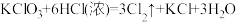
③
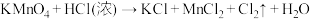 (未配平)
(未配平)④
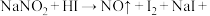 ______(未配平)
______(未配平)根据以上四个反应,回答下列有关问题:
(1)反应②的离子方程式为
(2)反应②中,氧化产物与还原产物的质量比为
(3)请将反应配平:
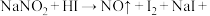
(4)若要制得相同质量的氯气,①②③反应中电子转移数目之比为
(5)已知反应:⑤
 ,该反应也能制得氯气,则
,该反应也能制得氯气,则 、
、 、
、 三种物质氧化性由强到弱的顺序为
三种物质氧化性由强到弱的顺序为一种有效成分为
 、
、 、
、 的“二氧化氯泡腾片”能快速溶于水,放出大量
的“二氧化氯泡腾片”能快速溶于水,放出大量 ,得到
,得到 溶液。生成
溶液。生成 的化学方程式为
的化学方程式为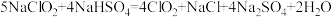 。
。(6)该反应中氧化剂为
(7)用双线桥法表示该反应中电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】黄铁矿主要成分是FeS2 。某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。(M(FeS2)=120g/mol)
已知:SO2 + Fe3+ + H2O ——SO42- +Fe2+ + H+
Cr2O7 2-+ 6 Fe2+ + 14 H+ ==== 2 Cr3+ + 6 Fe3+ + 7 H2O
(1)将此方程式配平:_______________________________________________________________ H+
(2)样品中FeS2的质量分数是(假设杂质不参加反应)________________ 。
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为_______________ L,制得98%的硫酸 质量为__________ t 。
已知:SO2 + Fe3+ + H2O ——SO42- +Fe2+ + H+
Cr2O7 2-+ 6 Fe2+ + 14 H+ ==== 2 Cr3+ + 6 Fe3+ + 7 H2O
(1)将此方程式配平:
(2)样品中FeS2的质量分数是(假设杂质不参加反应)
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题。
(1)体检报告中的一些指标常用物质的量浓度表示,如人体血糖(即血液中的葡萄糖,葡萄糖摩尔质量为180g/mol)可用“mmol∙L−1”表示,也可以用“mg∙dL−1”(1L=10dL)表示。已知以“mmol∙L−1”表示时,人的血糖正常值为3.9~6.1mmol∙L−1。某同学体检单显示血糖结果为97.2mg∙dL−1,则该同学血糖值为_______ mmol∙L−1,说明该同学血糖指标_______ (填“正常”/“不正常”)。
(2)取部分被氧化的铁粉若干克,将其溶于200ml某浓度的硝酸,恰好完全反应,并释放出448mLNO(标准状况下)。将所得溶液平均分为两份,向第一份溶液中加入足量氢氧化钠溶液,过滤、洗涤、灼烧,得到8.00g红棕色固体;向第二份溶液中通入672mLCl2(标准状况下),恰好完全反应(不考虑氯气的溶解)。试计算:
①样品和硝酸反应后的溶液中,n(Fe2+):n(Fe3+)=________ 。
②硝酸溶液的浓度c=_______ mol∙L−1。
(1)体检报告中的一些指标常用物质的量浓度表示,如人体血糖(即血液中的葡萄糖,葡萄糖摩尔质量为180g/mol)可用“mmol∙L−1”表示,也可以用“mg∙dL−1”(1L=10dL)表示。已知以“mmol∙L−1”表示时,人的血糖正常值为3.9~6.1mmol∙L−1。某同学体检单显示血糖结果为97.2mg∙dL−1,则该同学血糖值为
(2)取部分被氧化的铁粉若干克,将其溶于200ml某浓度的硝酸,恰好完全反应,并释放出448mLNO(标准状况下)。将所得溶液平均分为两份,向第一份溶液中加入足量氢氧化钠溶液,过滤、洗涤、灼烧,得到8.00g红棕色固体;向第二份溶液中通入672mLCl2(标准状况下),恰好完全反应(不考虑氯气的溶解)。试计算:
①样品和硝酸反应后的溶液中,n(Fe2+):n(Fe3+)=
②硝酸溶液的浓度c=
您最近一年使用:0次

 固体,加入足量
固体,加入足量 溶液,使
溶液,使 全部转化成
全部转化成 ,并放出NO气体。
,并放出NO气体。
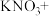
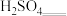

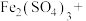

 。
。

