《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶端分许,名曰发烛。”《资治通鉴》中记载:“陈宣帝太建九年,齐后妃贫苦,至以卖烛为业。”文中的“发烛”就是原始的火柴。已知K2Cr2O7用于工业中制造火柴头。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)___ (填元素名称 )元素被氧化,__ (填化学式 ,下同)是氧化剂。
(2)__ 是氧化产物,__ 发生氧化反应。
(3)参加反应的盐酸,表现了__ 性质。(填“还原性”“氧化性”或“酸性”)
(4)该反应中每生成3分子Cl2转移电子个数为__ 个。
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目___ 。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)
(2)
(3)参加反应的盐酸,表现了
(4)该反应中每生成3分子Cl2转移电子个数为
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目
更新时间:2020-10-25 15:13:28
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】化学与人类生活密切相关。请按要求回答下列问题:
(1)小苏打可用于治疗胃酸过多,其反应的化学方程式为_______ 。
(2)电子工业中常用氯化铁溶液刻蚀覆铜板制印刷电路板,该反应的离子方程式为_______ 。
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是NaClO)而发生氯气中毒事件,其原理为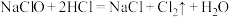 。该反应的氧化剂是
。该反应的氧化剂是_______ (填化学式);当生成的气体在标准状况下的体积为5.6L时转移的电子数为_______ 个。
(1)小苏打可用于治疗胃酸过多,其反应的化学方程式为
(2)电子工业中常用氯化铁溶液刻蚀覆铜板制印刷电路板,该反应的离子方程式为
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是NaClO)而发生氯气中毒事件,其原理为
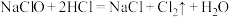 。该反应的氧化剂是
。该反应的氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】配平以下反应方程式:_______
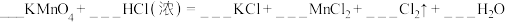
氧化剂是___________ ,氧化产物是___________ ;反应产生标准状况下 氯气时,被氧化是
氯气时,被氧化是 的物质的量为
的物质的量为___________  ,转移电子数为
,转移电子数为___________ .
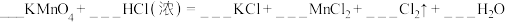
氧化剂是
 氯气时,被氧化是
氯气时,被氧化是 的物质的量为
的物质的量为 ,转移电子数为
,转移电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】过氧化氢溶液在医疗上用来杀菌消毒、清洗伤口。根据下列A-D涉及H2O2的反应填空。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.2H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是_______ (填字母,下同)。
(2)H2O2仅体现还原性的反应是_______ 。
(3)H2O2既体现氧化性又体现还原性的反应是_______ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.2H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是
(2)H2O2仅体现还原性的反应是
(3)H2O2既体现氧化性又体现还原性的反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式是__ (填“游离态”或“化合态”)。
②氯碱工业是重要的化学工业之一,写出该反应原理的离子方程式:__ 。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①铁和铝是两种常见的金属材料,在空气中铝比铁耐腐蚀的原因是__ 。
②新型陶瓷氮化铝可用氧化铝高温还原法制备,化学方程式如下,请配平该化学反应方程式并标出电子转移方向和数目。_________
Al2O3+C+N2 AlN+CO
AlN+CO
(3)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。
①写出二氧化硫与足量NaOH溶液反应的离子方程式:__ 。
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强。写出这一过程的化学方程式:__ 。
(1)海水中蕴含的元素有80多种。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式是
②氯碱工业是重要的化学工业之一,写出该反应原理的离子方程式:
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①铁和铝是两种常见的金属材料,在空气中铝比铁耐腐蚀的原因是
②新型陶瓷氮化铝可用氧化铝高温还原法制备,化学方程式如下,请配平该化学反应方程式并标出电子转移方向和数目。
Al2O3+C+N2
 AlN+CO
AlN+CO(3)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。
①写出二氧化硫与足量NaOH溶液反应的离子方程式:
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强。写出这一过程的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在K2Cr2O7+14HCl===2KCl+2CrCl3+3Cl2↑+7H2O反应中。
(1)________ 元素被氧化,________ 是氧化剂。
(2)________ 是氧化产物,________ 发生氧化反应。
(3)用双线桥法标明电子转移的方向和数目___________________________________________________
(1)
(2)
(3)用双线桥法标明电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】大气污染是环境污染的一个重要方面,《国家环境保护法》严禁把大气污染物大量排入大气。硫元素的氢化物与氧化物都是大气污染物,它的单质是我国古代四大发明之一黑火药的重要成分。试回答:
(1)写出硫元素的氢化物的化学式______ ,存在的化学键类型是______ 。
(2)用足量氢氧化钠溶液来吸收硫元素的氢化物,其反应的离子方程式是________ 。
(3)硫和氧气直接反应的产物是形成酸雨的主要原因之一,则该氧化物的名称是____ 。
(4)下列实验,能说明浓硫酸有脱水性的是______ ,有氧化性的是______ 。
a. 能与铜反应放出SO2
b. 能与NaCl反应制取氯化氢
c.浓硫酸滴在纸片上发生炭化变黑现象
(5)火药点燃后发生的反应如下:S+2KNO3+3C=K2S+3CO2↑+N2↑,其中还原剂是______ 。
(1)写出硫元素的氢化物的化学式
(2)用足量氢氧化钠溶液来吸收硫元素的氢化物,其反应的离子方程式是
(3)硫和氧气直接反应的产物是形成酸雨的主要原因之一,则该氧化物的名称是
(4)下列实验,能说明浓硫酸有脱水性的是
a. 能与铜反应放出SO2
b. 能与NaCl反应制取氯化氢
c.浓硫酸滴在纸片上发生炭化变黑现象
(5)火药点燃后发生的反应如下:S+2KNO3+3C=K2S+3CO2↑+N2↑,其中还原剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】2FeCl3+Fe=3FeCl2的氧化剂为___ ;还原剂为___ ;氧化产物为___ ;还原产物为___ 。
您最近一年使用:0次
【推荐1】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷的电子式为__ 。
(2)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是__ 。
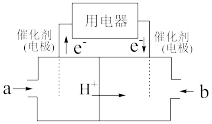
(3)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为__ ,通入b气体的电极反应式__ 。(质子交换膜只允许H+通过)
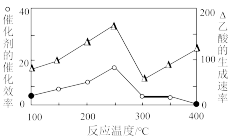
(4)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在__ 左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为__ 。
(5)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为__ 。
(1)甲烷的电子式为
(2)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是
(3)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为

(4)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在

②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
(5)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】实验室用金属铜和稀硝酸制取NO,而NO是有毒气体,某学生为防止污染,设 计了一套能随开随用随关随停的NO气体发生装置,如图所示。

反应开始后,可以在U形管右端观察到无色的NO气体。
(1)长玻璃管的作用是_______ ;让反应停止的操作方法及原因是_______
(2)现U形管中有500mL的稀硝酸(足量)与铜丝反应,当收集到2.24 L(标准状况)NO后 停止反应,测得反应前后铜丝质量减少了xg,向剩余溶液中加入VmLa mol/L的NaOH 溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为______ (忽略装置内残留的气体)

反应开始后,可以在U形管右端观察到无色的NO气体。
(1)长玻璃管的作用是
(2)现U形管中有500mL的稀硝酸(足量)与铜丝反应,当收集到2.24 L(标准状况)NO后 停止反应,测得反应前后铜丝质量减少了xg,向剩余溶液中加入VmLa mol/L的NaOH 溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】铁及其化合物在日常生产生活中应用广泛,研究意义重大。
(1)医疗上流行的“理疗特效热”,是利用铁缓慢氧化放出均匀、稳定的热,使患处保持温热状态。若56g铁粉完全被氧化成氧化铁,则需要消耗标况下氧气的体积为___________ L。
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。检验某固体补铁剂中铁元素已被氧化的实验方法及结论为___________ 。
(3)氯化铁的用途之一是五金蚀刻,蚀刻产品有眼镜架、钟表、电子元件和不锈钢标牌等。氯化铁溶液蚀刻不锈钢时发生的主要反应的离子方程式为___________ 。
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。湿法制备高铁酸钠反应体系中有六种微粒:Fe3+、ClO-、OH-、 、Cl-、H2O,则湿法制高铁酸钠的离子反应方程式为
、Cl-、H2O,则湿法制高铁酸钠的离子反应方程式为___________ ,该反应中,被氧化的元素是___________ (填元素符号),氧化剂是___________ (填化学式),生成lmol高铁酸钠时,转移电子的物质的量为___________ mol。
(1)医疗上流行的“理疗特效热”,是利用铁缓慢氧化放出均匀、稳定的热,使患处保持温热状态。若56g铁粉完全被氧化成氧化铁,则需要消耗标况下氧气的体积为
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。检验某固体补铁剂中铁元素已被氧化的实验方法及结论为
(3)氯化铁的用途之一是五金蚀刻,蚀刻产品有眼镜架、钟表、电子元件和不锈钢标牌等。氯化铁溶液蚀刻不锈钢时发生的主要反应的离子方程式为
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。湿法制备高铁酸钠反应体系中有六种微粒:Fe3+、ClO-、OH-、
 、Cl-、H2O,则湿法制高铁酸钠的离子反应方程式为
、Cl-、H2O,则湿法制高铁酸钠的离子反应方程式为
您最近一年使用:0次

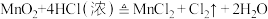 ,据此回答下列问题:
,据此回答下列问题: 发生了
发生了 电子转移的方向和数目:
电子转移的方向和数目:

