I.原电池是化学电源的雏形。
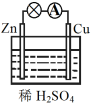
(1)如图连接好装置后,负极材料是_______ (填“Zn”或“Cu”)。
(2)相应原电池的总反应方程式为_______ 。
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是_______ (填序号)。
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2 2CO2 +3H2O
2CO2 +3H2O
II.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极。
(5)若X为银,Y为硝酸银溶液,则X的电极方程式_______
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是_______ 。

(1)如图连接好装置后,负极材料是
(2)相应原电池的总反应方程式为
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2
 2CO2 +3H2O
2CO2 +3H2OII.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
(5)若X为银,Y为硝酸银溶液,则X的电极方程式
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是
更新时间:2022-09-15 19:16:03
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】回答以下问题:
(1)将Cu片加入稀硝酸中,反应开始时,在试管中可以看到红棕色气体,原因是_______ 。
(2)将足量Cu片加入浓硝酸中,充分反应后,产生的气体有_______ 。
(3)将Cu片加入KNO3溶液中,再加入稀硫酸,发生反应的离子方程式为_______ 。
(1)将Cu片加入稀硝酸中,反应开始时,在试管中可以看到红棕色气体,原因是
(2)将足量Cu片加入浓硝酸中,充分反应后,产生的气体有
(3)将Cu片加入KNO3溶液中,再加入稀硫酸,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】请按要求书写下列方程式。
(1)实验室常用热的氢氧化钠溶液洗去试管内壁附着的硫磺,其原理为___________ (用化学方程式表示)。
(2)实验室中可利用 粉末与质量分数为70%的硫酸反应制取少量
粉末与质量分数为70%的硫酸反应制取少量 反应的化学方程式为
反应的化学方程式为___________ 。
(3)写出氨气实验室制法的化学方程式___________ 。
(4)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:___________ 。
(5)铜与稀硝酸的离子方程式为:___________ 。
(1)实验室常用热的氢氧化钠溶液洗去试管内壁附着的硫磺,其原理为
(2)实验室中可利用
 粉末与质量分数为70%的硫酸反应制取少量
粉末与质量分数为70%的硫酸反应制取少量 反应的化学方程式为
反应的化学方程式为(3)写出氨气实验室制法的化学方程式
(4)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:
(5)铜与稀硝酸的离子方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知:浓硝酸和铜在常温下反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。回答下列问题:
(1)在这个反应中,浓硝酸表现的化学性质是____ 性(填“酸”或“碱”)和____ 性(填“氧化”或“还原”)。
(2)Cu(NO3)2的电离方程式为____ 。
(3)在离子方程式中,单质、氧化物、水、气体、难溶物等不写成离子形式,该反应的离子方程式为____ 。
(4)随着反应的进行,硝酸的浓度减小,发生3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应。在该反应中,有3个Cu原子反应,有____ 个NO 转化为气体。
转化为气体。
(5)氮的氧化物有毒。用等量的铜制备Cu(NO3)2,有三种方法:
方法一:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
方法二:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
方法三:2Cu+O2+4HNO3 2Cu(NO3)2+2H2O
2Cu(NO3)2+2H2O
请从经济效益(硝酸根都进入硝酸铜)和社会效益(无有毒气体排放)考虑,最优方法是____ 。
(1)在这个反应中,浓硝酸表现的化学性质是
(2)Cu(NO3)2的电离方程式为
(3)在离子方程式中,单质、氧化物、水、气体、难溶物等不写成离子形式,该反应的离子方程式为
(4)随着反应的进行,硝酸的浓度减小,发生3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应。在该反应中,有3个Cu原子反应,有
 转化为气体。
转化为气体。(5)氮的氧化物有毒。用等量的铜制备Cu(NO3)2,有三种方法:
方法一:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
方法二:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
方法三:2Cu+O2+4HNO3
 2Cu(NO3)2+2H2O
2Cu(NO3)2+2H2O请从经济效益(硝酸根都进入硝酸铜)和社会效益(无有毒气体排放)考虑,最优方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】依据氧化还原反应:2Ag+(aq)+Zn(s)=Zn2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
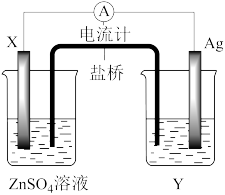
(1)电极X的材料是_______ ;电解质溶液Y是_______ ;
(2)银电极为电池的_______ 极(填“正”或“负”);X发生的电极反应为_______
(3)外电路中的电子是从_______ 电极流向_______ 电极。(填“X”或“银”)

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】人们常常利用化学反应中的能量变化为人类服务。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是_________ 。
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是_________ 。
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:
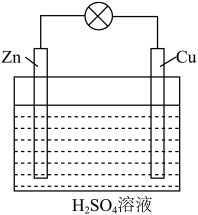
①负极材料是_______ ,正极上能够观察到的现象是_______________________ ,
②正极的电极反应式是______________ 。
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体________ L(标况下)。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:

①负极材料是
②正极的电极反应式是
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】1836年丹尼尔发明了世界上第一个实用电池,下图是实验室模拟原电池原理组装的丹尼尔电池,盐桥中装有饱和 溶液的琼胶,回答下列问题。
溶液的琼胶,回答下列问题。
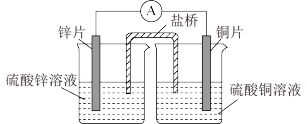
(1)上图装置中能量的转化形式为___________ 能转化为___________ 能;
(2)在该原电池中,___________ 是负极材料(填“锌片”或“铜片”),铜片一极发生___________ 反应(填“氧化”或“还原”);
(3)当该原电池开始工作时,盐桥中的 的移动方向是
的移动方向是___________ (请在下列选项中选择)
A. 流向硫酸锌溶液 B. 流向硫酸铜溶液
(4)该原电池的正极电极反应式为___________ ;当电路中转移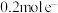 时,锌片溶解的质量为
时,锌片溶解的质量为___________  。
。
 溶液的琼胶,回答下列问题。
溶液的琼胶,回答下列问题。
(1)上图装置中能量的转化形式为
(2)在该原电池中,
(3)当该原电池开始工作时,盐桥中的
 的移动方向是
的移动方向是A. 流向硫酸锌溶液 B. 流向硫酸铜溶液
(4)该原电池的正极电极反应式为
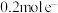 时,锌片溶解的质量为
时,锌片溶解的质量为 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】分离出合成气中的H2,用于氢氧燃料电池。如图为电池示意图。
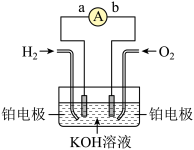
(1)氢氧燃料电池的能量转化主要形式是___ ,在导线中电子流动方向为___ (用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___ 。
(3)当电池工作时,在KOH溶液中阴离子向___ 移动(填正极或负极)。

(1)氢氧燃料电池的能量转化主要形式是
(2)正极反应的电极反应方程式为
(3)当电池工作时,在KOH溶液中阴离子向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】利用反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是__ ,发生__ (填“氧化”或“还原”)反应,电解质溶液是__ 。
(2)正极上出现的现象是___ 。
(3)若导线上转移电子1mol,则生成银__ g。
(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子1mol,则生成银
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】工厂烟气(主要污染物有SO2、NO)直接排放会造成空气污染,水溶性硝态氮(NO 、NO
、NO 等)是水体污染物,需要处理才能排放。
等)是水体污染物,需要处理才能排放。
(1)CO(NH2)2溶液脱硫的反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2(该反应为非氧化还原反应)。若吸收烟气时通入少量ClO2,可同时实现脱硫、脱硝。脱硝的反应分为两步。
第一步:5NO+2ClO2+H2O=5NO2+2HCl
第二步:NO2和CO(NH2)2反应生成N2、CO2和水。
请写出第二步反应的化学方程式为__ 。
(2)“纳米零价铁—H2O2”体系可将烟气中难溶的NO氧化为可溶的NO 。
。
在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①NO与H2O2反应生成HNO3的化学方程式为__ 。
②Fe2+催化H2O2分解产生HO•,HO•将NO氧化为NO 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为__ 。

③通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示。已知O2-可在固体电解质中自由移动。NiO电极上的电极反应式为__ 。

(3)纳米铁粉可用于去除废水中的硝态氮(以NO 表示)可大致分为2个过程,反应原理如图所示。
表示)可大致分为2个过程,反应原理如图所示。
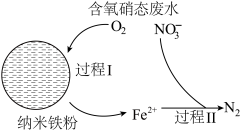
①有研究发现,在铁粉总量一定的条件下,水中的溶解氧过少或过多均不利于硝态氮去除。若水中的溶解氧过少,硝态氮去除率下降的原因是__ 。
②利用纳米铁粉与活性炭混合物可提升硝态废水中硝态氮的去除效率,可能原因是__ 。
 、NO
、NO 等)是水体污染物,需要处理才能排放。
等)是水体污染物,需要处理才能排放。(1)CO(NH2)2溶液脱硫的反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2(该反应为非氧化还原反应)。若吸收烟气时通入少量ClO2,可同时实现脱硫、脱硝。脱硝的反应分为两步。
第一步:5NO+2ClO2+H2O=5NO2+2HCl
第二步:NO2和CO(NH2)2反应生成N2、CO2和水。
请写出第二步反应的化学方程式为
(2)“纳米零价铁—H2O2”体系可将烟气中难溶的NO氧化为可溶的NO
 。
。在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①NO与H2O2反应生成HNO3的化学方程式为
②Fe2+催化H2O2分解产生HO•,HO•将NO氧化为NO
 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为
③通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示。已知O2-可在固体电解质中自由移动。NiO电极上的电极反应式为

(3)纳米铁粉可用于去除废水中的硝态氮(以NO
 表示)可大致分为2个过程,反应原理如图所示。
表示)可大致分为2个过程,反应原理如图所示。
①有研究发现,在铁粉总量一定的条件下,水中的溶解氧过少或过多均不利于硝态氮去除。若水中的溶解氧过少,硝态氮去除率下降的原因是
②利用纳米铁粉与活性炭混合物可提升硝态废水中硝态氮的去除效率,可能原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是_______ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是_______ 。
(3)欲使3 mol VO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少_______ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是_______ (用化学方程式表示)。
(5)下列变化为化学变化的是_______ (填标号)。
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3 mol VO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学是一门实用性很强的科学。根据题意填空:
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g) Fe3O4+4H2.该反应中H2O作
Fe3O4+4H2.该反应中H2O作___________ (填“氧化剂”或“还原剂”);
(2)常温条件下,可以用铁罐盛装浓硫酸和浓硝酸,是因为常温下,浓硫酸和浓硝酸可以使铁发生___________ ;
(3)人们使用量最大的传统硅酸盐产品有水泥、玻璃和___________ ;
(4)浓硫酸可以干燥氢气、氧气、氯气、二氧化硫等气体,这体现了浓硫酸具有___________ ;
(5)某学习小组为了探究碳与浓H2SO4反应的产物,将浓H2SO4和木炭反应产生的气体进行了实验:当把产生的气体通入足量的澄清石灰水,产生白色沉淀。该小组认为气体中含有CO2,你认为该结论:___________ (填“正确”或“不正确”)。
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g)
 Fe3O4+4H2.该反应中H2O作
Fe3O4+4H2.该反应中H2O作(2)常温条件下,可以用铁罐盛装浓硫酸和浓硝酸,是因为常温下,浓硫酸和浓硝酸可以使铁发生
(3)人们使用量最大的传统硅酸盐产品有水泥、玻璃和
(4)浓硫酸可以干燥氢气、氧气、氯气、二氧化硫等气体,这体现了浓硫酸具有
(5)某学习小组为了探究碳与浓H2SO4反应的产物,将浓H2SO4和木炭反应产生的气体进行了实验:当把产生的气体通入足量的澄清石灰水,产生白色沉淀。该小组认为气体中含有CO2,你认为该结论:
您最近一年使用:0次

 B.
B.  C.
C.