Ⅰ.(1)标准状况下,5.6LO2的质量为_____ 克,共含有_____ 个原子。
(2)在标准状况下,8gCO2和CO组成的混合气体,其体积为5.6L,则此混合气体中CO2的质量分数为_____
(3)用托盘天平称取5.0gCuSO4·5H2O晶体,溶于水配成100mL溶液,其物质的量浓度为_ 。
Ⅱ.欲用 的浓硫酸(密度为
的浓硫酸(密度为 )配制成浓度为
)配制成浓度为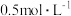 的稀硫酸480ml。
的稀硫酸480ml。
(1)选用的主要仪器有:①玻璃棒,②烧杯,③量筒,④胶头滴管,⑤_____ 。
(2)请将下列各操作相应的序号按要求填在横线上。
A.用量筒量取浓硫酸 B.反复颠倒摇匀 C.用胶头滴管加蒸馏水至刻度线
D.稀释浓硫酸 E.将溶液转入容量瓶
其正确的操作顺序依次为______ 。
(3)简要回答下列问题:
①所需浓硫酸的体积为________ mL。
②定容时必须使溶液凹液面与刻度线相切,若仰视会使浓度________ 。(填“偏大”、“偏小”、“不变”)
(2)在标准状况下,8gCO2和CO组成的混合气体,其体积为5.6L,则此混合气体中CO2的质量分数为
(3)用托盘天平称取5.0gCuSO4·5H2O晶体,溶于水配成100mL溶液,其物质的量浓度为
Ⅱ.欲用
 的浓硫酸(密度为
的浓硫酸(密度为 )配制成浓度为
)配制成浓度为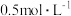 的稀硫酸480ml。
的稀硫酸480ml。(1)选用的主要仪器有:①玻璃棒,②烧杯,③量筒,④胶头滴管,⑤
(2)请将下列各操作相应的序号按要求填在横线上。
A.用量筒量取浓硫酸 B.反复颠倒摇匀 C.用胶头滴管加蒸馏水至刻度线
D.稀释浓硫酸 E.将溶液转入容量瓶
其正确的操作顺序依次为
(3)简要回答下列问题:
①所需浓硫酸的体积为
②定容时必须使溶液凹液面与刻度线相切,若仰视会使浓度
20-21高一上·黑龙江佳木斯·阶段练习 查看更多[2]
更新时间:2020-12-30 23:23:41
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知反应:2SO2+O2 2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率
2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率____ 、____ 、____ 。
 2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率
2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率
您最近一年使用:0次
【推荐2】某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为_______ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH−)=_______ mol·L−1。
(2)煤燃烧排放的烟气中含有SO2和NOx,易形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式_______ 。
_______ClO +_______NO+_______OH−=_______Cl−+_______NO
+_______NO+_______OH−=_______Cl−+_______NO +_______
+_______
(3)汽车尾气中NOx和CO的生成及转化。
①汽车启动时汽缸温度高,汽缸中会生成NO,化学方程式为_______ 。
②汽车燃油不完全燃烧时产生CO。在汽车尾气系统中装上催化转化器可使CO和NO反应转化为无污染、无毒性的两种气体,其化学反应方程式为_______ 。
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl− |
| 浓度/mol·L−1 | 4×10−6 | 6×10−6 | 2×10−5 | 4×10−5 | 3×10−5 | 2×10−5 |
(2)煤燃烧排放的烟气中含有SO2和NOx,易形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式
_______ClO
 +_______NO+_______OH−=_______Cl−+_______NO
+_______NO+_______OH−=_______Cl−+_______NO +_______
+_______(3)汽车尾气中NOx和CO的生成及转化。
①汽车启动时汽缸温度高,汽缸中会生成NO,化学方程式为
②汽车燃油不完全燃烧时产生CO。在汽车尾气系统中装上催化转化器可使CO和NO反应转化为无污染、无毒性的两种气体,其化学反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)含有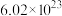 个氧原子的
个氧原子的 的物质的量是
的物质的量是___________  。
。
(2)与标准状况下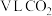 所含氧原子数目相同的水的质量是
所含氧原子数目相同的水的质量是___________ (用最简分数表示)。
(3)标准状况下有①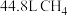 ,②
,② 个
个 分子,③
分子,③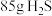 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是___________ 。(填序号)
(4)在一定的温度和压强下,1体积气体 跟3体积气体
跟3体积气体 化合生成2体积化合物,则该化合物的化学式是
化合生成2体积化合物,则该化合物的化学式是___________ 。
(5)某盐混合溶液中含有离子: 、
、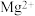 、
、 、
、 ,测得
,测得 、
、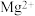 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则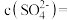
___________ 。
(1)含有
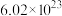 个氧原子的
个氧原子的 的物质的量是
的物质的量是 。
。(2)与标准状况下
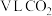 所含氧原子数目相同的水的质量是
所含氧原子数目相同的水的质量是(3)标准状况下有①
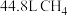 ,②
,② 个
个 分子,③
分子,③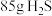 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(4)在一定的温度和压强下,1体积气体
 跟3体积气体
跟3体积气体 化合生成2体积化合物,则该化合物的化学式是
化合生成2体积化合物,则该化合物的化学式是(5)某盐混合溶液中含有离子:
 、
、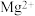 、
、 、
、 ,测得
,测得 、
、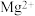 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则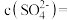
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现用质量分数为36.5%的浓盐酸(密度为1.19 g/cm3)配制1 mol/L的稀盐酸100 mL。
(1)实验中应选用的仪器是____ (填序号);
①100 mL量筒 ②托盘天平(带砝码) ③玻璃棒 ④50 mL容量瓶 ⑤10 mL量筒 ⑥50 mL烧杯 ⑦100 mL容量瓶 ⑧胶头滴管
(2)经计算,需浓盐酸的体积为____ mL;
(3)此实验中玻璃棒的作用是_________ ;
(4)某学生实际配制稀盐酸的浓度经滴定测定为 0.98 mol/L,原因可能是____ (填序号)。
①取用完浓盐酸的量筒未洗涤
②转移溶液后,小烧杯未洗涤
③定容时俯视容量瓶刻度线
④移液前容量瓶内有少量蒸馏水
(1)实验中应选用的仪器是
①100 mL量筒 ②托盘天平(带砝码) ③玻璃棒 ④50 mL容量瓶 ⑤10 mL量筒 ⑥50 mL烧杯 ⑦100 mL容量瓶 ⑧胶头滴管
(2)经计算,需浓盐酸的体积为
(3)此实验中玻璃棒的作用是
(4)某学生实际配制稀盐酸的浓度经滴定测定为 0.98 mol/L,原因可能是
①取用完浓盐酸的量筒未洗涤
②转移溶液后,小烧杯未洗涤
③定容时俯视容量瓶刻度线
④移液前容量瓶内有少量蒸馏水
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学就在我们身边,它与我们的日常生活生产密切相关,按要求回答以下问题
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的_______ 操作(填操作名称)
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的 转化为
转化为_______ 。
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成 和
和 ,其反应的离子方程式为
,其反应的离子方程式为_______ 。
(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为_______ ;漂白粉敞放在空气中会变质,其发生的化学方程式为_______ 。
(5)某同学需帮助水质检测站配制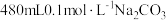 溶液以备使用。
溶液以备使用。
①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、_______ 。
②该同学应称取 固体
固体_______ g
③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度_______ (填“偏大”、“偏小”或“不变”)。
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的
 转化为
转化为(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成
 和
和 ,其反应的离子方程式为
,其反应的离子方程式为(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为
(5)某同学需帮助水质检测站配制
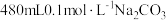 溶液以备使用。
溶液以备使用。①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、
②该同学应称取
 固体
固体③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】实验室用密度为1.25 ,质量分数为36.5%的浓盐酸配制240mL 0.1
,质量分数为36.5%的浓盐酸配制240mL 0.1 的盐酸,请回答下列问题:
的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为_______ 。
(2)配制240mL 0.1 的盐酸应量取浓盐酸体积
的盐酸应量取浓盐酸体积_______ mL。
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)_______ 。
A.用30mL水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2厘米处
(4)操作A中,将洗涤液都移入容量瓶,其目的是_______
(5)若实验过程中出现如下情况如何处理?向容量瓶中转移溶液时不慎有溶液溅出_______
 ,质量分数为36.5%的浓盐酸配制240mL 0.1
,质量分数为36.5%的浓盐酸配制240mL 0.1 的盐酸,请回答下列问题:
的盐酸,请回答下列问题:(1)浓盐酸的物质的量浓度为
(2)配制240mL 0.1
 的盐酸应量取浓盐酸体积
的盐酸应量取浓盐酸体积(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2厘米处
(4)操作A中,将洗涤液都移入容量瓶,其目的是
(5)若实验过程中出现如下情况如何处理?向容量瓶中转移溶液时不慎有溶液溅出
您最近一年使用:0次



