某化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。

按要求回答下列问题。
(1)写出A装置制取氯气的化学方程式:___________________
(2)①装置B中盛放的试剂名称为__________ ,作用是__________ 。
②装置D和E中出现的不同现象说明:_____________________ 。
③写出装置G中发生反应的离子方程式_____________________ 。
(3)实验室也可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑+8H2O
①该反应中浓盐酸体现出来的性质为____________
②氧化剂与还原剂之比是_____________
③若反应中转移了0.4mol电子,则产生的气体在标准状况下体积为_______ .

按要求回答下列问题。
(1)写出A装置制取氯气的化学方程式:
(2)①装置B中盛放的试剂名称为
②装置D和E中出现的不同现象说明:
③写出装置G中发生反应的离子方程式
(3)实验室也可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑+8H2O
①该反应中浓盐酸体现出来的性质为
②氧化剂与还原剂之比是
③若反应中转移了0.4mol电子,则产生的气体在标准状况下体积为
更新时间:2020-12-30 23:23:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现用二氧化锰与浓盐酸反应制备纯净干燥的氯气,再用氯气与铜粉反应制取少量CuCl2,其装置如下:
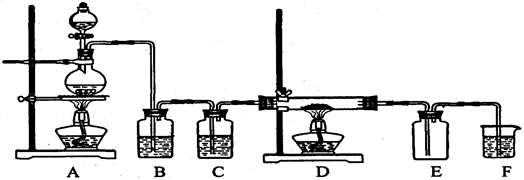
(1)写出装置A中发生反应的离子方程式_________________________ 。
(2)B中选用的试剂是饱和食盐水,其作用是除去Cl2中混有的__________ 杂质;装置E的作用是___________________ 。
(3)即使A装置中的MnO2和D装置中的Cu都是足量的,100mL 12mol/L浓盐酸经充分反应后得到的CuCl2也不足0.3mol,其原因是______________
A.装置漏气 B.A装置在加热过程中盐酸易挥发
C.CuCl2潮解吸水 D.A装置中反应生成的水要稀释盐酸,剩余的盐酸不再反应
(4)某实验小组的同学用经Cl2消毒的自来水配制下列溶液:①KI;②AgNO3;③AlCl3;④FeCl2;⑤稀盐酸,发现部分药品变质,它们是(请用序号作答)____________________ 。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_____________________________________ 。
(6)一定条件下,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
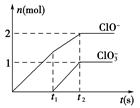
该过程中参加反应Cl2的物质的量是________ mol。若产生的n(C1-)为11mol,n(C1O3-)为2 mol,则参加反应的Ca(OH)2的物质的量为________ mol。

(1)写出装置A中发生反应的离子方程式
(2)B中选用的试剂是饱和食盐水,其作用是除去Cl2中混有的
(3)即使A装置中的MnO2和D装置中的Cu都是足量的,100mL 12mol/L浓盐酸经充分反应后得到的CuCl2也不足0.3mol,其原因是
A.装置漏气 B.A装置在加热过程中盐酸易挥发
C.CuCl2潮解吸水 D.A装置中反应生成的水要稀释盐酸,剩余的盐酸不再反应
(4)某实验小组的同学用经Cl2消毒的自来水配制下列溶液:①KI;②AgNO3;③AlCl3;④FeCl2;⑤稀盐酸,发现部分药品变质,它们是(请用序号作答)
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)
(6)一定条件下,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO
 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
该过程中参加反应Cl2的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用如图装置制备并收集干燥纯净 的Cl2。

(1)装置A中反应的化学方程式是______ 。
(2)装置B的作用是______ 。
(3)装置C中盛放的物质是______ 。
(4)装置D用于收集Cl2,请将图中装置D的导气管补充完整_____ 。
(5)装置E用于吸收尾气,E中反应的离子方程式是______ 。
(6)可用Cl2和Ca(OH)2制备漂粉精,其有效成分是_______________________ 。
(7)漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO)2 + 2H2O ⇌Ca(OH)2+2HClO
途径二:Ca(ClO)2 + H2O + CO2=___________ + ___________ (把反应补充完整)
(8)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会_____________ (填“增强”或“减弱”)。
②池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是_________________ (填离子符号)。

(1)装置A中反应的化学方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集Cl2,请将图中装置D的导气管补充完整
(5)装置E用于吸收尾气,E中反应的离子方程式是
(6)可用Cl2和Ca(OH)2制备漂粉精,其有效成分是
(7)漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO)2 + 2H2O ⇌Ca(OH)2+2HClO
途径二:Ca(ClO)2 + H2O + CO2=
(8)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会
②池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯及其化合物在工业生产生活中有很重要的作用。图中为实验室通常制取氯气及性质验证的装置图:
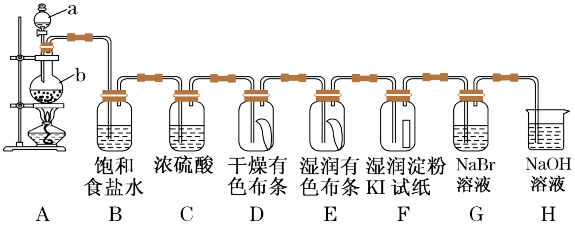
(1)H装置的作用____ ,写出发生的离子反应方程式____ 。
(2)在装置E中可观察到的现象是____ ,通过D、E中的现象说明什么结论____ 。
(3)装置G中发生的离子方程式____ 。
(4)可用KMnO4与浓盐酸快速制氯气,发生如下反应(未配平):KMnO4+HCl(浓)—KCl+Cl2↑+H2O+MnCl2。
写出配平的该反应的离子方程式_____ 。该反应中氧化剂与还原剂的物质的量之比为____ 。标况下反应生成11.2L的Cl2,则该反应转移的电子的数目为____ ;被氧化的HCl的物质的量为____ 。
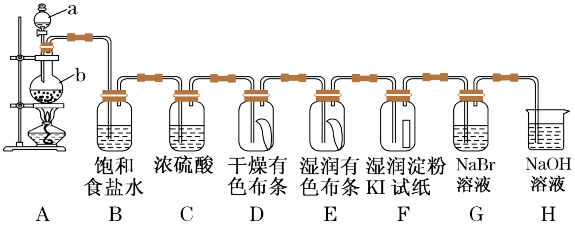
(1)H装置的作用
(2)在装置E中可观察到的现象是
(3)装置G中发生的离子方程式
(4)可用KMnO4与浓盐酸快速制氯气,发生如下反应(未配平):KMnO4+HCl(浓)—KCl+Cl2↑+H2O+MnCl2。
写出配平的该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.2019年3月1日晚,一艘外籍冷藏运输船在山东威海荣成市荣喜港装卸过程中,货舱发生液氨泄漏事故,造成5名中国籍雇员死亡。试回答下列问题:
(1)液氨能做制冷剂的原因是_________
(2)实验室制取氨气的化学方程式为________ ;
Ⅱ.液氨是否泄漏可以用氯气进行检验,某学生利用以下装置探究氯气与氨之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。
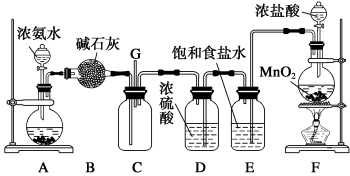
请回答下列问题:
(1)装置B中仪器的名称是_________ ;装置E的作用是 ____________ 。
(2)D中体现了浓硫酸的___________ 性。
(3)装置F中发生反应的化学方程式:_______ ,若生成标况下的氯气2.24L,则被氧化的盐酸的物质的量为__________ 。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,试写出检验液氨泄漏的化学方程式____________ 。
(1)液氨能做制冷剂的原因是
(2)实验室制取氨气的化学方程式为
Ⅱ.液氨是否泄漏可以用氯气进行检验,某学生利用以下装置探究氯气与氨之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。

请回答下列问题:
(1)装置B中仪器的名称是
(2)D中体现了浓硫酸的
(3)装置F中发生反应的化学方程式:
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,试写出检验液氨泄漏的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡与氯气反应制备SnCl4,装置如下图所示:
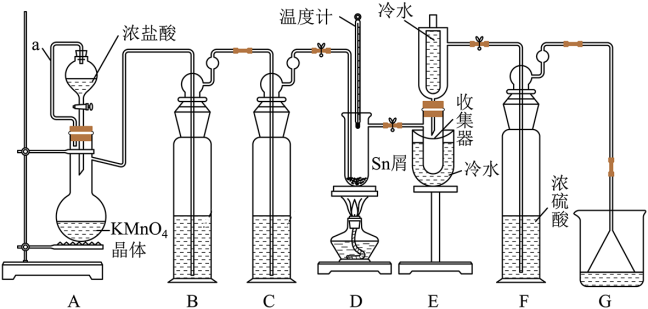
已知:①Sn、SnCl2、SnCl4有关的物理性质如下表:
②SnCl4在空气中极易水解生成SnO2•xH2O;Cl2易溶于SnCl4。
请回答下列问题:
(1)A装置中制备氯气的离子方程式是_______ 。
(2)下列关于实验装置的说法正确的是_______ 。
A.整套实验装置先检漏,再连接,再添加药品,最后检查气密性
B.A中盛放KMnO4晶体的仪器名称为圆底烧瓶
C.B中盛放饱和食盐水,C中盛放浓硫酸,G中盛放浓NaOH溶液
D.装置E中上方冷水的作用是冷凝回流SnCl4至收集器中
(3)当观察到装置F上方出现_______ 现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是_______ 。
(4)若上述装置中缺少装置C(其它均相同),则D处具支试管中发生的主要副反应的化学方程式为_______ 。
(5)收集器中收集到的液体略显黄色,原因是_______ ;F与G两个装置可用球型干燥管代替,则球型干燥管中应盛放_______ 。(填写干燥剂名称)

已知:①Sn、SnCl2、SnCl4有关的物理性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 颜色、状态 |
| Sn | 232 | 2260 | 银白色固体 |
| SnCl2 | 246 | 623 | 无色晶体 |
| SnCl4 | -30 | 114 | 无色液体 |
请回答下列问题:
(1)A装置中制备氯气的离子方程式是
(2)下列关于实验装置的说法正确的是
A.整套实验装置先检漏,再连接,再添加药品,最后检查气密性
B.A中盛放KMnO4晶体的仪器名称为圆底烧瓶
C.B中盛放饱和食盐水,C中盛放浓硫酸,G中盛放浓NaOH溶液
D.装置E中上方冷水的作用是冷凝回流SnCl4至收集器中
(3)当观察到装置F上方出现
(4)若上述装置中缺少装置C(其它均相同),则D处具支试管中发生的主要副反应的化学方程式为
(5)收集器中收集到的液体略显黄色,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酰氯(SO2Cl2)是重要的化工试剂,常作氯化剂或氯磺化剂。也可用于制作药品、染料、表面活性剂等。有关物质的性质如下表:
在实验室利用SO2和Cl2在活性炭催化作用下制取SO2Cl2,装置如图所示。



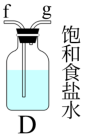
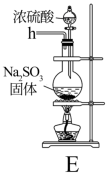
(1)实验时,A装置中发生的离子方程式___________ 。
(2)B装置中冷凝管进水口是___________ 。(填“m”或“n”),B中干燥管盛有的物质是___________ 。
(3)欲制取少量SO2Cl2,选择图中的装置(可以重复选用),其连接顺序为:a、___________ 、h。
(4)去除C装置会降低SO2和Cl2的利用率,可能的原因是___________ 。
(5)已知SO2Cl2遇水强烈水解生成两种强酸。向SO2Cl2溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是_____ 。[已知Ksp(AgCl)=1.8×10-10、Ksp(Ag2SO4)=1.2×10-5]
(6)少量硫酰氯也可由氯磺酸(ClSO3H)分解获得,该反应的化学方程式为2ClSO3H=H2SO4+SO2Cl2从分解的产物中分离初硫酰氯的操作方法是___________ 。
(7)当通入装置B中的氯气为1.12L(已转化为标准状况),最后通过蒸馏得到纯净的硫酰氯5.4g,则磺酰氯的产率为___________ 。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有___________ (填序号)。
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈瓶发烫,可适当降温 ④加热三颈瓶
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2Cl2 | -54.1 | 69.1 | 易水解 |
| H2SO4 | 10.4 | 338 |





(1)实验时,A装置中发生的离子方程式
(2)B装置中冷凝管进水口是
(3)欲制取少量SO2Cl2,选择图中的装置(可以重复选用),其连接顺序为:a、
(4)去除C装置会降低SO2和Cl2的利用率,可能的原因是
(5)已知SO2Cl2遇水强烈水解生成两种强酸。向SO2Cl2溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是
(6)少量硫酰氯也可由氯磺酸(ClSO3H)分解获得,该反应的化学方程式为2ClSO3H=H2SO4+SO2Cl2从分解的产物中分离初硫酰氯的操作方法是
(7)当通入装置B中的氯气为1.12L(已转化为标准状况),最后通过蒸馏得到纯净的硫酰氯5.4g,则磺酰氯的产率为
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈瓶发烫,可适当降温 ④加热三颈瓶
您最近一年使用:0次



