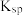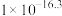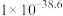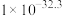硫化铋在光电、催化及储能方面有着广泛应用,还可用作新型锂离子电池的电极材料。以浮选过的辉铋矿(主要成分是Bi2S3,还含少量Fe2O3、SiO2等杂质)为原料制备高纯 Bi2S3的工艺流程如下:

已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:___________ 。
(2)“浸出”时加入盐酸,既可提高铋的浸出率,又可_____ ;滤渣1的主要成分是S和______ 。
(3) “还原”过程中发生置换反应的离子是___________ ,过量的铁粉可用___________ 除去。检验过滤后的铋粉是否洗净的方法是___________ 。
(4)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是___________ 。
(5)用Bi2S3/石墨烯复合材料、高纯锂作电极,LiPF6+EC/EMC作电解液制成的电池如图所示。放电时电池的总反应为:Bi2S3+6Li=3Li2S+2Bi,电极材料中石墨烯的作用是___________ 。放电时负极的电极反应为___________ 充电时阳极的电极反应为___________ 。


已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:
(2)“浸出”时加入盐酸,既可提高铋的浸出率,又可
(3) “还原”过程中发生置换反应的离子是
(4)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是
(5)用Bi2S3/石墨烯复合材料、高纯锂作电极,LiPF6+EC/EMC作电解液制成的电池如图所示。放电时电池的总反应为:Bi2S3+6Li=3Li2S+2Bi,电极材料中石墨烯的作用是

2021·四川绵阳·二模 查看更多[3]
四川省绵阳市2021届高三第二次诊断性测试理综化学试题 (已下线)大题02 化学工艺流程题(二)-【考前抓大题】备战2021年高考化学(全国通用)四川省眉山市彭山区第一中学2023-2024学年高三上学期开学考试理综化学试题
更新时间:2021-01-16 23:20:29
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】试根据以下信息进行判断:下列为A、B、C、D四种物质的转化关系,a、b为反应条件:

(1)若A为气态化合物,B到C转化不需要条件,则A为
(2)把某黑色固体Y加热至红热,投入到上述某种黄色溶液D中产生两种气体组成的混合气体X,将X作如下所示实验:
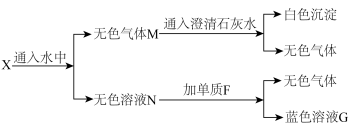
写出下列物质的化学式Y
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系图如下。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应的化学方程式:_______ 。
(3)实验室中,检验溶液中含有NH 的操作方法是
的操作方法是___________ 。
(4)请写出物质C的稀溶液与金属Cu反应的化学方程式_______ 。
(5)物质B为红棕色气体,写出该物质与水反应的离子方程式_______ 。当反应消耗3.36 L(标准状况)物质B时,转移电子的物质的量为_______ mol。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(2)在加热条件下,物质C的浓溶液与碳单质反应的化学方程式:
(3)实验室中,检验溶液中含有NH
 的操作方法是
的操作方法是(4)请写出物质C的稀溶液与金属Cu反应的化学方程式
(5)物质B为红棕色气体,写出该物质与水反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】Ⅰ.金属铝在酸性或碱性溶液中均可与 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:

已知,气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。请回答下列问题:
(1)A和B两溶液混合产生白色沉淀,反应的离子方程式为_________________________ 。
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,任意写出其中一个反应的化学方程式:_________________ 。
(3)写出铝在碱性条件下与 反应的离子方程式:
反应的离子方程式:________________ 。
(4)除去气体C中的杂质气体E的化学方法:__________________ (用化学方程式表示)。
(5)Al与 在酸性条件下反应,Al与被还原的
在酸性条件下反应,Al与被还原的 的物质的量之比是
的物质的量之比是________ 。
Ⅱ.向FeI2溶液中不断通入Cl2,溶液中I-、I2、 、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)的变化可用下图简单表示
、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)的变化可用下图简单表示

(1)当n(Cl2)∶n(FeI2)=6.5时,溶液中n(Cl-)∶n( )=
)=_____________ 。
(2)当n(Cl2)∶n(FeI2)=1.2时,离子方程式可表示为___________________ 。
 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:
已知,气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。请回答下列问题:
(1)A和B两溶液混合产生白色沉淀,反应的离子方程式为
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,任意写出其中一个反应的化学方程式:
(3)写出铝在碱性条件下与
 反应的离子方程式:
反应的离子方程式:(4)除去气体C中的杂质气体E的化学方法:
(5)Al与
 在酸性条件下反应,Al与被还原的
在酸性条件下反应,Al与被还原的 的物质的量之比是
的物质的量之比是Ⅱ.向FeI2溶液中不断通入Cl2,溶液中I-、I2、
 、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)的变化可用下图简单表示
、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)的变化可用下图简单表示
(1)当n(Cl2)∶n(FeI2)=6.5时,溶液中n(Cl-)∶n(
 )=
)=(2)当n(Cl2)∶n(FeI2)=1.2时,离子方程式可表示为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列框图中,已知A、E、F、H是单质,其中只有A是固体,其它都是气体,且H呈黄绿色;B是最常见液体,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。部分反应的某些产物未标出。
(1)写出B的化学式:______________ C的化学式:____________________ 。
(2)写出D与I溶液发生反应的离子方程式:_________________ 。
(3)写出L→M的现象是:________________________ 。
(4)从G与J反应后的混合物中得到M的操作方法叫做___________________ 。

(1)写出B的化学式:
(2)写出D与I溶液发生反应的离子方程式:
(3)写出L→M的现象是:
(4)从G与J反应后的混合物中得到M的操作方法叫做
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某废料铁泥主要成分为Fe2O3、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:
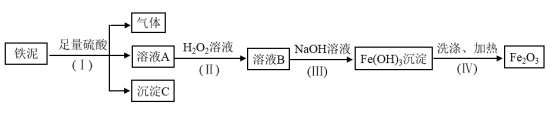
(1)写出步骤(I)中铁单质参与的有关反应的离子方程式______ 、______ ,分离溶液A和沉淀C的操作名称是______ 。
(2)检验溶液A中含有 应选用的试剂是
应选用的试剂是______
A.铁粉 B. 溶液 C.酸性
溶液 C.酸性 溶液 D.KSCN溶液
溶液 D.KSCN溶液
(3)步骤(Ⅱ)中加入 溶液,
溶液, 在反应中作
在反应中作______ (用离子反应方程式解释)。
(4)若最终获得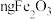 ,则铁泥中铁元素的质量分数为
,则铁泥中铁元素的质量分数为______ 。
 ,设计实验流程如下:
,设计实验流程如下:
(1)写出步骤(I)中铁单质参与的有关反应的离子方程式
(2)检验溶液A中含有
 应选用的试剂是
应选用的试剂是A.铁粉 B.
 溶液 C.酸性
溶液 C.酸性 溶液 D.KSCN溶液
溶液 D.KSCN溶液(3)步骤(Ⅱ)中加入
 溶液,
溶液, 在反应中作
在反应中作(4)若最终获得
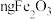 ,则铁泥中铁元素的质量分数为
,则铁泥中铁元素的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________ 。
(2)根据框图反应关系,写出下列B、C、D、E所含物质的化学式

沉淀固体B_________ ;C_________ ;沉淀D ___________ 。
(3)写出②的离子反应方程,③的化学反应方程。
②_________________________________ ;
③_________________________________ ;
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据框图反应关系,写出下列B、C、D、E所含物质的化学式

沉淀固体B
(3)写出②的离子反应方程,③的化学反应方程。
②
③
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】四氧化三锰( )广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含
)广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含 、
、 、MnOOH及少量
、MnOOH及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下:
①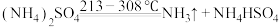
②已知:25℃时相关物质的 见表
见表
③当 时,
时, 开始溶解
开始溶解
回答下列问题:
(1)Mn元素在周期表中的______ 区,从核外电子排布的角度,稳定性Mn(Ⅱ)______ Mn(Ⅲ)(填“>”或“<”)。
(2)“溶浸”过程中, 可用
可用______ (填标号)代替,理由是______ 。
A.盐酸 B.硫酸 C.硝酸
(3)加入 调节
调节 时,杂质离子是否能完全沉淀
时,杂质离子是否能完全沉淀______ (填“是”或“否”),此时“滤渣2”的主要成分是______ 。(溶液中离子浓度 视为完全沉淀)
视为完全沉淀)
(4)“沉锰”步骤中,杂质含量直接影响 的品位,实验测得温度对
的品位,实验测得温度对 中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是
中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是______ 。“母液”中,能转换成可循环利用的物质是______ 。 是制备电池正极材料
是制备电池正极材料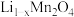 的优质原料,该电极在电池放电过程中转化为
的优质原料,该电极在电池放电过程中转化为 ,写出正极放电时的电极反应式
,写出正极放电时的电极反应式______ 。
 )广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含
)广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含 、
、 、MnOOH及少量
、MnOOH及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下: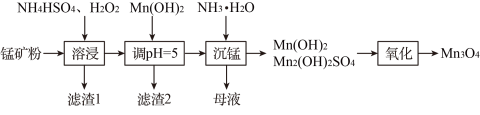
①
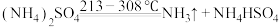
②已知:25℃时相关物质的
 见表
见表③当
 时,
时, 开始溶解
开始溶解物质 |
|
|
|
|
|
|
|
|
|
(1)Mn元素在周期表中的
(2)“溶浸”过程中,
 可用
可用A.盐酸 B.硫酸 C.硝酸
(3)加入
 调节
调节 时,杂质离子是否能完全沉淀
时,杂质离子是否能完全沉淀 视为完全沉淀)
视为完全沉淀)(4)“沉锰”步骤中,杂质含量直接影响
 的品位,实验测得温度对
的品位,实验测得温度对 中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是
中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是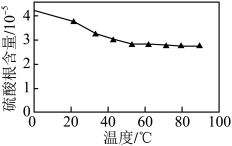
 是制备电池正极材料
是制备电池正极材料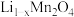 的优质原料,该电极在电池放电过程中转化为
的优质原料,该电极在电池放电过程中转化为 ,写出正极放电时的电极反应式
,写出正极放电时的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】已知25℃时 的电离常数
的电离常数 。常温下,往25mL氢氧化钠标准溶液中逐滴加入
。常温下,往25mL氢氧化钠标准溶液中逐滴加入 的
的 溶液,pH变化曲线如图所示:
溶液,pH变化曲线如图所示:_____ 。
(2)A点对应的横坐标为25mL,请用离子方程式解释A点所示的溶液显碱性的原因:_____ 。
(3)A点所示的溶液中各离子浓度由大到小的排列顺序是:_____ 。
(4)电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_____ (填字母序号)
(5)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。下图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。_____ 极(填“正”或“负”)。F电极上的电极反应式为_____ 。
(6)乙醛酸(HOOC−CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。已知乙二酸的结构简式为HOOC−COOH_____ 。
②若有 通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为_____ mol
 的电离常数
的电离常数 。常温下,往25mL氢氧化钠标准溶液中逐滴加入
。常温下,往25mL氢氧化钠标准溶液中逐滴加入 的
的 溶液,pH变化曲线如图所示:
溶液,pH变化曲线如图所示: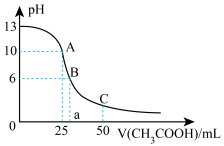
(2)A点对应的横坐标为25mL,请用离子方程式解释A点所示的溶液显碱性的原因:
(3)A点所示的溶液中各离子浓度由大到小的排列顺序是:
(4)电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

(5)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。下图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

(6)乙醛酸(HOOC−CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。已知乙二酸的结构简式为HOOC−COOH
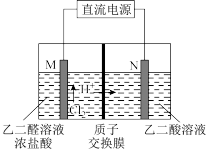
②若有
 通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲醇是一种重要的工业品,也可作燃料电池的原料。回答下列问题:
(1)CH3OH的电子式为___ ;Sn与C位于同一主族,核电荷数为50,其在元素周期表中的位置为___ 。
(2)微型直接甲醇燃料电池是通过MEMS工艺制作的一种微型能源装置,具有结构简单、体积小、质量轻、比能量密度高、环境污染小等优点,其装置如图所示:
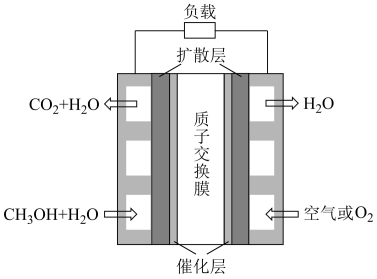
①通入CH3OH和H2O的电极为该电池的___ (填“正极”或“负极”),该电极上的电极反应式为___ 。
②电解质溶液可能为____ (填“稀H2SO4”或“KOH溶液”)。
(3)T℃时,将0.75molCO2和2.25molH2的混合气体通入体积为1L的恒容密闭容器中,在一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),5min后反应达到平衡,此时容器压强为起始压强的
CH3OH(g)+H2O(g),5min后反应达到平衡,此时容器压强为起始压强的 。
。
①平衡时,CH3OH的物质的量为___ mol。
②0~5min内,v(H2)=__ mol·L-1·min-1。
③CO2的转化率为___ 。(保留3位有效数字)
(1)CH3OH的电子式为
(2)微型直接甲醇燃料电池是通过MEMS工艺制作的一种微型能源装置,具有结构简单、体积小、质量轻、比能量密度高、环境污染小等优点,其装置如图所示:

①通入CH3OH和H2O的电极为该电池的
②电解质溶液可能为
(3)T℃时,将0.75molCO2和2.25molH2的混合气体通入体积为1L的恒容密闭容器中,在一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),5min后反应达到平衡,此时容器压强为起始压强的
CH3OH(g)+H2O(g),5min后反应达到平衡,此时容器压强为起始压强的 。
。①平衡时,CH3OH的物质的量为
②0~5min内,v(H2)=
③CO2的转化率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】工业上从海水中获得纯净氯化钠溶液经过下列流程生产焦亚硫酸钠( ,能溶于水,在空气中容易被氧化),回答下列问题:
,能溶于水,在空气中容易被氧化),回答下列问题:

(1)反应I中应该先通入___________ 。
(2)Y的主要成分是___________ 。
(3)从溶液乙中结晶的具体操作是___________ 过滤、洗涤、干燥。
(4)该流程中,___________ 可以循环使用。
(5)已知 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为______ 。焦亚硫酸钠常用作食物的抗氧化剂,在空气中容易被氧化而变质。要检验焦亚硫酸钠是否变质,具体的实验操作为_______ 。
 ,能溶于水,在空气中容易被氧化),回答下列问题:
,能溶于水,在空气中容易被氧化),回答下列问题:
(1)反应I中应该先通入
(2)Y的主要成分是
(3)从溶液乙中结晶的具体操作是
(4)该流程中,
(5)已知
 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】爱国实业家侯德榜在氨碱法的基础上,发明了“联合制碱法”,简单流程如图。完成下列问题:

(1)在饱和食盐水中通入X和Y,则X______ 和Y_______ (填物质名称),先通X后通Y的原因是_______________________ 。
(2)写出通入X和Y的化学反应方程式____________________________ 。
(3)操作Z包括________ 和________ (填名称)。
(4)溶液B中含有的主要离子是_____________ ,为了得到化肥(NH4Cl),需要在溶液B中通入NH3、冷冻、加食盐,其中通入NH3的作用一_______________________________ ,作用二_______________________________ 。
(5)工业生产的纯碱常会含少量NaCl杂质。现用重量法测定其纯度,步骤如下:
① 称取样品ag,加水溶解;
② 加入足量的BaCl2溶液;
③ 过滤、_________ 、烘干、冷却、称量、烘干、冷却、_________ ,最终得到固体bg。样品中纯碱的质量分数为___________________ (用含a、b的代数式表示)。

(1)在饱和食盐水中通入X和Y,则X
(2)写出通入X和Y的化学反应方程式
(3)操作Z包括
(4)溶液B中含有的主要离子是
(5)工业生产的纯碱常会含少量NaCl杂质。现用重量法测定其纯度,步骤如下:
① 称取样品ag,加水溶解;
② 加入足量的BaCl2溶液;
③ 过滤、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是___________ 、____________ 。
(2) 从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为__________ 、__________ 、过滤、冰水洗涤、低温干燥。
(3)在“溶解II”步骤中,发生反应的离子方程式为____________________________ 。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol·L-1Na2S2O3溶液至刚好完全反应,消耗Na2S2O3溶液25.00mL。已知:2Cu2++4I-===2CuI(白色)↓+I2, 2S2O32-+I2===2I-+S4O62-请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程)_______________________ 。

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是
(2) 从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为
(3)在“溶解II”步骤中,发生反应的离子方程式为
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol·L-1Na2S2O3溶液至刚好完全反应,消耗Na2S2O3溶液25.00mL。已知:2Cu2++4I-===2CuI(白色)↓+I2, 2S2O32-+I2===2I-+S4O62-请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程)
您最近一年使用:0次