已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E。它们之间转化关系如图所示。
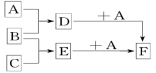
(1)写出A的化学式___________ ,B所含元素的原子结构示意图___________ ;
(2)写出D和E分别与A反应的离子方程式:
D+A:___________ ;
E+A:___________ ;
(3)写出在F中加入NaOH的产物在空气中放置所发生的反应的化学方程式___________ 。

(1)写出A的化学式
(2)写出D和E分别与A反应的离子方程式:
D+A:
E+A:
(3)写出在F中加入NaOH的产物在空气中放置所发生的反应的化学方程式
更新时间:2021-01-07 14:53:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】I.固体A是一种二元化合物,会发生如下的转化(注: C是空气的主要组成成分):
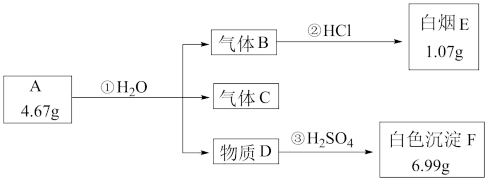
(1)写出C的结构式:___________ ;
(2)写出①的化学反应方程式:___________ 。
(3)设计实验方案检验E中的阳离子:___________ 。
II.某兴趣小组为探究有关物质的反应,按下图装置进行实验,实验中观察到试管内充满了红棕色气体且有深红棕色油状液体生成。请回答:

(1)蒸馏烧瓶中生成红棕色物质的反应化学方程式为___________ 。
(2)本实验要用倒挂的三角漏斗防倒吸的原因是___________ 。

(1)写出C的结构式:
(2)写出①的化学反应方程式:
(3)设计实验方案检验E中的阳离子:
II.某兴趣小组为探究有关物质的反应,按下图装置进行实验,实验中观察到试管内充满了红棕色气体且有深红棕色油状液体生成。请回答:

(1)蒸馏烧瓶中生成红棕色物质的反应化学方程式为
(2)本实验要用倒挂的三角漏斗防倒吸的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去)。

(1)若A是能使湿润红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体。
①C的电子式为______________ 。
②写出反应Ⅰ的化学方程式____________________________ 。
③写出反应Ⅱ的化学方程式_______________________________ 。
(2)若A是淡黄色化合物;常温下D是无色气体;C中含有的阴、阳离子均为10电子粒子。
①D的结构式为____________ ,C中所含化学键的类型是____________________ 。
②写出反应Ⅰ的化学方程式__________________________ 。
③写出反应Ⅱ的化学方程式_________________________ 。
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。

①O点溶液中所含溶质的化学式为__________ ,常温下a点溶液的pH________ (填“>”、“=”或“<”)7,a点溶液中各离子浓度由大到小的关系是________________________ 。
②标况下,通入气体D的体积为__________ L,C溶液的物质的量浓度为________ mol·L-1。

(1)若A是能使湿润红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体。
①C的电子式为
②写出反应Ⅰ的化学方程式
③写出反应Ⅱ的化学方程式
(2)若A是淡黄色化合物;常温下D是无色气体;C中含有的阴、阳离子均为10电子粒子。
①D的结构式为
②写出反应Ⅰ的化学方程式
③写出反应Ⅱ的化学方程式
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。

①O点溶液中所含溶质的化学式为
②标况下,通入气体D的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】甲、乙同学对Fe及其化合物的相关性质与用途进行探究。
(1)实验I:甲、乙两同学分别用下图装置进行Fe粉与水蒸气反应的实验。
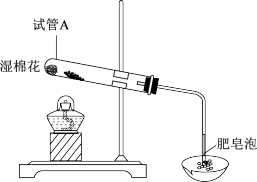
①证明生成的气体是氢气,依据的现象是_______ 。
②该反应的化学方程式是_______ 。
(2)实验II:甲、乙同学分别对各自实验I反应后的黑色固体进行研究。冷却取试管A中冷却后的固体加入过量稀HCl,充分反应后将溶液分成两份(如图)。请将下表中的现象或结论补充完整。
已知: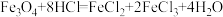
(1)实验I:甲、乙两同学分别用下图装置进行Fe粉与水蒸气反应的实验。

①证明生成的气体是氢气,依据的现象是
②该反应的化学方程式是
(2)实验II:甲、乙同学分别对各自实验I反应后的黑色固体进行研究。冷却取试管A中冷却后的固体加入过量稀HCl,充分反应后将溶液分成两份(如图)。请将下表中的现象或结论补充完整。
已知:
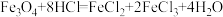
| 操作过程 | 现象及结论 | |
| 甲同学 | 乙同学 | |
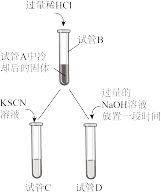 | 试管B中固体全部溶解,得到溶液M | 试管B固体全部溶解,同时有大量气泡产生,得到溶液N |
| 试管C溶液变红 | 试管C溶液没有变红,用离子方程式解释原因② | |
| 试管D开始有红褐色和灰绿色沉淀生成,最终全部变为红褐色。则溶液M中存在的阳离子有① | 试管D实验现象是③ 产生该现象发生的氧化还原反应的化学方程式是④ | |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】常温下D、E、F、I、J为气体,H、I、J都为氧化物;C的焰色反应为黄色;M为红褐色的固体,由G分解得到的H、I、J三者的物质的量相等.下图表示各物质之间的转化关系.
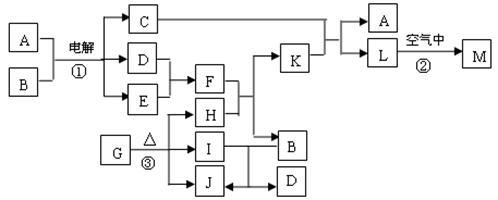
试回答下列问题:
(1)写出L的化学式____________ .
(2)基于反应①原理的化学工业称为______________ .
写出该反应①的离子方程式__________________________________________ .
(3)反应②的现象是__________________________________________ .
(4)写出H与Al在高温下反应的化学方程式___________________________________ .
(5)写出反应③的化学方程式___________________________________ .

试回答下列问题:
(1)写出L的化学式
(2)基于反应①原理的化学工业称为
写出该反应①的离子方程式
(3)反应②的现象是
(4)写出H与Al在高温下反应的化学方程式
(5)写出反应③的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下列物质均为常见物质或它们的溶液,其中A为淡黄色固体,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱.根据它们之间的转化关系(如图),用化学用语回答问题。(部分产物已省略)
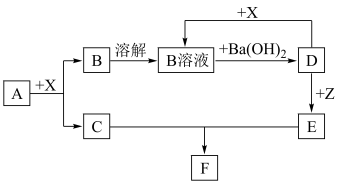
(1)写出下列物质的化学式:A____ D ____ 。
(2)物质E转化为物质F的现象为____ ,化学方程式为 ____ 。
(3)写出向B溶液中通入X气体的离子方程式_________________________ 。
(4)电子工业上,常使用向Z溶液中通入一定量的Cl2后所得溶液来刻蚀印刷电路板铜箔,写出刻蚀印刷电路板铜箔的离子方程式_________________________________ 。
(5)向含10gD的溶液中通入一定里的X,完全反应后,在低温条件下蒸发结晶,最终得到14.8g固体。所得固体中含有的物质及其物质的量之比为____ 。 (表达示例:n(A)︰n(B)=a︰b);简述蒸发结晶在低温条件下进行的理由: ____ (用必要文字回答)。

(1)写出下列物质的化学式:A
(2)物质E转化为物质F的现象为
(3)写出向B溶液中通入X气体的离子方程式
(4)电子工业上,常使用向Z溶液中通入一定量的Cl2后所得溶液来刻蚀印刷电路板铜箔,写出刻蚀印刷电路板铜箔的离子方程式
(5)向含10gD的溶液中通入一定里的X,完全反应后,在低温条件下蒸发结晶,最终得到14.8g固体。所得固体中含有的物质及其物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸亚铁铵【(NH4)2Fe(SO4)2·6H2O】,化学名称又名铁铵钒,也称摩尔盐,它是一种浅绿色的单斜晶体,它在空气中比一般的亚铁盐稳定,不易被氧化,易溶于水,工业上常用作废水处理的混凝剂,在定量分析中用作标定重铬酸钾、高锰酸钾等溶液。以硫铁矿(主要成分是FeS2,含少量Al2O3、SiO2和Fe3O4)为原料制备摩尔盐的流程如图:

反应的原理:FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2·6H2O,根据原理回答下列问题
(1)为使硫铁矿充分焙烧,可采取的措施___________ (答出一点即可),滤渣1的主要成分是___________ ,
(2)焙烧过程中可将FeS2转化为Fe2O3,反应的方程式___________ 焙烧过程中产生SO2,用过量的氨水吸收SO2的离子方程式为___________ 。
(3) “除杂”加入的试剂为___________ (写出一个即可)“除杂”的原理:___________ (用离子方程式表示)
(4)已知三种盐的溶解度:
则从溶液中得到摩尔盐【(NH4)2Fe(SO4)2·6H2O】,要经过___________ 、___________ 、过滤、洗涤、干燥一系列步骤,其中用乙醇进行洗涤的优点___________ (至少答出两点)
(5)用(NH4)2Fe(SO4)2·6H2O配置溶液时,需要加入少量的___________ ,目的是___________
(6)已知Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=___________ 。

反应的原理:FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2·6H2O,根据原理回答下列问题
(1)为使硫铁矿充分焙烧,可采取的措施
(2)焙烧过程中可将FeS2转化为Fe2O3,反应的方程式
(3) “除杂”加入的试剂为
(4)已知三种盐的溶解度:
| 温度 | FeSO4 | (NH4)2SO4 | (NH4)2Fe(SO4)2 6H2O 6H2O |
| 10 | 20.0 | 73.0 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78.0 | 28.1 |
(5)用(NH4)2Fe(SO4)2·6H2O配置溶液时,需要加入少量的
(6)已知Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A为淡黄色固体,T、R 为两种常见的用途广泛的金属单质,D具有磁性的黑色晶体,C是无色无味的气体,M为红褐色固体。回答相关问题

(1)写出D的化学式:____________
(2)写出A的电子式:_____________
(3)H在潮湿空气中变为M的现象是:______________ 化学方程式为: ________________
(4)B与R反应的化学方程式为:__________________________
(5)向沸水中加入W饱和溶液,可制得一种红褐色透明液体,区别该液体和溶液W的简单实验方法是____________________

(1)写出D的化学式:
(2)写出A的电子式:
(3)H在潮湿空气中变为M的现象是:
(4)B与R反应的化学方程式为:
(5)向沸水中加入W饱和溶液,可制得一种红褐色透明液体,区别该液体和溶液W的简单实验方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】框图所示的转化关系中,A、C均为常见的金属单质,A、C在冷的H的浓溶液中均会发生钝化;E为固体非金属单质。B为红色固体氧化物,X为常见的无色液体。L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)

请回答以下问题:
(1)含碳量在0.03 %~2 %之间的C的合金,是目前世界上使用量最大的合金,这种合金是_______ ;
A.铝合金 B.青铜 C.镁合金 D.钢铁
(2)F的化学式为_______ ;
(3)I与氯气反应的离子方程式为_______ ;
(4)A与B生成C和D的反应是_______ (填“放出”或“吸收”)大量热量的反应;
(5)D与L反应的离子方程式为_______ 。

请回答以下问题:
(1)含碳量在0.03 %~2 %之间的C的合金,是目前世界上使用量最大的合金,这种合金是
A.铝合金 B.青铜 C.镁合金 D.钢铁
(2)F的化学式为
(3)I与氯气反应的离子方程式为
(4)A与B生成C和D的反应是
(5)D与L反应的离子方程式为
您最近一年使用:0次




