通过Al2O3+N2+3C 2AlN+3CO可制得陶瓷材料AlN,下列说法正确的是
2AlN+3CO可制得陶瓷材料AlN,下列说法正确的是
 2AlN+3CO可制得陶瓷材料AlN,下列说法正确的是
2AlN+3CO可制得陶瓷材料AlN,下列说法正确的是| A.AlN既是氧化产物也是还原产物 | B.每生成 3.36 L CO,转移 0.3 mol 电子 |
| C.氧化剂与还原剂的物质的量之比为 1:3 | D.14N2和12C18O所含中子数相等 |
更新时间:2021-01-19 07:53:50
|
相似题推荐
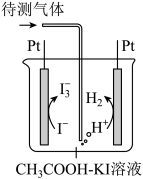
【推荐1】库仑滴定法是常用的快捷检测煤中全硫含量的方法。其方法为将煤中的硫元素在催化剂作用下转化为 ,再将
,再将 通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中
通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解到
还原,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法不正确 的是
 ,再将
,再将 通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中
通入库仑测硫仪中,库仑测硫仪中电解原理示意图如图所示,检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解到
还原,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量,下列说法
A. 在电解池中发生反应的离子方程式为 在电解池中发生反应的离子方程式为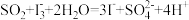 |
B.测硫仪工作时电解池的阳极反应式为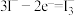 |
C.煤样为 ,电解消耗的电量为 ,电解消耗的电量为 库仑,煤样中硫的质量分数为 库仑,煤样中硫的质量分数为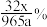 (已知:电解中转移 (已知:电解中转移 电子所消耗的电量为96500库仑) 电子所消耗的电量为96500库仑) |
D.煤中硫元素在催化剂作用下会有少量 产生,使测得的全硫含量偏小 产生,使测得的全硫含量偏小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用H2还原某+n价的金属氧化物,如有1克H2恰好还原a克氧化物时,则该金属的相对原子质量(原子量)为 ( )
| A.(8-a)n | B.(a-8)n | C.an+8n | D.an+16n |
您最近半年使用:0次
【推荐1】 催化除去HCHO的机理如图所示。下列说法正确的是
催化除去HCHO的机理如图所示。下列说法正确的是
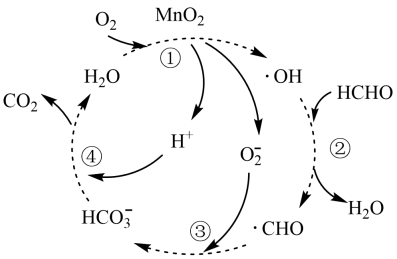
 催化除去HCHO的机理如图所示。下列说法正确的是
催化除去HCHO的机理如图所示。下列说法正确的是
A. 降低了反应的焓变 降低了反应的焓变 |
| B.反应②中断裂C—H键 |
| C.反应①~④均是氧化还原反应 |
| D.上述机理中,反应物和产物只含σ键,不含π键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列变化需要加入还原剂才能实现的是
| A.Cl2→NaClO | B.HCl→Cl2 | C.H2SO4(浓) →SO2 | D.Na2SO3→SO2 |
您最近半年使用:0次
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4
下列有关说法不正确的是:
下列有关说法不正确的是:
| A.高铁酸钾与水反应时,水发生还原反应 |
| B.湿法中每生成1molNa2FeO4转移3mol电子 |
| C.干法中每生成1molNa2FeO4转移4mol电子 |
| D.K2FeO4处理水时,不仅能消毒杀菌,还能除去H2S、NH3等,并使悬浮杂质沉降 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某元素R的阴离子Rn-,其核外共有y个电子,该元素的原子的质量数为A,则该元素的核内中子数为
| A.A-y-n | B.A+y-n | C.A+y+n | D.A-y+n |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用中子轰击 X原子产生α粒子(即氦核
X原子产生α粒子(即氦核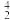 He)的核反应为
He)的核反应为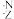 X+
X+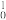
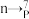 Y+
Y+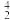 He。已知元素Y在化合物中显+1价。下列说法正确的是
He。已知元素Y在化合物中显+1价。下列说法正确的是
 X原子产生α粒子(即氦核
X原子产生α粒子(即氦核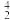 He)的核反应为
He)的核反应为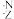 X+
X+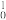
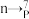 Y+
Y+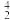 He。已知元素Y在化合物中显+1价。下列说法正确的是
He。已知元素Y在化合物中显+1价。下列说法正确的是| A.Y不能在氮气中燃烧 |
| B.XF3分子的空间结构为三角锥形 |
| C.H3XO3可用于中和溅在皮肤上的NaOH溶液 |
D. X的相对原子质量为10 X的相对原子质量为10 |
您最近半年使用:0次


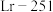 ,熔合反应为
,熔合反应为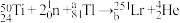 。下列叙述正确的是
。下列叙述正确的是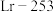 的物理性质完全相同
的物理性质完全相同

