如图是原电池电解池的组合装置图。
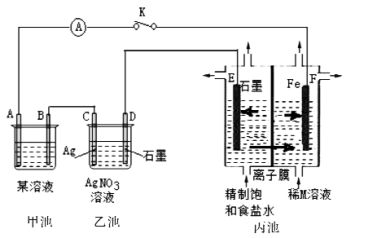
请回答:
(1)若甲池某溶液为稀H2SO4,闭合K时,电流表指针发生偏转,电极材料A为Fe,B为碳棒。则:
①甲池为______ (填“原电池”或“电解池”);B电极上发生的现象为______ 。
②乙池中的银电极上的电极反应式为______ 。
③丙池中E电极为______ (填“正极”、“负极”、“阴极”或“阳极”);闭合K一段时间后,稀M溶液的浓度会增加,则M溶液中的溶质是______ (填化学式);丙池中的离子膜为______ (填“阳离子交换膜”或“阴离子交换膜”)
(2)若将甲池的某溶液改为FeCl3,电极材料A为Cu、B为碳棒,则甲池的总反应的离子方程式为______ 。
(3)若甲池为氢氧燃料电池,某溶液为KOH溶液,A极通入氢气。则:
①A电极的反应方程式为______ 。
②若线路中转移0.02mol电子,乙池中D极质量变化______ g。
③二氧化氯(ClO2)为黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出也能用丙池装置制取二氧化氯。写出生成二氧化氯的电极反应式为______ 。

请回答:
(1)若甲池某溶液为稀H2SO4,闭合K时,电流表指针发生偏转,电极材料A为Fe,B为碳棒。则:
①甲池为
②乙池中的银电极上的电极反应式为
③丙池中E电极为
(2)若将甲池的某溶液改为FeCl3,电极材料A为Cu、B为碳棒,则甲池的总反应的离子方程式为
(3)若甲池为氢氧燃料电池,某溶液为KOH溶液,A极通入氢气。则:
①A电极的反应方程式为
②若线路中转移0.02mol电子,乙池中D极质量变化
③二氧化氯(ClO2)为黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出也能用丙池装置制取二氧化氯。写出生成二氧化氯的电极反应式为
更新时间:2021-01-28 16:54:44
|
相似题推荐
【推荐1】如图是一个化学过程的示意图
(1)图中甲池是_______ 装置(填“电解池”或“原电池”),其中 移向极
移向极_______ (填“ ”或“
”或“ ”)。
”)。
(2)写出通入 的电极的电极反应式:
的电极的电极反应式:_______ 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为_______ 极(填“A”或“B”),并写出此电极的反应式:_______
(4)乙池中总反应的离子方程式_______ 。
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的氢离子浓度是_______ (若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是_______
A. B.
B. C.NaCl D.
C.NaCl D.

(1)图中甲池是
 移向极
移向极 ”或“
”或“ ”)。
”)。(2)写出通入
 的电极的电极反应式:
的电极的电极反应式:(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为
(4)乙池中总反应的离子方程式
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的氢离子浓度是
A.
 B.
B. C.NaCl D.
C.NaCl D.
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以接用作燃料。
已知:
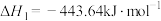
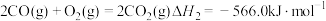
(1)试写出CH3OH(l)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式:___________ 。
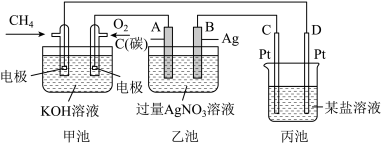
(2)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:
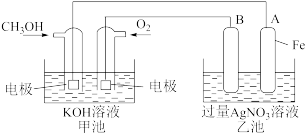
①放电时,甲醇在___________ (填“正”或“负”)极发生反应,正极的电极反应为___________
②工作时,B极的电极反应式为___________ ,A极的电极反应式为___________
(3)某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。

已知:

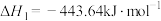
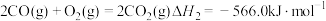
(1)试写出CH3OH(l)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式:
(2)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

①放电时,甲醇在
②工作时,B极的电极反应式为
(3)某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。

| A.a为电源正极,b为电源负极 |
| B.可以用NaCl溶液作为电解质溶液 |
| C.A、B两端都必须用铁作电极 |
D.阴极发生的反应为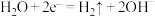 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是一个电化学原理的示意图。填写下列空白:
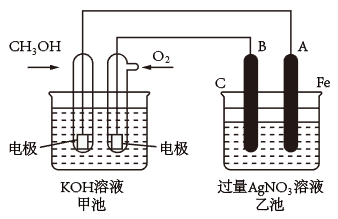
(1)请写出甲、乙两池的名称。甲池是_______ ,乙池是_______ 。
(2)甲池中通入 的电极名称是
的电极名称是_______ ,电极反应方程式为_______ ;乙池中 (石墨)电极的名称是
(石墨)电极的名称是_______ 。
(3)电解过程中,乙池溶液 的变化为(“升高”“降低”或“不变”)
的变化为(“升高”“降低”或“不变”)_______ 。
(4)当乙池中 极的质量增加
极的质量增加 时,甲池中理论上消耗
时,甲池中理论上消耗
_______  (标准状况下)。
(标准状况下)。
(5)若乙池中的 换成一定量
换成一定量 溶液,通电一段时间后,向所得的溶液中加入
溶液,通电一段时间后,向所得的溶液中加入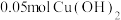 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和 ,则电解过程中转移的电子数为
,则电解过程中转移的电子数为_______  (忽略溶液体积的变化)。
(忽略溶液体积的变化)。

(1)请写出甲、乙两池的名称。甲池是
(2)甲池中通入
 的电极名称是
的电极名称是 (石墨)电极的名称是
(石墨)电极的名称是(3)电解过程中,乙池溶液
 的变化为(“升高”“降低”或“不变”)
的变化为(“升高”“降低”或“不变”)(4)当乙池中
 极的质量增加
极的质量增加 时,甲池中理论上消耗
时,甲池中理论上消耗
 (标准状况下)。
(标准状况下)。(5)若乙池中的
 换成一定量
换成一定量 溶液,通电一段时间后,向所得的溶液中加入
溶液,通电一段时间后,向所得的溶液中加入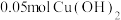 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和 ,则电解过程中转移的电子数为
,则电解过程中转移的电子数为 (忽略溶液体积的变化)。
(忽略溶液体积的变化)。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】科学家舍勒和戴维对氯气的制取和研究做出了重大贡献。根据所学知识,回答下列问题:
(1)下图中仪器a的名称是___________ , 的最佳收集装置是
的最佳收集装置是___________ (填标号)。
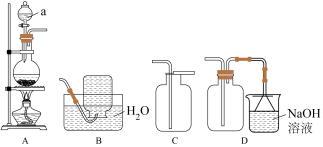
(2)实验室常用 和浓盐酸制取氯气,写出反应的化学方程式:
和浓盐酸制取氯气,写出反应的化学方程式:___________ 。
(3)工业上常用电解饱和食盐水的方法制备氯气,同时负极有氢气和氢氧化钠生成,其装置如图。
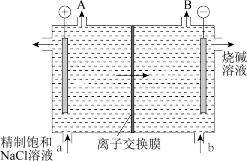
①工业上电解饱和食盐水制备 ,反应的离子方程式为
,反应的离子方程式为___________ 。
②阳离子交换膜只能通过阳离子和 ,阴离子交换膜只能通过阴离子和
,阴离子交换膜只能通过阴离子和 ,则图示中应选择
,则图示中应选择___________ (填“阳”或“阴”)离子交换膜,A口可收集到的气体为___________ (填化学式)。
③若不使用离子交换膜,则可制得消毒液,该消毒液的有效成分为___________ (填化学式)。
④若用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加NaOH溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是___________ (填标号)。
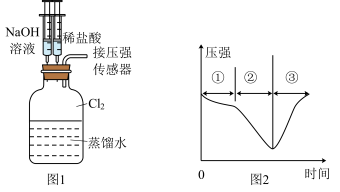
A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段②的压强变小,该过程发生了氧化还原反应
C.阶段③可能存在的化学反应为
D.若将 换成
换成 ,所得的压强变化趋势与图2相似
,所得的压强变化趋势与图2相似
(1)下图中仪器a的名称是
 的最佳收集装置是
的最佳收集装置是
(2)实验室常用
 和浓盐酸制取氯气,写出反应的化学方程式:
和浓盐酸制取氯气,写出反应的化学方程式:(3)工业上常用电解饱和食盐水的方法制备氯气,同时负极有氢气和氢氧化钠生成,其装置如图。

①工业上电解饱和食盐水制备
 ,反应的离子方程式为
,反应的离子方程式为②阳离子交换膜只能通过阳离子和
 ,阴离子交换膜只能通过阴离子和
,阴离子交换膜只能通过阴离子和 ,则图示中应选择
,则图示中应选择③若不使用离子交换膜,则可制得消毒液,该消毒液的有效成分为
④若用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加NaOH溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是
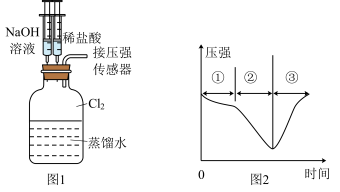
A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段②的压强变小,该过程发生了氧化还原反应
C.阶段③可能存在的化学反应为

D.若将
 换成
换成 ,所得的压强变化趋势与图2相似
,所得的压强变化趋势与图2相似
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】中国科学院提出的“液态阳光”项目为碳中和目标的达成进行积极探索,将工业生产过程中排放的 转化为
转化为 的研究取得初步成果。按要求回答下列问题。
的研究取得初步成果。按要求回答下列问题。
(1)实现该转化如图所示反应的能量变化。
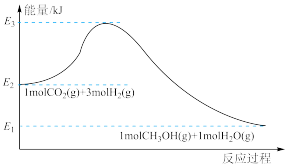
①写出该图示反应的热化学方程式:________________ ;
②若使用催化剂,反应的活化能E________  。
。
③判断该反应在________ (填“高温”“低温”或“任何温度”)条件下可自发进行。
④在恒容条件下,下列措施能加快该反应速率的是________ ;能提高 转化率的是
转化率的是________ 。
A.降温 B.减压 C.增加 投料量 D.将
投料量 D.将 及时液化
及时液化
⑤在一恒温恒容的密闭容器中,该可逆反应达到平衡的标志是________ (填字母)。
A.容器内压强不随时间变化 B.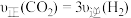
C.容器内各物质的浓度相等 D.混合气体的密度不再改变
(2)实现该转化所需高纯 的来源是目前的研究热点。利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
的来源是目前的研究热点。利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。
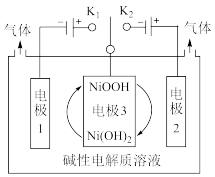
①图示装置的能量转化方式是________________ 。
②制 时,控制开关应连接
时,控制开关应连接________ (填“ ”或“
”或“ ”)。产生
”)。产生 的电极反应式是
的电极反应式是________________ 。
③改变开关连接方式,可得 的电极为
的电极为________ (填“阳极”或“阴极”)。此时电极3的电极反应式是________________ 。
 转化为
转化为 的研究取得初步成果。按要求回答下列问题。
的研究取得初步成果。按要求回答下列问题。(1)实现该转化如图所示反应的能量变化。

①写出该图示反应的热化学方程式:
②若使用催化剂,反应的活化能E
 。
。③判断该反应在
④在恒容条件下,下列措施能加快该反应速率的是
 转化率的是
转化率的是A.降温 B.减压 C.增加
 投料量 D.将
投料量 D.将 及时液化
及时液化⑤在一恒温恒容的密闭容器中,该可逆反应达到平衡的标志是
A.容器内压强不随时间变化 B.
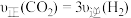
C.容器内各物质的浓度相等 D.混合气体的密度不再改变
(2)实现该转化所需高纯
 的来源是目前的研究热点。利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
的来源是目前的研究热点。利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。
①图示装置的能量转化方式是
②制
 时,控制开关应连接
时,控制开关应连接 ”或“
”或“ ”)。产生
”)。产生 的电极反应式是
的电极反应式是③改变开关连接方式,可得
 的电极为
的电极为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】我国力争实现2030年前碳达峰、2060年前碳中和的目标,研究碳的化合物对减少 在大气中累积及实现可再生能源的有效利用具有重要意义。
在大气中累积及实现可再生能源的有效利用具有重要意义。
(1)已知 和
和 在一定条件下能发生反应
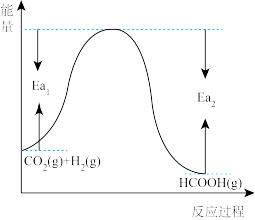
在一定条件下能发生反应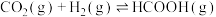 ,反应物与生成物的能量与活化能的关系如图所示,该反应的
,反应物与生成物的能量与活化能的关系如图所示,该反应的
______ kJ/mol(用含 和
和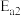 的代数式表示)。
的代数式表示)。
(2)恒温恒容条件下,为了提高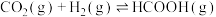 反应中
反应中 的平衡转化率,可采取的措施为
的平衡转化率,可采取的措施为______ (任写一项)。
(3)下列能说反应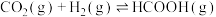 达到平衡状态的是______(填字母)。
达到平衡状态的是______(填字母)。
(4)一定温度下,在一刚性密闭容器中,充入等物质的量的 和
和 此时容器的压强为48kPa,发生反应
此时容器的压强为48kPa,发生反应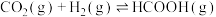 ,6min时达到平衡,此时容器压强为36kPa,则0~6min内用
,6min时达到平衡,此时容器压强为36kPa,则0~6min内用 分压表示的化学反应速率为
分压表示的化学反应速率为______ kPa/min。相同温度下,该反应的逆反应平衡常数
______ kPa( 是平衡分压代替平衡浓度计算的平衡常数)。
是平衡分压代替平衡浓度计算的平衡常数)。
(5)除合成甲酸(HCOOH)外,有科学家以 、
、 为原料合成
为原料合成 达到有效降低空气中二氧化碳含量的目的,其中涉及的主要反应如下:
达到有效降低空气中二氧化碳含量的目的,其中涉及的主要反应如下:
Ⅰ.
 kJ⋅mol
kJ⋅mol
Ⅱ.
 kJ⋅mol
kJ⋅mol
不同条件下,按照 投料,
投料, 的平衡转化率如图所示:
的平衡转化率如图所示:

压强 、
、 、
、 由小到大的顺序是
由小到大的顺序是______ 。压强为 时,温度高于300℃后,
时,温度高于300℃后, 的平衡转化率随温度升高而升高的原因是
的平衡转化率随温度升高而升高的原因是________________________ 。
(6)近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示:
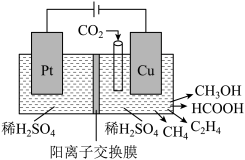
请写出Cu电极上产生 的电极反应式
的电极反应式______ 。
 在大气中累积及实现可再生能源的有效利用具有重要意义。
在大气中累积及实现可再生能源的有效利用具有重要意义。(1)已知
 和
和 在一定条件下能发生反应
在一定条件下能发生反应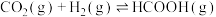 ,反应物与生成物的能量与活化能的关系如图所示,该反应的
,反应物与生成物的能量与活化能的关系如图所示,该反应的
 和
和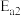 的代数式表示)。
的代数式表示)。
(2)恒温恒容条件下,为了提高
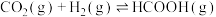 反应中
反应中 的平衡转化率,可采取的措施为
的平衡转化率,可采取的措施为(3)下列能说反应
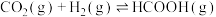 达到平衡状态的是______(填字母)。
达到平衡状态的是______(填字母)。A.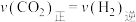 | B.HCOOH的体积分数不再变化 |
| C.混合气体的密度不再变化 | D. |
(4)一定温度下,在一刚性密闭容器中,充入等物质的量的
 和
和 此时容器的压强为48kPa,发生反应
此时容器的压强为48kPa,发生反应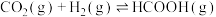 ,6min时达到平衡,此时容器压强为36kPa,则0~6min内用
,6min时达到平衡,此时容器压强为36kPa,则0~6min内用 分压表示的化学反应速率为
分压表示的化学反应速率为
 是平衡分压代替平衡浓度计算的平衡常数)。
是平衡分压代替平衡浓度计算的平衡常数)。(5)除合成甲酸(HCOOH)外,有科学家以
 、
、 为原料合成
为原料合成 达到有效降低空气中二氧化碳含量的目的,其中涉及的主要反应如下:
达到有效降低空气中二氧化碳含量的目的,其中涉及的主要反应如下:Ⅰ.

 kJ⋅mol
kJ⋅mol
Ⅱ.

 kJ⋅mol
kJ⋅mol
不同条件下,按照
 投料,
投料, 的平衡转化率如图所示:
的平衡转化率如图所示:
压强
 、
、 、
、 由小到大的顺序是
由小到大的顺序是 时,温度高于300℃后,
时,温度高于300℃后, 的平衡转化率随温度升高而升高的原因是
的平衡转化率随温度升高而升高的原因是(6)近年来,有研究人员用
 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示:
请写出Cu电极上产生
 的电极反应式
的电极反应式
您最近一年使用:0次



