如图是一个电化学原理的示意图。填写下列空白:
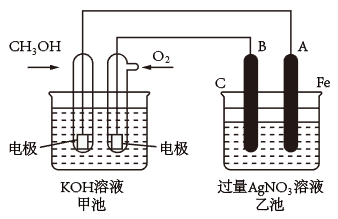
(1)请写出甲、乙两池的名称。甲池是_______ ,乙池是_______ 。
(2)甲池中通入 的电极名称是
的电极名称是_______ ,电极反应方程式为_______ ;乙池中 (石墨)电极的名称是
(石墨)电极的名称是_______ 。
(3)电解过程中,乙池溶液 的变化为(“升高”“降低”或“不变”)
的变化为(“升高”“降低”或“不变”)_______ 。
(4)当乙池中 极的质量增加
极的质量增加 时,甲池中理论上消耗
时,甲池中理论上消耗
_______  (标准状况下)。
(标准状况下)。
(5)若乙池中的 换成一定量
换成一定量 溶液,通电一段时间后,向所得的溶液中加入
溶液,通电一段时间后,向所得的溶液中加入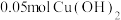 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和 ,则电解过程中转移的电子数为
,则电解过程中转移的电子数为_______  (忽略溶液体积的变化)。
(忽略溶液体积的变化)。

(1)请写出甲、乙两池的名称。甲池是
(2)甲池中通入
 的电极名称是
的电极名称是 (石墨)电极的名称是
(石墨)电极的名称是(3)电解过程中,乙池溶液
 的变化为(“升高”“降低”或“不变”)
的变化为(“升高”“降低”或“不变”)(4)当乙池中
 极的质量增加
极的质量增加 时,甲池中理论上消耗
时,甲池中理论上消耗
 (标准状况下)。
(标准状况下)。(5)若乙池中的
 换成一定量
换成一定量 溶液,通电一段时间后,向所得的溶液中加入
溶液,通电一段时间后,向所得的溶液中加入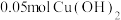 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和 ,则电解过程中转移的电子数为
,则电解过程中转移的电子数为 (忽略溶液体积的变化)。
(忽略溶液体积的变化)。
21-22高二上·黑龙江哈尔滨·开学考试 查看更多[5]
河北省石家庄元氏县第四中学2021-2022学年高二上学期期中考试化学试题湖南省长沙市宁乡市2021-2022学年高二上学期期末调研考试化学试题(已下线)选择性必修1 综合检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)湖北省罗田县第一中学2021-2022学年高二上学期9月月考化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题
更新时间:2021-09-04 10:38:29
|
【知识点】 原电池、电解池综合考查解读
相似题推荐
【推荐1】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制品的主要原料。
(1)已知多晶硅第三代工业制取流程如图所示。
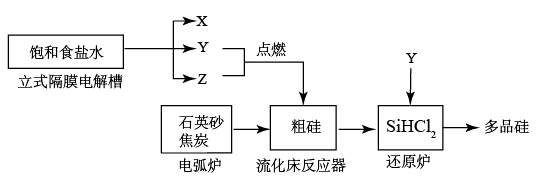
①物质Z的名称是_______ 。
②用石英砂和焦在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为_______
③在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和_______ 。
(2)利用晶体硅的粉末与干燥的氮气在1300~1400℃下反应,可制取结构陶瓷材料氮化硅(Si3N4)。现用如图所示装置(部分仪器已省略)制取少量氮化硅。
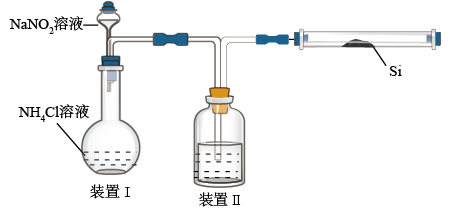
①装置II中所盛试剂为_______ 。
②装置I和装置皿均需要加热,实验中应先_______ (填“皿”或“I”)的热源。
(3)由晶体硅制成的n型半导体、p型半导体可用于太阳能电池。一种太阳能储能电池的工作原理如图所示,已知锂离子电池的总反应为:Li1-xNiO2+xLiC6 LiNiO2+xC6。完成下列问题。
LiNiO2+xC6。完成下列问题。
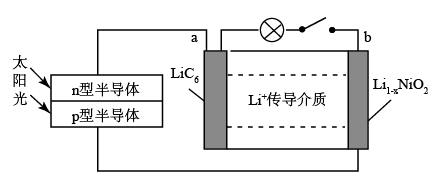
①该锂离子电池充电时,n型半导体作为电源_______ .(填“正”或“负”)极。
②该锂离子电池放电时,b极上的电极反应式为_______ 。
(1)已知多晶硅第三代工业制取流程如图所示。

| 发生的主要反应 | |
| 电弧炉 | SiO2+2C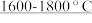 Si+CO↑ Si+CO↑ |
| 流化床反应器 | Si+3HCl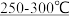 SiHCl3+H2 SiHCl3+H2 |
②用石英砂和焦在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为
③在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |

①装置II中所盛试剂为
②装置I和装置皿均需要加热,实验中应先
(3)由晶体硅制成的n型半导体、p型半导体可用于太阳能电池。一种太阳能储能电池的工作原理如图所示,已知锂离子电池的总反应为:Li1-xNiO2+xLiC6
 LiNiO2+xC6。完成下列问题。
LiNiO2+xC6。完成下列问题。
①该锂离子电池充电时,n型半导体作为电源
②该锂离子电池放电时,b极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子交换膜只允许阳离子通过。

回答下列有关问题:
(1)图中X是_______ (填化学式),图中a%_______ c%(填“>”或“<”或“=”)。
(2)电解池的阴极反应式为_______ 。
(3)通入空气的电极的电极反应式为_______ ,燃料电池中阳离子的移动方向_______ (“从左向右”或“从右向左”)。
(4)写出电解饱和食盐水的化学方程式_______ ,电解池中产生2mol  ,理论上燃料电池中消耗
,理论上燃料电池中消耗 的物质的量为
的物质的量为_______ mol。
(5)在工业上利用电解NaOH溶液可以生产 ,装置如下图。
,装置如下图。
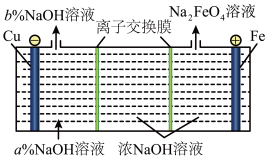
①阳极的电极反应式为_______ 。
②右侧的离子交换膜为_______ (填“阴”或“阳”)。

回答下列有关问题:
(1)图中X是
(2)电解池的阴极反应式为
(3)通入空气的电极的电极反应式为
(4)写出电解饱和食盐水的化学方程式
 ,理论上燃料电池中消耗
,理论上燃料电池中消耗 的物质的量为
的物质的量为(5)在工业上利用电解NaOH溶液可以生产
 ,装置如下图。
,装置如下图。
①阳极的电极反应式为
②右侧的离子交换膜为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】如图是原电池电解池的组合装置图。
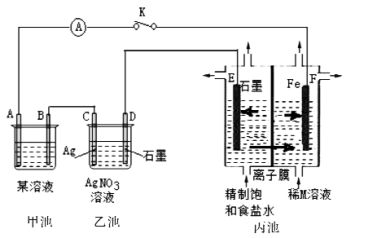
请回答:
(1)若甲池某溶液为稀H2SO4,闭合K时,电流表指针发生偏转,电极材料A为Fe,B为碳棒。则:
①甲池为______ (填“原电池”或“电解池”);B电极上发生的现象为______ 。
②乙池中的银电极上的电极反应式为______ 。
③丙池中E电极为______ (填“正极”、“负极”、“阴极”或“阳极”);闭合K一段时间后,稀M溶液的浓度会增加,则M溶液中的溶质是______ (填化学式);丙池中的离子膜为______ (填“阳离子交换膜”或“阴离子交换膜”)
(2)若将甲池的某溶液改为FeCl3,电极材料A为Cu、B为碳棒,则甲池的总反应的离子方程式为______ 。
(3)若甲池为氢氧燃料电池,某溶液为KOH溶液,A极通入氢气。则:
①A电极的反应方程式为______ 。
②若线路中转移0.02mol电子,乙池中D极质量变化______ g。
③二氧化氯(ClO2)为黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出也能用丙池装置制取二氧化氯。写出生成二氧化氯的电极反应式为______ 。

请回答:
(1)若甲池某溶液为稀H2SO4,闭合K时,电流表指针发生偏转,电极材料A为Fe,B为碳棒。则:
①甲池为
②乙池中的银电极上的电极反应式为
③丙池中E电极为
(2)若将甲池的某溶液改为FeCl3,电极材料A为Cu、B为碳棒,则甲池的总反应的离子方程式为
(3)若甲池为氢氧燃料电池,某溶液为KOH溶液,A极通入氢气。则:
①A电极的反应方程式为
②若线路中转移0.02mol电子,乙池中D极质量变化
③二氧化氯(ClO2)为黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出也能用丙池装置制取二氧化氯。写出生成二氧化氯的电极反应式为
您最近一年使用:0次



