已知:H2O(l)=H2O(g) △H=+44kJ·mol-1,结合下表中化学键的键能(测定温度:373K,单位:kJ·mol-1),下列表示甲烷燃烧热的热化学方程式正确的是
| 化学键 | C—H | O=O | C=O | O—H |
| 键能 | 412 | 497 | 799 | 463 |
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-808kJ·mol-1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-852kJ·mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-896kJ·mol-1 |
| D.2CH4(g)+4O2(g)=2CO2(g)+4H2O(l) △H=-1616kJ·mol-1 |
更新时间:2021/01/31 17:32:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g) =CO2(g)+2H2O(g) ΔH=−890.3 kJ/mol |
B.500℃、30MPa下将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3,放出19.3kJ热量,其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=−38.6 kJ/mol 2NH3(g) ΔH=−38.6 kJ/mol |
| C.HCl和NaOH反应的中和热为 ΔH=−57.3kJ/mol,则1 mol稀盐酸与1molNaOH反应放出的热量为−57.3kJ/mol |
| D.已知H2+Cl2 =2HCl 为放热反应,则1 mol H2与1molCl2 所具有的总键能小于2molHCl所具有的总键能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于热化学方程式的叙述正确的是
A.已知石墨比金刚石稳定,则C(石墨,s) C(金刚石,s) C(金刚石,s)  |
B.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
C.稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为 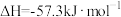 |
D.甲烷的燃烧热为890.3 ,热化学方程式为 ,热化学方程式为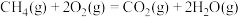  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用CH4催化还原NOx可以消除氮氧化物的污染。已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH= -1160kJ·mol-1
③H2O(g)=H2O(l) ΔH= -44kJ·mol-1,下列说法不正确的是( )
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH= -1160kJ·mol-1
③H2O(g)=H2O(l) ΔH= -44kJ·mol-1,下列说法不正确的是( )
| A.等物质的量的CH4参加反应,反应①、②转移的电子数相同 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ΔH= -618kJ·mol-1 |
| C.0.2mol CH4还原NO2至N2,并生成H2O(g),放出的热量为173.4 kJ |
| D.若用4.48L(标准状况)CH4还原NO2至N2并生成H2O(g),整个过程中转移电子1.6mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知几种离子反应的热化学方程式如下
①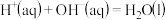
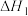
②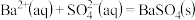

③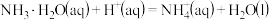
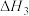
④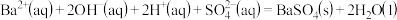
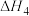
下列有关判断正确的是
①
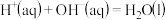
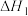
②
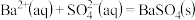

③
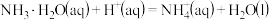
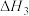
④
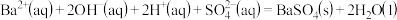
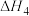
下列有关判断正确的是
A.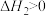 , ,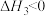 | B.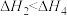 |
C.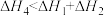 | D.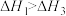 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
【推荐1】点阵能(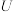 )是衡量晶体中离子间键结合能大小的一个量度,是阐明晶体化学性质的重要物理量。为探究
)是衡量晶体中离子间键结合能大小的一个量度,是阐明晶体化学性质的重要物理量。为探究 的离子键强弱,设计如下图所示的Born-Haber循环:
的离子键强弱,设计如下图所示的Born-Haber循环:
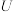 )是衡量晶体中离子间键结合能大小的一个量度,是阐明晶体化学性质的重要物理量。为探究
)是衡量晶体中离子间键结合能大小的一个量度,是阐明晶体化学性质的重要物理量。为探究 的离子键强弱,设计如下图所示的Born-Haber循环:
的离子键强弱,设计如下图所示的Born-Haber循环: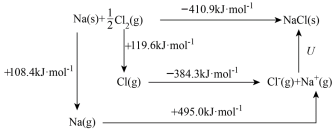
| A.+786.5 | B.-786.5 | C.+749.6 | D.-749.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】知某物质的标准生成焓(△f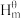 )的定义为用标准状态下的各种元素的最稳定单质,生成标准状态下1mol该物质所吸收或放出的能量,其中△f
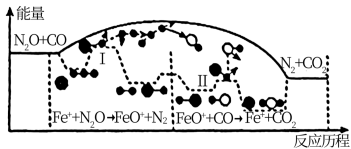
)的定义为用标准状态下的各种元素的最稳定单质,生成标准状态下1mol该物质所吸收或放出的能量,其中△f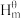 (单质)=0kJ/mor。N2O、CO、CO2的标准生成焓分别为82.1kJ/mol、110.5kJ/mol、-393.5kJ/mol。研究表明N2O与CO在Fe+的催化下发生反应NO(g)+CO(g)=N2(g)+CO2(g),△H的能量变化及反应历程如图所示,下列说法错误的是
(单质)=0kJ/mor。N2O、CO、CO2的标准生成焓分别为82.1kJ/mol、110.5kJ/mol、-393.5kJ/mol。研究表明N2O与CO在Fe+的催化下发生反应NO(g)+CO(g)=N2(g)+CO2(g),△H的能量变化及反应历程如图所示,下列说法错误的是
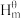 )的定义为用标准状态下的各种元素的最稳定单质,生成标准状态下1mol该物质所吸收或放出的能量,其中△f
)的定义为用标准状态下的各种元素的最稳定单质,生成标准状态下1mol该物质所吸收或放出的能量,其中△f (单质)=0kJ/mor。N2O、CO、CO2的标准生成焓分别为82.1kJ/mol、110.5kJ/mol、-393.5kJ/mol。研究表明N2O与CO在Fe+的催化下发生反应NO(g)+CO(g)=N2(g)+CO2(g),△H的能量变化及反应历程如图所示,下列说法错误的是
(单质)=0kJ/mor。N2O、CO、CO2的标准生成焓分别为82.1kJ/mol、110.5kJ/mol、-393.5kJ/mol。研究表明N2O与CO在Fe+的催化下发生反应NO(g)+CO(g)=N2(g)+CO2(g),△H的能量变化及反应历程如图所示,下列说法错误的是
| A.△H=-36.1kJ/mol |
| B.由过程I可得N2O的能量要高于N2的能量 |
| C.催化剂会改变反应途径和降低反应活化能,且反应速率由过程I决定 |
| D.在过程II中同时存在碳氧键的断裂和形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:N2(g)+3H2(g)  2NH3(g) △H = -92.2 kJ/mol。下列说法
2NH3(g) △H = -92.2 kJ/mol。下列说法不正确 的是
 2NH3(g) △H = -92.2 kJ/mol。下列说法
2NH3(g) △H = -92.2 kJ/mol。下列说法| A.1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3 (g)的能量 |
| B.形成2 mol NH3(g)的化学键释放的总能量大于断裂1 mol N2 (g) 和3 mol H2 (g) 的化学键所吸收的总能量 |
| C.加入催化剂是为了加大反应速率,缩短生产周期,降低生产成本 |
| D.将1 mol N2(g)和3 mol H2(g)充入一密闭容器中充分反应,放出92.2 kJ 的热量 |
您最近一年使用:0次


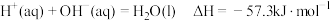
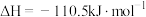
 的能量比
的能量比 的能量高
的能量高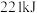
 溶液反应生成
溶液反应生成 水时,放出的热量为
水时,放出的热量为
 的
的 与
与 固体反应,放出的热量为
固体反应,放出的热量为

 的燃烧热
的燃烧热 为-266
为-266 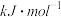

 =-572
=-572  所需能量较多的是系统(I)
所需能量较多的是系统(I)


