下列关于热化学方程式的叙述正确的是
A.已知石墨比金刚石稳定,则C(石墨,s) C(金刚石,s) C(金刚石,s)  |
B.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
C.稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为 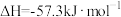 |
D.甲烷的燃烧热为890.3 ,热化学方程式为 ,热化学方程式为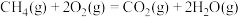  |
更新时间:2024-03-06 15:54:14
|
相似题推荐
【推荐1】2-甲氧-2-甲基丁烷(用TAME表示)常用作汽油添加剂。在催化剂作用下,可通过甲醇与烯烃的液相反应制得,体系中同时存在如下反应:
反应I:
反应II:
反应III:

反应Ⅰ、Ⅱ、Ⅲ的平衡常数Kx分别为Kx1、Kx2、Kx3(Kx是以物质的量分数代替物质的量浓度表示的平衡常数)与温度T变化关系如上图所示。现向某反应容器中加入1.0molTAME,控制温度为353K,反应30min后达到平衡状态。下列说法正确的是
反应I:

反应II:

反应III:


反应Ⅰ、Ⅱ、Ⅲ的平衡常数Kx分别为Kx1、Kx2、Kx3(Kx是以物质的量分数代替物质的量浓度表示的平衡常数)与温度T变化关系如上图所示。现向某反应容器中加入1.0molTAME,控制温度为353K,反应30min后达到平衡状态。下列说法正确的是
| A.烯烃A和B,其中A相对稳定 |
| B.反应Ⅰ、Ⅱ中,△H1大于△H2 |
| C.达到平衡时,容器中烯烃A与CH3OH的物质的量之比为1:10 |
| D.同温同压下,向该容器中注入惰性溶剂稀释,反应Ⅰ的平衡将正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某反应的能量关系如图所示,下列有关说法正确的是


| A.C(金刚石,s)=C(石墨,s) ΔH<0 |
| B.金刚石比石墨稳定 |
| C.1 mol C(石墨,s)转化为1 mol C(金刚石,s)的ΔH=E2-E1 |
| D.断开1 mol石墨中的化学键所吸收的能量小于断开1 mol金刚石中化学键所吸收的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);△H=a kJ/mol,下列叙述不正确的是
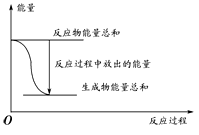
| A.反应过程中能量关系如上图表示,则该反应为放热反应 |
| B.若将该反应设计成原电池,锌为负极 |
| C.化学反应的焓变与反应方程式的计量数有关 |
| D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于车用燃料及安全气囊的说法正确的是
| A.选择车用燃料时,应选择热值高且燃点非常低的燃料 |
| B.汽车排气系统使用三元催化器可使氮氧化物完全转化为无害气体 |
C.已知氮气分子的键能非常大,所以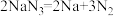 为吸热反应 为吸热反应 |
| D.甲醇可作新能源汽车燃料,完全燃烧等质量的甲醇和乙醇,甲醇的耗氧量低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于热化学反应的描述中正确的是
| A.若盐酸和NaOH溶液反应生成1molH2O(l)的ΔH为-57.3kJ•mol-1,则CH3COOH溶液和Ba(OH)2溶液反应生成1molH2O(l)的ΔH也为-57.3kJ•mol-1 |
| B.CO(g)燃烧热是283.0kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)的ΔH=-(2×283.0)kJ•mol-1 |
| C.N2(g)燃烧热是指在101kPa,1molN2(g)完全生成NO2(g)时所放出的热量 |
| D.同温同压下,4Al(s)+3O2(g)=2Al2O3(s)在常温和点燃条件下的ΔH相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列依据热化学方程式得出的结论正确的是( )
| 选项 | 热化学方程式 | 结论 |
| A | 2C(石墨)+O2(g)=2CO(g)ΔH=-222kJ·mol-1 | 石墨的燃烧热为111kJ/mol |
| B | OH-(aq)+H+(aq)=H2O(g)△H=-57.3kJ/mol | 含1molNaOH的稀溶液与浓H2SO4完全中和,放出热量小于57.3kJ |
| C | 2C(s)+2O2(g)=2CO2(g)△H=-akJ/mol 2C(s)+O2(g)=2CO(g)△H=-bkJ/mol | b<a |
| D | C(石墨,s)=C(金刚石,s)△H=+1.5kJ/mol | 金刚石比石墨稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,H2的燃烧热为285.8kJ/mol,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8kJ/mol |
| D.在稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molKOH的溶液混合,放出的热量大于57.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.如果旧化学键断裂吸收的能量大于新化学键形成释放的能量,则该反应为吸热反应 |
| B.H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ•mol-1可以表示所有强酸和强碱的中和反应 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ•mol-1 2NH3(g) △H=-38.6kJ•mol-1 |
| D.根据CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ•mol-1,可以得出CH4的燃烧热为890.3kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列热化学方程式正确的是(ΔH的绝对值均正确)( )
| A.Hg+1/2O2=HgO ΔH=-90.7 kJ·mol-1(反应热) |
| B.P(s)+3/2Cl2(g)=PCl3(g) ΔH=-306 kJ·mol-1(反应热) |
| C.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-725.76 kJ·mol-1(燃烧热) |
| D.NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l) ΔH=+57.3 kJ·mol-1(中和热) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列描述中正确的是
| A.纯碱溶于热水后去污效果增强,说明纯碱的水解反应是吸热反应 |
| B.NH3(g) + HCl(g) = NH4Cl(s) 在较低温度下能自发进行,说明该反应的ΔH>0 |
C.500℃、30 MPa下,将7 g N2和3 g H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
| D.甲烷的燃烧热(ΔH)为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)= CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
您最近一年使用:0次

 ,能与水混溶)的装置(夹持装置已省略)如图所示。下列说法错误的是
,能与水混溶)的装置(夹持装置已省略)如图所示。下列说法错误的是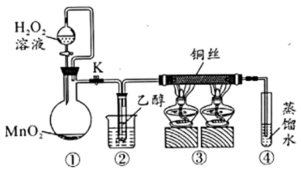
 ,最后点燃③处酒精灯
,最后点燃③处酒精灯

