对于化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);△H=a kJ/mol,下列叙述不正确的是
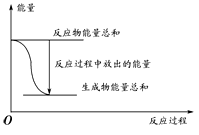
| A.反应过程中能量关系如上图表示,则该反应为放热反应 |
| B.若将该反应设计成原电池,锌为负极 |
| C.化学反应的焓变与反应方程式的计量数有关 |
| D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
更新时间:2017-02-27 21:29:51
|
相似题推荐
【推荐1】已知某化学反应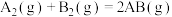 的能量变化如图所示,下列有关叙述中正确的是
的能量变化如图所示,下列有关叙述中正确的是
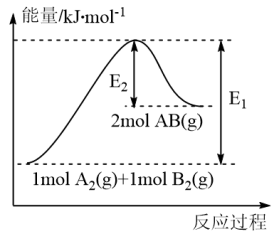
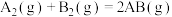 的能量变化如图所示,下列有关叙述中正确的是
的能量变化如图所示,下列有关叙述中正确的是
| A.该反应是放热反应 |
| B.该反应中反应物的键能总和大于生成物的键能总和 |
C.该反应的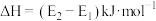 |
| D.由2 molA(g)和2 molB(g)形成2 molA-B键吸收的能量为E2 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某反应由两步反应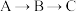 构成,其反应能量曲线如图所示,下列叙述正确的是
构成,其反应能量曲线如图所示,下列叙述正确的是

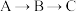 构成,其反应能量曲线如图所示,下列叙述正确的是
构成,其反应能量曲线如图所示,下列叙述正确的是
A. 的反应不一定需要加热 的反应不一定需要加热 | B.两步反应均为吸热反应 |
C.A与C的能量差为 | D.三种物质中B最稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实能够说明甲比乙金属性强的是
| A.乙单质能从甲的盐溶液中置换出甲单质 |
| B.甲单质与乙单质构成原电池,甲单质作负极 |
| C.最高价氧化物对应的水化物碱性比较,乙比甲的强 |
| D.甲、乙的单质都能与盐酸反应,相同条件下甲单质与盐酸反应更剧烈 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】与甲、乙两套装置有关的下列说法正确的是
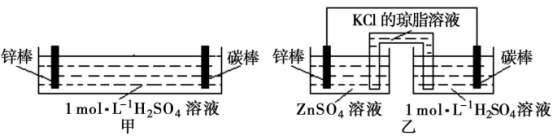

| A.甲、乙装置中,锌棒均作负极,发生氧化反应 |
| B.甲中锌棒直接与稀H2SO4接触,故甲生成气泡的速率更快 |
| C.甲、乙装置的电解质溶液中,阳离子均向碳棒定向迁移 |
| D.乙中盐桥设计的优点是迅速平衡电荷,提高电池效率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在理论上不能用于设计原电池的化学反应是( )
| A.HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) |
| C.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) |
| D.2H2(g)+O2(g)=2H2O(l) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】实现化学能转变为电能的装置是( )
A. 干电池 干电池 | B. 电解水 电解水 |
C. 太阳能热水器 太阳能热水器 | D. 水力发电 水力发电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】肼(N2H4)暴露在空气中容易爆炸,但利用其作燃料电池是一种理想的电池,具有容量大、能量转化效率高、产物无污染等特点,其工作原理如图所示,下列叙述错误的是
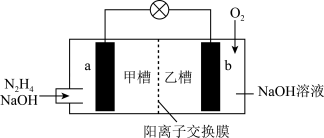

| A.电池工作时,正极附近的pH升高 |
| B.当消耗1molO2时,有2molNa+由甲槽向乙槽迁移 |
| C.负极反应为4OH-+N2H4-4e-=N2+4H2O |
| D.若去掉离子交换膜电池不能正常工作 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】硝酸汞和碘化钾溶液混合后会生成红色的碘化汞沉淀,为了探究硝酸汞和碘化钾溶液之间能否发生氧化还原反应,研究人员设计了如图的实验装置,结果电流计指针发生了偏转,下列分析正确的是


| A.如图装置的电流方向是从C1到C2 |
| B.C1是负极,发生的反应是2I--2e-=I2 |
| C.K+向C1电极流动 |
| D.装置发生的总反应是Hg2++2I-=HgI2↓ |
您最近一年使用:0次



