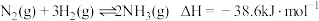下列说法正确的是
| A.如果旧化学键断裂吸收的能量大于新化学键形成释放的能量,则该反应为吸热反应 |
| B.H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ•mol-1可以表示所有强酸和强碱的中和反应 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ•mol-1 2NH3(g) △H=-38.6kJ•mol-1 |
| D.根据CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ•mol-1,可以得出CH4的燃烧热为890.3kJ•mol-1 |
更新时间:2022-11-08 21:28:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】创新实验小组设计如图装置进行乙醇催化氧化的实验探究。下列叙述错误的是
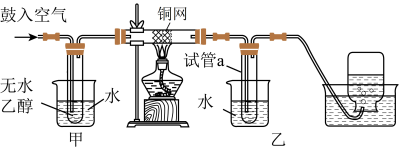
| A.甲、乙烧杯中的水均起冷却作用 |
| B.铜网表面乙醇发生氧化反应 |
| C.试管a收集到的液体中至少有两种有机物 |
| D.反应开始后熄灭酒精灯,铜网仍能红热,说明乙醇的催化氧化是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下图是计算机模拟的在催化剂表面上水煤气变化的反应历程。吸附在催化剂表面的物种用“*”标注。
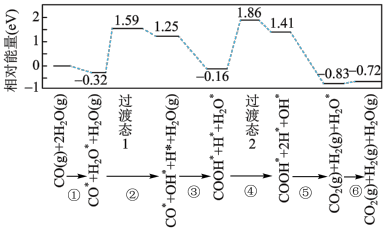
A.①表示 和 和 在催化剂表面吸附的过程 在催化剂表面吸附的过程 |
| B.②和④中化学键变化相同,因此吸收的能量相同 |
C.由图可知 为放热反应 为放热反应 |
D.该历程中决速步骤为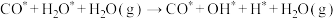 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关热化学方程式的说法正确的是
A.甲烷的标准燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为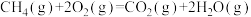  |
B.500℃、30MPa下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为: ,放热19.3kJ,其热化学反应方程式为:  |
C.已知稀溶液中 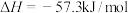 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
D.CO(g)的燃烧热是283.0kJ/mol,则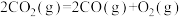 反应的 反应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知如下化学键的键能:
则下列热化学方程式不 正确的是
| 化学键 | H—H | Cl—Cl | H—Cl |
| 生成1 mol化学键时放出的能量 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
A. H2(g)+ H2(g)+ Cl2(g)=HCl(g) ΔH=-91.5kJ/mol Cl2(g)=HCl(g) ΔH=-91.5kJ/mol |
| B.H2(g)+Cl2(g)=2HCl(g) ΔH=-183kJ/mol |
| C.2HCl(g)=H2(g)+Cl2(g) ΔH=+183kJ/mol |
D. H2(g)+ H2(g)+ Cl2(g)=HCl(g) ΔH=+91.5kJ/mol Cl2(g)=HCl(g) ΔH=+91.5kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有关热化学方程式书写与对应关系表述均正确的是
| A.稀醋酸与0.1mol•L-1NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=+57.3kJ•mol-1 |
| B.在101KPa下氢气的燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5kJ•mol-1 |
| C.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)=FeS(s)△H=-95.6kJ•mol-1 |
| D.已知2C(s)+O2(g)=2CO(g)△H=-221kJ•mol-1,则可知C的燃烧热为110.5 kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是( )
| A.酸和碱发生中和反应生成H2O时所放出的热量称为中和热 |
| B.物质完全燃烧生成氧化物时所放出的热量叫做该物质的燃烧热 |
| C.反应物所具有的总能量大于生成物所具有的总能量时,△H<0 |
| D.反应物所具有的总能量小于生成物所具有的总能量时,△H<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列热化学方程式正确的是
A.乙烷的燃烧热为1560 kJ·mol-1,则乙烷燃烧热的热化学方程式可表示为C2H6(g)+ O2(g)=2CO2(g)+3H2O(l) △H=-1560 kJ·mol-1 O2(g)=2CO2(g)+3H2O(l) △H=-1560 kJ·mol-1 |
B.500℃、30MPa下,将1 mol SO2(g)和0.5 mol O2(g)置于密闭容器中充分反应生成SO3(g),放热80 kJ,其热化学方程式为2SO2(g)+O2(g) 2SO3(g) △H>-160 kJ·mol-1 2SO3(g) △H>-160 kJ·mol-1 |
| C.已知1 g液态偏二甲肼(C2H8N2)和足量液态四氧化二氮反应生成CO2、N2和水蒸气时放出a kJ的热量,肼和过氧化氢反应的热化学方程式为C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(l)+3N2(g) △H=-60a kJ·mol-1 |
| D.含29.0 g KOH的稀溶液与稀醋酸完全中和,放出21 kJ的热量,则稀盐酸和稀NaOH溶液反应的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-42 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列方程式中,正确的是()
| A.已知H+(a)+OH-(ag)= H2O(l) △H= - 57.3kJ/mol,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ/mol |
| B.H2(g)的燃烧热是285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g) △H= +571.6 kJ/mol |
C.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+  O2(g)= CO2(g)+ 2H2(g)△H=-192.9 kJ/mol,则CH3OH(g)的燃烧热为192.9 kJ/mol O2(g)= CO2(g)+ 2H2(g)△H=-192.9 kJ/mol,则CH3OH(g)的燃烧热为192.9 kJ/mol |
| D.31 g白磷比31 g红磷能量多b kJ,P4(白磷, s)=4P(红磷, s)△H= -4b kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式正确的是( )
| A.甲烷的燃烧热为890.3KJ•mol-1,则甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 |
B.500℃、30 MPa 下,将0.1mol N2 和 0.3mol H2 置于密闭容器中充分反应生成NH3(g),放热3.86 kJ,其热化学方程式为:N2(g)+3H2(g)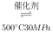 2NH3(g)△H=-38.6kJ•mol-1 2NH3(g)△H=-38.6kJ•mol-1 |
| C.已知1g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05kJ的热量,肼和过氧化氢反应的热化学方程式为: N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.6 kJ•mol-1 |
| D.CO(g)的燃烧热是283.0 KJ•mol-1,则2CO2(g)═2CO(g)+O2(g) 反应的△H=+283.0 kJ•mol-1 |
您最近一年使用:0次

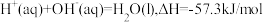 ,若将含0.5 mol H2SO4的稀硫酸与含
,若将含0.5 mol H2SO4的稀硫酸与含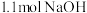 的稀溶液混合,放出的热量等于57.3 kJ
的稀溶液混合,放出的热量等于57.3 kJ 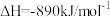 ,则甲烷燃烧的热化学方程式为:
,则甲烷燃烧的热化学方程式为: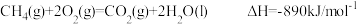
 键、
键、 键和
键和 键的键能分别为
键的键能分别为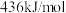 ,
,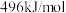 和
和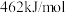 ,则反应
,则反应 的
的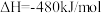
 ,石墨比金刚石稳定
,石墨比金刚石稳定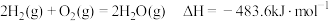 ,则氢气的燃烧热为
,则氢气的燃烧热为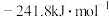
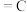 (金刚石,s)
(金刚石,s) ,则石墨比金刚石更稳定
,则石墨比金刚石更稳定 、
、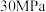 下,将
下,将 和
和 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成 ,放热
,放热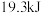 ,则其热化学方程式
,则其热化学方程式