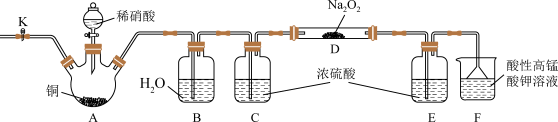
已知:2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3。
(1)装置A中发生反应的离子方程式为
(2)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡后再关上止水夹K。
①通入N2的目的是
②若通入N2未达到预期目的,装置B可除去NO中的NO2杂质,该反应的化学方程式为
(3)实验时装置D中的实验现象是
(4)装置C、E不可省去,省去会导致产品中混有杂质
(5)装置F的作用是
相似题推荐
回答下列问题:
(1)向银催化剂中加入稀硝酸溶解的化学方程式为
(2)用氯化钠溶液沉淀银离子可发生下列反应:
Ⅰ.
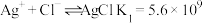
Ⅱ.
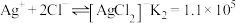
Ⅲ.
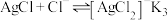
①计算

②根据上述平衡信息,为了使
 沉淀完全,应注意控制的条件是
沉淀完全,应注意控制的条件是(3)亚硫酸钠-甲醛还原法浸取
 的主要反应为
的主要反应为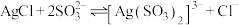 。
。①该反应在敞口容器中进行,其他条件不变时,浸出时间过长会使银的浸出率降低,原因可能是
②浸出液中含银微粒总浓度随含硫微粒总浓度及浸出液
 的关系如图所示:
的关系如图所示: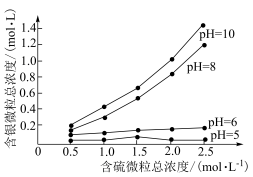
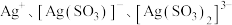 、
、 和
和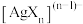 (X为
(X为 或
或 ),则含硫微粒的总浓度
),则含硫微粒的总浓度 +
+ ;
; 时,含银微粒总浓度随含硫微粒总浓度的变化不大,
时,含银微粒总浓度随含硫微粒总浓度的变化不大, 时,含银微粒总浓度随含硫微粒总浓度的变化较大,原因是
时,含银微粒总浓度随含硫微粒总浓度的变化较大,原因是(4)常温下用氨浸-水合肼还原法浸取
 ,已知:
,已知: ,
, ,写出
,写出 溶于氨水发生反应的离子方程式:
溶于氨水发生反应的离子方程式:
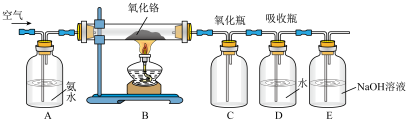
(1)实验装置B中氧化铬的作用是
(2)C中发生的主要化学反应方程式是
(3)为探究白烟的成分,检验其中的阳离子,具体操作是
(4)若D装置中为稀溶液,在D中置入Cu片,反应的化学方程式是
(5)某小组同学认为该装置存在不足,欲对实验装置进行改进。小组同学通过查阅资料并讨论后,得到改进后的装置如下图所示。
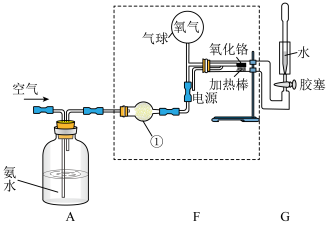
其中甲同学认为可以将B装置改为F装置所示,目的是

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式
(2)若A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是
(3)诺实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式
 ,还含有CaO、
,还含有CaO、 、FeS等杂质,以该软锰矿为原料制备碳酸锰(
、FeS等杂质,以该软锰矿为原料制备碳酸锰( )的工业流程图如下:
)的工业流程图如下:
已知:①部分阳离子沉淀时溶液的pH如下表。
| 阳离子 |  |  |
| 开始沉淀的pH | 8.8 | 10.6 |
| 沉淀完全的pH | 10.1 | 13.1 |
 为难溶物
为难溶物回答下列问题:
(1)用稀硫酸“浸出”软锰矿时,要在适当的高温下进行,并不断搅拌的目的是
(2)“操作Ⅰ”需要加入试剂X调节溶液的pH,试剂X最好选用
A.
 溶液 B.NaOH溶液 C.氨水 D.
溶液 B.NaOH溶液 C.氨水 D. 固体
固体已知室温下
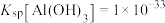 ,
, ,则室温下“操作Ⅰ”中除去杂质离子(要求杂质离子浓度均小于
,则室温下“操作Ⅰ”中除去杂质离子(要求杂质离子浓度均小于 )所需调节溶液的pH在
)所需调节溶液的pH在(3)写出“沉锰”时加入足量
 的离子方程式为
的离子方程式为【推荐2】过碳酸钠 是过氧化物类的消毒剂,可以利用侯氏制碱法得到的
是过氧化物类的消毒剂,可以利用侯氏制碱法得到的 ,进行制备,流程图如下:
,进行制备,流程图如下:
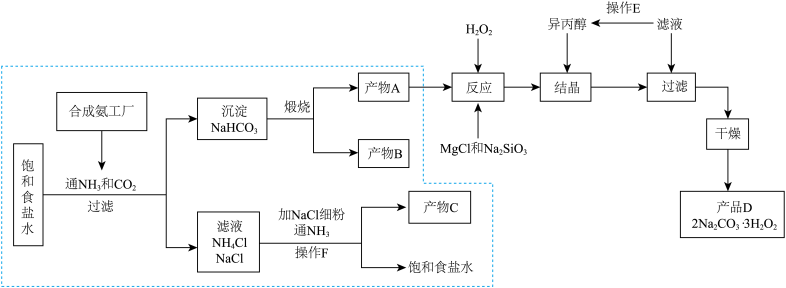
已知:①产物 中可能含有少量的
中可能含有少量的 、
、 金属离子杂质。②硅酸钠可与
金属离子杂质。②硅酸钠可与 、
、 等高价金属离子形成沉淀。
等高价金属离子形成沉淀。
请回答下列问题:
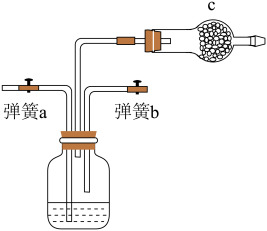
(1)虚线框中是侯氏制碱法的原理,某同学用右图装置在实验室模拟侯氏制碱法,实验中应先打开弹簧夹 或
或 ),通入
),通入
(2)索尔维制碱法是利用石灰石分解制备 ,并用生成的
,并用生成的 和
和 反应制备氨气,将
反应制备氨气,将 和
和 通入饱和食盐水制备
通入饱和食盐水制备 晶体,分离提纯后分解制备纯碱。与索尔维制碱法相比,侯氏制碱法的优点是(至少写两点)
晶体,分离提纯后分解制备纯碱。与索尔维制碱法相比,侯氏制碱法的优点是(至少写两点)
(3)“反应”需控制温度在 左右,写出“反应”中生成产品
左右,写出“反应”中生成产品 的化学方程式
的化学方程式 的作用是
的作用是
(4)流程图中可循环使用的物质有
(5)操作 的主要步骤有
的主要步骤有 和
和 的溶解度曲线如图所示)
的溶解度曲线如图所示)

(6)为了测定产品 的纯度,某小组的方法是:取
的纯度,某小组的方法是:取 产品配成
产品配成 的溶液,取出
的溶液,取出 用
用 用硫酸酸化的
用硫酸酸化的 溶液滴定至终点,该滴定过程中消耗高锰酸钾标准溶液的体积为
溶液滴定至终点,该滴定过程中消耗高锰酸钾标准溶液的体积为 。产品的纯度为
。产品的纯度为 和
和 的式子表示)。
的式子表示)。
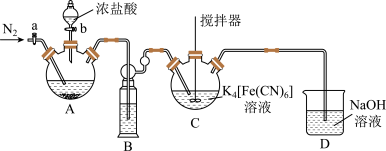
(1)装置B中试剂是
(2)反应结束后通入N2一段时间的目的是
(3)实验室用于检验溶液中是否含有Fe2+的试剂是:
(4)工业上可用铁氰化钾法测定蔗糖(C12H22O11)的水解程度(杂质不参与反应)。
Ⅰ.反应原理:铁氰化钾在碱性溶液中有氧化性,能将葡萄糖(或果糖)氧化,反应的化学方程式为
C6H12O6+6 K3[Fe(CN)6]+6KOH= (CHOH)4·(COOH)2 +6 K4[Fe(CN)6]+4H2O
Ⅱ.实验步骤:
i.称取纯净的蔗糖1.000g,置于锥形瓶中,加入少量水溶解:再加5 mL 2mol·L-1稀硫酸、摇匀,加热20分钟:
ii.向i中所得溶液加入KOH调节pH至碱性;
iii.加入2滴次甲基兰指示剂,用cmol·L-1铁氰化钾标准液滴定,终点时消耗标准液V mL。
已知:铁氰化钾溶液中加入次甲基兰指示剂,溶液迅速变蓝。
①蔗糖的水解程度为
②下列操作会导致测定结果偏低的是
a.配制铁氰化钾溶液时,转移操作未洗涤烧杯
b.溶液变蓝立即读数,后又恢复无色
c.滴定前俯视,滴定后仰视
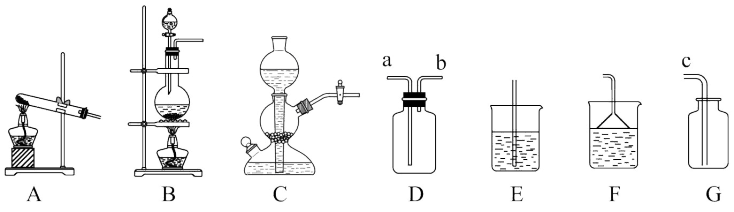
(1)该反应的化学方程式为
(2)要得到干燥的氯化氢气体,还需要在制取和收集装置之间插入一个装置D,此时D中装入的液体应该是
(3)气体发生在装置的选择要考虑反应物状态和反应条件等因素。
实验室制取氧气(氯酸钾和二氧化锰)和二氧化碳的发生装置都不用装置B,其原因分别是制取氧气时
(4)将标准状况下的200体积HCl气体溶于1体积水中,得到密度为1.12g/mL的盐酸,则该盐酸的物质的量浓度是
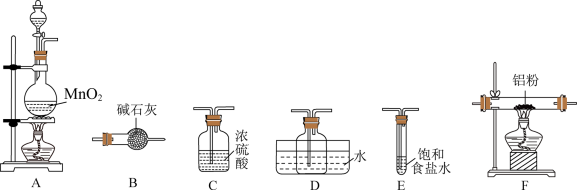
(1)本实验制备氯气的离子方程式为
(2)气体流动方向是从左至右,装置的连接顺序为
(3)装置B的作用有
(4)装置D的作用为冷凝并收集AlCl3,D装置存在的明显缺陷是
(5)连接装置之后,检查装置的气密性,装药品。先点燃A处酒精灯,当
 是黄绿色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会燃烧并爆炸。一种制取
是黄绿色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会燃烧并爆炸。一种制取 的装置如图所示。
的装置如图所示。
已知:
 的熔点为
的熔点为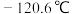 ,沸点为
,沸点为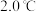 ;
; 的沸点为
的沸点为 ;
;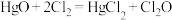 。
。回答下列问题:
(1)写出装置①发生反应的离子方程式:
(2)装置②③中盛装的试剂依次是
(3)通入干燥空气的目的是
(4)装置④与⑤之间不能用橡胶管连接,其目的是
(5)液氨的作用是



