水是生命的源泉、工业的血液、城市的命脉。河水是主要的饮用水源,污染物通过饮用水可毒害人体,也可通过食物链和灌溉农田间接危及健康。请回答下列问题:
(1)纯水在100℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=___________ mol•L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为___________ 。
(3)体积均为100mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数___________ (填“大于”或“小于”或“等丁”)CH3COOH的电离平衡常数,理由是___________ 。

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三种溶液的pH由大到小的顺序为___________ 。
(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH = 6,则溶液中c(CH3COO-)-c(Na+)=___________ mol•L-1(填精确值)。
(1)纯水在100℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为
(3)体积均为100mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃ ) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三种溶液的pH由大到小的顺序为
(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH = 6,则溶液中c(CH3COO-)-c(Na+)=
更新时间:2021-02-05 17:17:47
|
【知识点】 盐类水解的应用
相似题推荐
填空题
|
较难
(0.4)
【推荐1】“ 还原法”制备高纯度氢碘酸和亚磷酸钠
还原法”制备高纯度氢碘酸和亚磷酸钠 的工业流程如图。
的工业流程如图。

已知:ⅰ. 为一元弱酸
为一元弱酸
ⅱ. 为二元酸,25℃时其电离常数:
为二元酸,25℃时其电离常数: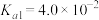 ,
,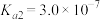
ⅲ.25℃时: ,
,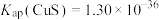
回答下列问题:
(1) 属于
属于______ (填“正盐”或“酸式盐”)。
(2)“合成”过程,主要氧化产物为 ,相应的化学方程式为
,相应的化学方程式为______ 。
(3)“除铜”过程发生的反应为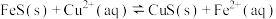 ,经过计算可得该反应的平衡常数
,经过计算可得该反应的平衡常数
______ 。
(4)常温下 的
的
______ 7(填“>”、“=”或“<”)。
(5)常温下 溶液呈碱性的原因为(用离子方程式表示)
溶液呈碱性的原因为(用离子方程式表示)______ 。
 还原法”制备高纯度氢碘酸和亚磷酸钠
还原法”制备高纯度氢碘酸和亚磷酸钠 的工业流程如图。
的工业流程如图。
已知:ⅰ.
 为一元弱酸
为一元弱酸ⅱ.
 为二元酸,25℃时其电离常数:
为二元酸,25℃时其电离常数: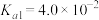 ,
,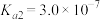
ⅲ.25℃时:
 ,
,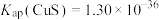
回答下列问题:
(1)
 属于
属于(2)“合成”过程,主要氧化产物为
 ,相应的化学方程式为
,相应的化学方程式为(3)“除铜”过程发生的反应为
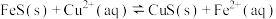 ,经过计算可得该反应的平衡常数
,经过计算可得该反应的平衡常数
(4)常温下
 的
的
(5)常温下
 溶液呈碱性的原因为(用离子方程式表示)
溶液呈碱性的原因为(用离子方程式表示)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】 (1)碳酸钠溶液中各离子按照浓度从大到小的顺序依次为: ___________________________ 。
(2)下表是几种常见弱酸的电离平衡常数(25℃)
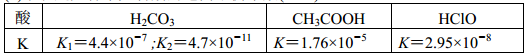
根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是_______________ ;25℃时, 等浓度的Na2CO3、NaAc 和NaClO三种溶液的pH从小到大依次是___________________ 。
(3)常温下,将0.02 mol·L-1 的 Ba(OH)2溶液100 mL和0.02 mol·L-1的NaHSO4溶液100 mL混合,若忽略溶液体积变化,则混合后的溶液的 pH 为___________ 。
(4)25℃时, Ksp[Mg(OH)2]=5.61×10-12, Ksp[MgF2]=7.42×10-11。 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,_________ (填化学式)溶液中的 c(Mg2+)大。
(2)下表是几种常见弱酸的电离平衡常数(25℃)
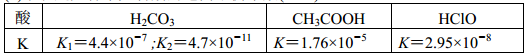
根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是
(3)常温下,将0.02 mol·L-1 的 Ba(OH)2溶液100 mL和0.02 mol·L-1的NaHSO4溶液100 mL混合,若忽略溶液体积变化,则混合后的溶液的 pH 为
(4)25℃时, Ksp[Mg(OH)2]=5.61×10-12, Ksp[MgF2]=7.42×10-11。 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______ (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) _______ c(CH3COO-)(填“ >”或“=”或“<” )。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________ ,溶液中c(Na+) ___________ c(CH3COO-) (填“ >” 或“=”或“<” )
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈________ .
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈
您最近一年使用:0次



