铁是人类最早使用的金属之一,人们在5000多年前就开始使用铁,如今它是应用最广泛的金属,被誉为“金属之王”。请回答下列问题:
(1)红热的铁与水蒸气发生反应生成的产物是_______ 。(填化学式)
(2)向盛有硫酸铁溶液的烧杯中滴加NaOH溶液,产生的现象是_______ 。
(3)氯化铁可用于五金蚀刻,不锈钢广告牌上的图形和文字就是用氯化铁溶液蚀刻而成,该过程发生的主要反应的离子方程式为_______ ,该反应说明_______ (填化学式)具有氧化性。
(4)某工业废水中含有大量FeSO4和较多Cu2+,为减少污染并变废为宝,向该废水中加入足量Fe并过滤以回收FeSO4和金属铜。
①加入Fe发生反应的离子方程式为_______ 。
②过滤后的固体中含有Cu和_______ (填化学式),可加入_______ (填试剂名称)再过滤,得到金属铜。
③若经过回收得到128g金属铜,则加入Fe的质量至少为_______ g。
(1)红热的铁与水蒸气发生反应生成的产物是
(2)向盛有硫酸铁溶液的烧杯中滴加NaOH溶液,产生的现象是
(3)氯化铁可用于五金蚀刻,不锈钢广告牌上的图形和文字就是用氯化铁溶液蚀刻而成,该过程发生的主要反应的离子方程式为
(4)某工业废水中含有大量FeSO4和较多Cu2+,为减少污染并变废为宝,向该废水中加入足量Fe并过滤以回收FeSO4和金属铜。
①加入Fe发生反应的离子方程式为
②过滤后的固体中含有Cu和
③若经过回收得到128g金属铜,则加入Fe的质量至少为
更新时间:2021-02-09 08:18:27
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空
(1)KAl(SO4)2的电离方程式:___________ 。
(2)NaHCO3的电离方程式:___________ 。
(3)铁与盐酸反应的离子方程式:___________ 。
(4)硫酸铜溶液与氢氧化钡溶液反应的离子方程式:___________ 。
(5)实验室制二氧化碳的反应的离子方程式:___________ 。
(6)家中用醋酸除水垢反应的离子方程式:___________ 。
(7)氧化亚铁与盐酸反应的离子方程式:___________ 。
(1)KAl(SO4)2的电离方程式:
(2)NaHCO3的电离方程式:
(3)铁与盐酸反应的离子方程式:
(4)硫酸铜溶液与氢氧化钡溶液反应的离子方程式:
(5)实验室制二氧化碳的反应的离子方程式:
(6)家中用醋酸除水垢反应的离子方程式:
(7)氧化亚铁与盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空:
(1)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:______________ 。






配制KMnO4溶液,定容的操作方法为_______________________ 。
(2)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是__________ (填化学方程式)。
(3)写出Na2SO4和NaCl混合溶液中 的检验方法:
的检验方法:___________________ 。
(4)从硫酸亚铁溶液中获得硫酸亚铁晶体FeSO4•7H2O的实验操作为__________ 、__________ 、过滤、冰水洗涤、烘干。取27.8g FeSO4•7H2O隔绝空气加热至不同温度,剩余固体的质量变化如图所示。
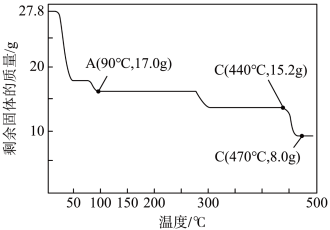
分析数据,写出90℃残留物的化学式:__________ ;440~470℃时固体物质发生反应的化学方程式是________________________ 。
(1)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:






配制KMnO4溶液,定容的操作方法为
(2)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是
(3)写出Na2SO4和NaCl混合溶液中
 的检验方法:
的检验方法:(4)从硫酸亚铁溶液中获得硫酸亚铁晶体FeSO4•7H2O的实验操作为

分析数据,写出90℃残留物的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】向少量 粉末中加入适量盐酸,反应后得到的
粉末中加入适量盐酸,反应后得到的 溶液呈棕黄色。回答下列问题:
溶液呈棕黄色。回答下列问题:
(1)赤铁矿的主要成分为 ,
, 俗称
俗称_______ ,请写出 的一种用途:
的一种用途:_______ 。
(2)取少量 溶液置于试管中,加入过量铁粉,该反应的离子方程式为
溶液置于试管中,加入过量铁粉,该反应的离子方程式为_______ 。
(3)向(2)反应后的溶液中加入NaOH溶液,产生的白色沉淀最终变为红褐色,请解释沉淀颜色变化的原因:_______ (用化学方程式表示)。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈_______ 色,即可制得 胶体。
胶体。
(5)取另一烧杯也加入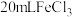 溶液,将此烧杯(编号甲)与盛有
溶液,将此烧杯(编号甲)与盛有 胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到_______ (填“编号甲”或“编号乙”)烧杯中的液体会产生丁达尔效应。这个实验可以用来区别_______ 。
 粉末中加入适量盐酸,反应后得到的
粉末中加入适量盐酸,反应后得到的 溶液呈棕黄色。回答下列问题:
溶液呈棕黄色。回答下列问题:(1)赤铁矿的主要成分为
 ,
, 俗称
俗称 的一种用途:
的一种用途:(2)取少量
 溶液置于试管中,加入过量铁粉,该反应的离子方程式为
溶液置于试管中,加入过量铁粉,该反应的离子方程式为(3)向(2)反应后的溶液中加入NaOH溶液,产生的白色沉淀最终变为红褐色,请解释沉淀颜色变化的原因:
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。
胶体。(5)取另一烧杯也加入
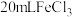 溶液,将此烧杯(编号甲)与盛有
溶液,将此烧杯(编号甲)与盛有 胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题:
(1)新制氯水在阳光照射下缓慢产生的无色气体为_______ (填化学式)。
(2)氢氟酸若用玻璃试剂瓶盛装,发生的主要反应的化学方程式为_______ 。
(3)实验室常用 Al2(SO4)3 和NH3·H2O制备Al(OH)3其反应的离子方程式为_______ 。
(4)用玻璃棒蘸浓硫酸滴在火柴梗上,火柴梗变黑,浓硫酸表现出来的性质为_______ 。
(5)维生素C能将人体摄取的Fe3+转变为Fe2+,说明维生素C 具有_______ (选填“氧化性”或“还原性”)。
(1)新制氯水在阳光照射下缓慢产生的无色气体为
(2)氢氟酸若用玻璃试剂瓶盛装,发生的主要反应的化学方程式为
(3)实验室常用 Al2(SO4)3 和NH3·H2O制备Al(OH)3其反应的离子方程式为
(4)用玻璃棒蘸浓硫酸滴在火柴梗上,火柴梗变黑,浓硫酸表现出来的性质为
(5)维生素C能将人体摄取的Fe3+转变为Fe2+,说明维生素C 具有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知:A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。___________ 。
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为___________ ;若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___________ 。(填字母)
a. 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液
(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入 溶液变红。
溶液变红。
①写出加热条件下C的浓溶液与X反应生成D的化学方程式___________ 。
②检验溶液D中还可能存在 的方法是
的方法是___________ 。
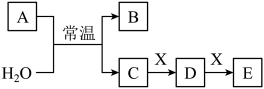
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则
 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为a.
 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入
 溶液变红。
溶液变红。①写出加热条件下C的浓溶液与X反应生成D的化学方程式
②检验溶液D中还可能存在
 的方法是
的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】黄铜矿(CuFeS2)是制铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是_____ (填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是_____ (填代号)
a.高空排放b.用于制备硫酸c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2: +2I-=2
+2I-=2 +I2
+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程___ 、___
(1)冶炼铜的反应为8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是
a.高空排放b.用于制备硫酸c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:
 +2I-=2
+2I-=2 +I2
+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常温下,0.1mol·L-1的 FeCl3 溶液呈___________ 性(填“酸”、“碱”或“中”),原因是___ (请用离子方程式表示)。电子工业曾用 30%的 FeCl3溶液腐蚀敷有铜箔的绝缘板制印刷电路板,为了从使用过的废腐蚀液中回收铜,并重新得到 FeCl3溶液,设计如下实验流程:
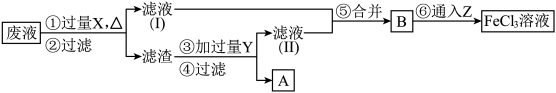
上述流程中,所加试剂的化学式为:X_____ ,Y_________ ,Z_____ ;第⑥步反应的离子方程 式为_____________________________ 。

上述流程中,所加试剂的化学式为:X
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁和铝是日常生活中用途广泛的金属。
I.(1)向NaAlO2溶液中滴加AlCl3溶液,生成白色胶状沉淀,则发生反应的离子方程式为_________________________ 。
(2)实验室常用还原性 Fe 粉与水蒸气反应的实验来研究 Fe 的还原性,则该反应的化学方程式为_________________________ 。
(3)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________________ 。
II.已知合金A由两种常见金属组成。为测定其组成,某同学的实验流程如图所示:
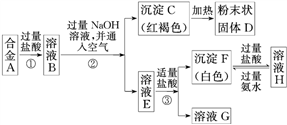
请回答:
(4)溶液E中所含的溶质是_________________ (写化学式)
(5)合金A中的一种金属可以与粉末状固体D在高温下反应生成合金A中的另一种金属,请写出该反应的化学方程式_____________________________ 。
I.(1)向NaAlO2溶液中滴加AlCl3溶液,生成白色胶状沉淀,则发生反应的离子方程式为
(2)实验室常用还原性 Fe 粉与水蒸气反应的实验来研究 Fe 的还原性,则该反应的化学方程式为
(3)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
II.已知合金A由两种常见金属组成。为测定其组成,某同学的实验流程如图所示:

请回答:
(4)溶液E中所含的溶质是
(5)合金A中的一种金属可以与粉末状固体D在高温下反应生成合金A中的另一种金属,请写出该反应的化学方程式
您最近一年使用:0次



