填空:
(1)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:______________ 。






配制KMnO4溶液,定容的操作方法为_______________________ 。
(2)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是__________ (填化学方程式)。
(3)写出Na2SO4和NaCl混合溶液中 的检验方法:
的检验方法:___________________ 。
(4)从硫酸亚铁溶液中获得硫酸亚铁晶体FeSO4•7H2O的实验操作为__________ 、__________ 、过滤、冰水洗涤、烘干。取27.8g FeSO4•7H2O隔绝空气加热至不同温度,剩余固体的质量变化如图所示。
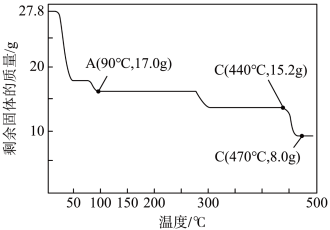
分析数据,写出90℃残留物的化学式:__________ ;440~470℃时固体物质发生反应的化学方程式是________________________ 。
(1)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:






配制KMnO4溶液,定容的操作方法为
(2)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是
(3)写出Na2SO4和NaCl混合溶液中
 的检验方法:
的检验方法:(4)从硫酸亚铁溶液中获得硫酸亚铁晶体FeSO4•7H2O的实验操作为

分析数据,写出90℃残留物的化学式:
更新时间:2023-10-04 15:00:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氨在国防、工农业等领域发挥着重要作用。某实验兴趣小组在实验室模拟工业制氨气,在400℃、2.8MPa时,将一定量N2和H2的混合气体充入一密闭容器中,发生反应N2(g)+3H2(g)⇌2NH3(g) ΔH<0。
回答下列问题:
(1)该反应的反应物的键能总和___________ (填“大于”或“小于”)生成物的键能总和。
(2)为了提高NH3的产率,可采用___________ (填一种即可)的方法。
(3)下列说法正确的是___________ (填标号)。
A.升高温度,该反应的反应速率加快,平衡常数减小
B.加入合适的催化剂,N2的转化率保持不变
C.n(N2):n(H2):n(NH3)=1:3:2时,该反应达到平衡状态
(4)每断裂0.6molH-H键,同时形成___________ molN-H键,转移的电子数为___________ NA,消耗___________ molN2。
回答下列问题:
(1)该反应的反应物的键能总和
(2)为了提高NH3的产率,可采用
(3)下列说法正确的是
A.升高温度,该反应的反应速率加快,平衡常数减小
B.加入合适的催化剂,N2的转化率保持不变
C.n(N2):n(H2):n(NH3)=1:3:2时,该反应达到平衡状态
(4)每断裂0.6molH-H键,同时形成
您最近一年使用:0次
【推荐2】由化合物E与乙二酸恰好完全反应生成1mol单一聚合度的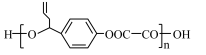 ,若生成H2O的质量为378g,则该聚合物的n值理论上应等于
,若生成H2O的质量为378g,则该聚合物的n值理论上应等于_______ 。
 ,若生成H2O的质量为378g,则该聚合物的n值理论上应等于
,若生成H2O的质量为378g,则该聚合物的n值理论上应等于
您最近一年使用:0次
【推荐3】(I)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的氧化产物是______ 。
(2)写出并配平该反应的化学方程式,______ 。
(II)氰[(CN)2]、硫氰[(SCN)2]的化学性质和卤素很相似,化学上称为拟卤素。如:(SCN)2+H2O=HSCN+HSCNO,它们的阴离子的还原性强弱为Cl-<Br-<CN-<SCN-<I-,试写出:NaBr和KSCN的混合溶液中加入(CN)2,反应的离子方程式____________________________ 。
(III)A、B两个烧杯中分别装有80mL 3.0mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体体积比为A:B=2:5,则加入的铝粉质量为_______ 。
(IV)准确称取某种铁的氧化物2.88g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4g,则这种铁的氧化物为____________ 。
A. Fe3O4 B. Fe2O3 C. FeO D.以上都不是
(1)该反应中的氧化产物是
(2)写出并配平该反应的化学方程式,
(II)氰[(CN)2]、硫氰[(SCN)2]的化学性质和卤素很相似,化学上称为拟卤素。如:(SCN)2+H2O=HSCN+HSCNO,它们的阴离子的还原性强弱为Cl-<Br-<CN-<SCN-<I-,试写出:NaBr和KSCN的混合溶液中加入(CN)2,反应的离子方程式
(III)A、B两个烧杯中分别装有80mL 3.0mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体体积比为A:B=2:5,则加入的铝粉质量为
(IV)准确称取某种铁的氧化物2.88g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4g,则这种铁的氧化物为
A. Fe3O4 B. Fe2O3 C. FeO D.以上都不是
您最近一年使用:0次
【推荐1】已知:还原性HSO3->I-,氧化性IO3-> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目_______ 。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为_______ (填化学式);
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式_______ ;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为_______ mol。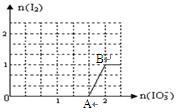
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式

您最近一年使用:0次
【推荐2】I.过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。对于下列AD涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2Cr2O4+3K2SO4+8H2O
(1)上述反应属于氧化还原反应的是____ (填代号)。
(2)H2O2仅体现氧化性的反应是____ (填代号)。
(3)KMnO4和H2O2能在酸性条件下发生氧化还原反应,反应前后涉及到的粒子有MnO 、Mn2+、H2O2、H+、H2O、O2,请写出该氧化还原反应的离子方程式:
、Mn2+、H2O2、H+、H2O、O2,请写出该氧化还原反应的离子方程式:____ 。
II.亚硝酸钠(NaNO2)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究NaNO2的性质。
(4)实验操作如表所示,请完善表格中的实验现象和结论(已知I2遇淀粉变蓝)。
③写出实验3中发生反应的化学方程式:____ 。
④实验2中化学反应方程式如下,请用双线桥表示电子转移情况____ 。
5NaNO2+3H2SO4+2KMnO4=5NaNO3+2MnSO4+K2SO4+3H2O
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2Cr2O4+3K2SO4+8H2O
(1)上述反应属于氧化还原反应的是
(2)H2O2仅体现氧化性的反应是
(3)KMnO4和H2O2能在酸性条件下发生氧化还原反应,反应前后涉及到的粒子有MnO
 、Mn2+、H2O2、H+、H2O、O2,请写出该氧化还原反应的离子方程式:
、Mn2+、H2O2、H+、H2O、O2,请写出该氧化还原反应的离子方程式:II.亚硝酸钠(NaNO2)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究NaNO2的性质。
(4)实验操作如表所示,请完善表格中的实验现象和结论(已知I2遇淀粉变蓝)。
| 实验 | 实验操作及现象或结果 | 结论 |
| 1 | 取5mLNaNO2溶液于试管中,加入少量淀粉-KI溶液,充分反应后,观察到① | NaNO2具有氧化性 |
| 2 | 取2mLKMnO4溶液(先用硫酸酸化)于试管中,滴加足量的NaNO2溶液,可观察到② | NaNO2具有还原性 |
| 3 | NaNO2固体与70%硫酸反应生成了NO和NO2两种气体 | NaNO2既有氧化性又有还原性 |
③写出实验3中发生反应的化学方程式:
④实验2中化学反应方程式如下,请用双线桥表示电子转移情况
5NaNO2+3H2SO4+2KMnO4=5NaNO3+2MnSO4+K2SO4+3H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂是__ 。(填化学式)
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:___ 。
②每生成2molFeO42-转移_______ mol电子,若反应过程中转移了0.5mol电子,则还原产物的物质的量为___ mol。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成2molFeO42-转移
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断正误:
1.能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2。(_______)
2.用硝酸酸化的硝酸银溶液能一次鉴别NaCl、NaBr、KI三种失去标签的溶液。(_______)
3.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-。(_______)
4.某浅黄色的溴水,加入CCl4振荡静置后,上层显橙红色。(_______)
5.溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯。(_______)
6.溴化银具有感光性,碘化银不具有感光性。(_______)
7.氟气跟氯化钠水溶液反应,一定有氟化氢和氧气生成。(_______)
8.海水中提取溴涉及不止一个氧化还原反应。(_______)
1.能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2。(_______)
2.用硝酸酸化的硝酸银溶液能一次鉴别NaCl、NaBr、KI三种失去标签的溶液。(_______)
3.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-。(_______)
4.某浅黄色的溴水,加入CCl4振荡静置后,上层显橙红色。(_______)
5.溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯。(_______)
6.溴化银具有感光性,碘化银不具有感光性。(_______)
7.氟气跟氯化钠水溶液反应,一定有氟化氢和氧气生成。(_______)
8.海水中提取溴涉及不止一个氧化还原反应。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】阅读下列科普短文并填空:
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如NaCl①,MgSO4②等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水③用以生产NaOH④、NaHCO3⑤、NaClO⑥、Cl2⑦、盐酸⑧等,苦卤经过氯气氧化、热空气吹出、SO2⑨吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼金属钠⑩。海底埋藏大量可燃冰资源,甲烷⑪是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是____________ (填序号);
(2)写出⑤溶于水的电离方程式:__________________ 。
将⑦通入④的溶液中,写出离子反应方程式__________________ 。
将⑨通入足量④的溶液中,写出离子反应方程式__________________ 。
将⑩投入②的溶液,写出离子反应方程式__________________ 。
(3)海水提溴的过程中涉及的反应有 ,
, ,根据上述反应可判断
,根据上述反应可判断 ,
, ,SO2、的还原性由强到弱的顺序为
,SO2、的还原性由强到弱的顺序为__________________ 。
(4)实验室检验自来水中含有氯离子的化学试剂为____________ 。
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如NaCl①,MgSO4②等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水③用以生产NaOH④、NaHCO3⑤、NaClO⑥、Cl2⑦、盐酸⑧等,苦卤经过氯气氧化、热空气吹出、SO2⑨吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼金属钠⑩。海底埋藏大量可燃冰资源,甲烷⑪是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
将⑦通入④的溶液中,写出离子反应方程式
将⑨通入足量④的溶液中,写出离子反应方程式
将⑩投入②的溶液,写出离子反应方程式
(3)海水提溴的过程中涉及的反应有
 ,
, ,根据上述反应可判断
,根据上述反应可判断 ,
, ,SO2、的还原性由强到弱的顺序为
,SO2、的还原性由强到弱的顺序为(4)实验室检验自来水中含有氯离子的化学试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是生活生产中常见的物质,表中列出了它们的化学式或主要成分,按要求填空:
(1)写出Fe粉与水蒸气反应制备少量磁性氧化铁的化学方程式:___________ ,②~⑥中属于电解质的是___________ (填序号)。
(2)次氯酸可用作棉、麻、纸张的漂白剂,但不稳定易分解,写出次氯酸在光照下分解的离子方程式:___________ 。
(3)次氯酸不稳定,人们制得了有漂白作用且较稳定的次氧酸盐,如将Cl2通入冷的石灰乳即可制得漂白粉,对应的化学方程式为___________ ,漂白粉的有效成分为___________ ,漂白粉在空气中久置也会变质,描述其变质原理:___________ 。
(4)胃舒平和小苏打均可用于治疗胃酸过多,写出治疗过程属于中和反应的离子方程式:___________ 。
| 名称 | 磁性氧化铁 | 次氯酸 | 胃舒平 | 小苏打 | 石灰乳 | 酒精 |
| 化学式或主要成分 | ①Fe3O4 | ②HClO | ③Al(OH)3 | ④NaHCO3 | ⑤Ca(OH)2 | ⑥C2H5OH |
(2)次氯酸可用作棉、麻、纸张的漂白剂,但不稳定易分解,写出次氯酸在光照下分解的离子方程式:
(3)次氯酸不稳定,人们制得了有漂白作用且较稳定的次氧酸盐,如将Cl2通入冷的石灰乳即可制得漂白粉,对应的化学方程式为
(4)胃舒平和小苏打均可用于治疗胃酸过多,写出治疗过程属于中和反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“生活无处不化学”,请你回答下列问题。
(1)小苏打可以治疗胃酸过多,用离子方程式表示其原理___________ 。
(2)使用“84消毒液(含NaClO)时,按一定比例与水混合,放置一段时间,其杀菌消毒的效果增强,用化学方程式表示其原理___________ 。
(3)食盐的精制,需要将粗盐中含有的SO 、Mg2+、Ca2+离子沉淀除去,进行提纯,下列加入试剂的顺序不可行的是
、Mg2+、Ca2+离子沉淀除去,进行提纯,下列加入试剂的顺序不可行的是___________ 。
A.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤→盐酸
B.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤→盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
D.BaCl2溶液→Na2CO3溶液→NaOH溶液→过滤→盐酸
(4)用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3(难溶于水),潮湿的FeCO3固体置于空气中易变质,反应为4FeCO3+6H2O+O2=4X+4CO2。则X的化学式为___________ 。
(5)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是___________ 。
(1)小苏打可以治疗胃酸过多,用离子方程式表示其原理
(2)使用“84消毒液(含NaClO)时,按一定比例与水混合,放置一段时间,其杀菌消毒的效果增强,用化学方程式表示其原理
(3)食盐的精制,需要将粗盐中含有的SO
 、Mg2+、Ca2+离子沉淀除去,进行提纯,下列加入试剂的顺序不可行的是
、Mg2+、Ca2+离子沉淀除去,进行提纯,下列加入试剂的顺序不可行的是A.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤→盐酸
B.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤→盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
D.BaCl2溶液→Na2CO3溶液→NaOH溶液→过滤→盐酸
(4)用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3(难溶于水),潮湿的FeCO3固体置于空气中易变质,反应为4FeCO3+6H2O+O2=4X+4CO2。则X的化学式为
(5)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一些物质的分类如图,根据所学知识填空。
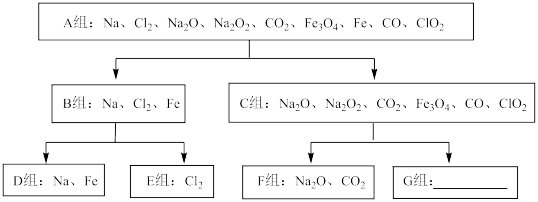
(1)A组物质中属于碱性氧化物的电解质是____ 。
(2)B组中两种金属均可在氯气中燃烧,lmolCl2分别与足量金属钠、铁粉充分反应,理论上转移电子数分别为____ mol和____ mol。
(3)D组中两种单质均能与H2O反应,分别写出反应的方程式____ 、____ (属于离子反应的写离子方程式)。
(4)C组物质中,一种淡黄色固体与另一种氧化物反应,产生一种能使带火星木条复燃的气体,写出化学反应方程式并用双线桥标明电子转移的方向和数目_____ ,氧化剂和还原剂物质的量之比为____ 。C组物质还可按另一标准分成H、I两组(每组各有3种物质),分类标准是_____ 。
(5)F组为酸性或碱性氧化物,写出另一种同类别且常温下可与水反应的氧化物的化学式____ 。写出G组中一种物质及其用途_____ 。

(1)A组物质中属于碱性氧化物的电解质是
(2)B组中两种金属均可在氯气中燃烧,lmolCl2分别与足量金属钠、铁粉充分反应,理论上转移电子数分别为
(3)D组中两种单质均能与H2O反应,分别写出反应的方程式
(4)C组物质中,一种淡黄色固体与另一种氧化物反应,产生一种能使带火星木条复燃的气体,写出化学反应方程式并用双线桥标明电子转移的方向和数目
(5)F组为酸性或碱性氧化物,写出另一种同类别且常温下可与水反应的氧化物的化学式
您最近一年使用:0次



