下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是__________ ,原子半径最小的是_________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是_________________ 。
(4)元素⑦的氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为__________ 和__________ 。①和⑨两元素形成化合物中化学键的类型为____________ ,该化合物灼烧时焰色为_________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑨的最高价氧化物对应的水化物化学式为
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
19-20高一下·新疆哈密·期中 查看更多[6]
新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练河南省新蔡县第一高级中学2020-2021学年高一下学期5月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题(已下线)专题17 化学键(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练福建省政和县第二中学2022-2023学年高一下学期第一次月考化学试题
更新时间:2021-01-20 07:27:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
(1)用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为_________________ 。
(2)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],发生反应的离子方程式为________________________________
(1)用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
(2)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】正确使用药物是维持身体健康的关键。下列是几种常用的药物:
A.青霉素 B.麻黄碱 C.阿司匹林 D.抗酸药(含氢氧化铝)
请根据题意,选择恰当的选项,用其字母代号填空:
(1)具有解热镇痛作用,用于治疗感冒的是____ 。
(2)____ 是最重要的抗生素,在注射之前,需要进行皮肤敏感试验。
(3)对支气管哮喘症有明显疗效的是_____ 。
(4)可用于治疗胃酸过多症的药物是____ ,其发挥功效时的化学方程式为____ 。
A.青霉素 B.麻黄碱 C.阿司匹林 D.抗酸药(含氢氧化铝)
请根据题意,选择恰当的选项,用其字母代号填空:
(1)具有解热镇痛作用,用于治疗感冒的是
(2)
(3)对支气管哮喘症有明显疗效的是
(4)可用于治疗胃酸过多症的药物是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】元素周期表是打开物质世界奥秘之门的一把金钥匙,1869年门捷列夫发现了元素周期律并发表元素周期表。下图为元素周期表的一部分回答下列问题。

(1)上述元素中化学性质最稳定的是_______ (填元素符号下同),金属性最强的是_______ 。
(2)b、c的最高价氧化物对应水化物中,酸性更强的是_______ (用化学式表示),d、e形成的简单阴离子中,还原性更强的是_______ (用离子符号表示)。
(3)h元素的原子结构示意图是_______ ,写出h元素最高价氧化物的一种用途_______ 。
(4)d、e、f三种元素原子半径由大到小的顺序是_______ (用化学符号表示)。
(5)写出j的最高价氧化物对应水化物与g的最高价氧化物对应水化物反应的离子方程式_______ 。
(6)12gb单质在足量d单质中燃烧,所得气体通入 的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是
的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是_______ 。

(1)上述元素中化学性质最稳定的是
(2)b、c的最高价氧化物对应水化物中,酸性更强的是
(3)h元素的原子结构示意图是
(4)d、e、f三种元素原子半径由大到小的顺序是
(5)写出j的最高价氧化物对应水化物与g的最高价氧化物对应水化物反应的离子方程式
(6)12gb单质在足量d单质中燃烧,所得气体通入
 的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是
的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分:
请回答下列问题:
(1)Z元素在周期表中的位置为________________ 。
(2)表中元素原子半径最大的是(写元素符号)________________ 。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是________ (填序号)。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol·L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为______________________________ ,生成硫酸铜物质的量为_______________________ 。
| 碳 | 氮 | Y | |
| X | 硫 | Z |
请回答下列问题:
(1)Z元素在周期表中的位置为
(2)表中元素原子半径最大的是(写元素符号)
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol·L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2019年是元素周期表诞生150周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
(1)元素①~⑧中,金属性最强的是________ (填元素符号)。
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是_________ ,其氢化物的电子式是_________ 。
(3)比较元素②、③的最高价氧化物对应水化物的酸性:______ >______ (填化学式)。说明你判断的理由:_________ 。
(4)主族元素砷(As)的部分信息如图所示。

①砷(As)在周期表中的位置是______ 。
②下列说法正确的是_______ (填序号)。
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。已知:常温下浓盐酸与高锰酸钾反应生成氯气。
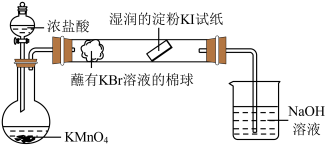
打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br >I,并说明理由_________ 。
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ||||||||
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是
(3)比较元素②、③的最高价氧化物对应水化物的酸性:
(4)主族元素砷(As)的部分信息如图所示。

①砷(As)在周期表中的位置是
②下列说法正确的是
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。已知:常温下浓盐酸与高锰酸钾反应生成氯气。

打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br >I,并说明理由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)若元素X和Y的核电荷数都小于18,最外层电子数分别为n和(m-5),次外层分别有(n+2)个和m个电子。据此推断元素X的名称为_______ ;Y的离子结构示意图为_______ 。
(2)不能比较或判断S、Cl的非金属性强弱的是_______ (填字母)。
a. 、
、 的还原性
的还原性
b.氯酸和硫酸的酸性
c.电子层数相同,S、Cl的原子半径
d.氯化氢和硫化氢溶液的酸性强弱
(3)原子序数为12、13、16、17的元素原子形成的简单离子,离子半径由大到小的顺序是(用离子符号表示)_______ 。
(4)已知X为第IA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第VIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。
(5)推测52号元素在元素周期表中的位置为_______ 。
(6)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O相互结合为二氧化碳,可得二氧化碳分子的种数为_______ 。
(1)若元素X和Y的核电荷数都小于18,最外层电子数分别为n和(m-5),次外层分别有(n+2)个和m个电子。据此推断元素X的名称为
(2)不能比较或判断S、Cl的非金属性强弱的是
a.
 、
、 的还原性
的还原性b.氯酸和硫酸的酸性
c.电子层数相同,S、Cl的原子半径
d.氯化氢和硫化氢溶液的酸性强弱
(3)原子序数为12、13、16、17的元素原子形成的简单离子,离子半径由大到小的顺序是(用离子符号表示)
(4)已知X为第IA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第VIIA族元素,则Y的原子序数b与a所有可能的关系式为
(5)推测52号元素在元素周期表中的位置为
(6)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O相互结合为二氧化碳,可得二氧化碳分子的种数为
您最近一年使用:0次
【推荐2】氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响。如氧气、水、二氧化硫等。
(1)氧族元素原子最外层电子数与次外层中p亚层电子数相同的元素名称是___ ;硫单质常见形式是S8,它的摩尔质量是___ ;Se是人体不可或缺的微量元素,它在周期表中的位置是___ ,Se原子最外层轨道表示式___ 。
(2)在氧、硫、硒(Se)、碲(Te)元素原子形成的简单阴离子中,其离子半径由大到小的顺序为__ (用离子符号表示)。用化学方程式表示SO2形成硫酸型酸雨的反应__ 。
(3)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是___
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(4)亚硫酸钠和碘酸钾在酸性溶液里反应生成硫酸钠、硫酸钾、碘和水。
__ Na2SO3+__ KIO3+__ H2SO4
__ Na2SO4+__ K2SO4+__ I2+_ H2O配平该反应,若反应中有0.5mol电子转移,则生成的碘是___ g。
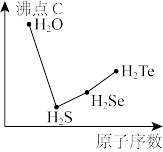
(5)从图中可知氧族元素氢化物的沸点变化规律是__ 。
(1)氧族元素原子最外层电子数与次外层中p亚层电子数相同的元素名称是
(2)在氧、硫、硒(Se)、碲(Te)元素原子形成的简单阴离子中,其离子半径由大到小的顺序为
(3)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(4)亚硫酸钠和碘酸钾在酸性溶液里反应生成硫酸钠、硫酸钾、碘和水。

(5)从图中可知氧族元素氢化物的沸点变化规律是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。

(1)上述所有元素的最高价氧化物对应水化物中,碱性最强的水化物是_______ (用化学式表示,下同)。
(2)b、c、d的简单离子半径由大到小的顺序为_______ 。
(3)b、f、g的简单氢化物中,稳定性最弱的是_______ 。
(4)设计由NaCl、AlCl3的混合溶液制取Al2O3固体的实验方案:_______ 。(实验中可以选用的试剂是盐酸、氨水和NaOH溶液)
(5)j是元素周期表中第32号元素。
①j在周期表中的位置是_______ 。
②j及其化合物的性质正确的是_______ (填字母)。
A.j的单质常温下为气体
B.j的单质可用于制半导体
C.j的单质可能具有强氧化性
D.j的最高价氧化物对应水化物的酸性比H3PO4弱

(1)上述所有元素的最高价氧化物对应水化物中,碱性最强的水化物是
(2)b、c、d的简单离子半径由大到小的顺序为
(3)b、f、g的简单氢化物中,稳定性最弱的是
(4)设计由NaCl、AlCl3的混合溶液制取Al2O3固体的实验方案:
(5)j是元素周期表中第32号元素。
①j在周期表中的位置是
②j及其化合物的性质正确的是
A.j的单质常温下为气体
B.j的单质可用于制半导体
C.j的单质可能具有强氧化性
D.j的最高价氧化物对应水化物的酸性比H3PO4弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】元素单质及其化合物有广泛用途,请根据周期表中第3周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是___________ 。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___________ ,氧化性最弱的简单阳离子是___________ 。
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是___________ ;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是___________ 。
a.NH3 b.HI c.SO2 d.CO2
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】五种短周期元素的某些性质如表所示(请用相应的元素符号或化学式作答)
(1)R元素在元素周期表中的位置∶第_______ 周期,第_______ 族。
(2)用电子式表示W与Y形成化合物W2Y的过程_______
(3)Q、W、Y的离子半径由大到小的顺序为_______ ,1molR4中含有共价键数目为_______ 。
(4)X2Z2的结构式_______ ,WYZ的电子式_______ 。
(5)W3Q与WZ还原性强弱为W3Q_______ WZ(填">"、"<"或"="),WZ溶于Z2Y的化学方程式为_______ 。
(6)Z2Y2能使硫酸酸化的KMnO4溶液褪色,写出该反应的离子方程式_______ 。
| 元素 | 元素的相关信息 |
| Q | 最高价氧化物对应的水化物能与其气态氢化物发生化合反应生成盐 |
| R | 其最高价和最低价的代数和为2 |
| W | 在短周期元素中,其原子半径最大 |
| X | 其原子的最外层电子数是次外层电子数的2倍, Y是地壳中含量最多的元素 |
| Z | 是元素周期表中原子半径最小的元紫 |
(2)用电子式表示W与Y形成化合物W2Y的过程
(3)Q、W、Y的离子半径由大到小的顺序为
(4)X2Z2的结构式
(5)W3Q与WZ还原性强弱为W3Q
(6)Z2Y2能使硫酸酸化的KMnO4溶液褪色,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36 号元素),对 比中学常见元素周期表思考扇形元素周期表的 填充规律,并用化学用语.回答下列问题:
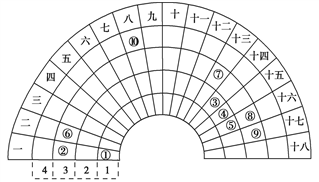
(1)若①~⑩分别代表十种元素,则⑧代表的元素在常见周期表中的位置是____________
(2)比较元素最高价氧化物对应水化物的碱性:②_____________ ⑥(填“>”或“<”)
(3)写出一种由①、④、⑤三种元素形成的常见离子化合物:___________ ,设计一个简单的实验检验其阳离子的存在:___________________ 。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________ 。
(5)①、③、⑤三种元素形成的18 电子结构的化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②的最高价氧化物对应的水化物作电解质的燃料电池的负极反应式:_________ 。

(1)若①~⑩分别代表十种元素,则⑧代表的元素在常见周期表中的位置是
(2)比较元素最高价氧化物对应水化物的碱性:②
(3)写出一种由①、④、⑤三种元素形成的常见离子化合物:
(4)用电子式表示⑥、⑨形成化合物的过程:
(5)①、③、⑤三种元素形成的18 电子结构的化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②的最高价氧化物对应的水化物作电解质的燃料电池的负极反应式:
您最近一年使用:0次



