人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
(1)用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为_________________ 。
(2)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],发生反应的离子方程式为________________________________
(1)用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
(2)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],发生反应的离子方程式为
更新时间:2019-12-09 15:34:30
|
相似题推荐
填空题
|
适中
(0.65)
真题
【推荐1】为确定Na2CO3和NaHCO3混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度盐酸30.0 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积,不考虑CO2在水中的溶解)如下表:
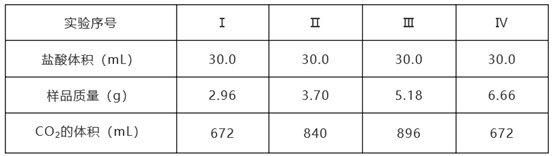
(1)样品中物质的量之比n(Na2CO3):n(NaHCO3)=_________ 。
(2)盐酸的物质的量浓度c(HCl)=______________ 。

(1)样品中物质的量之比n(Na2CO3):n(NaHCO3)=
(2)盐酸的物质的量浓度c(HCl)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原科,实验室常用 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数为_______ 个,此时被氧化的物质的物质的量为_______ mol。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ 。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(1)氯气是重要的化工原科,实验室常用
 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上产生的硫化氢要经过处理变成硫单质后方能排放,以防止大气污染。富玛克斯法治理硫化氢的方法和步骤如下:
①用2%~3%的Na2CO3溶液作吸收剂生成2种酸式盐;
②再加入一种RNO(液)(R表示芳香烃基)与生成的一种酸式盐的水溶液反应生成硫、碱和RNHOH;
③第②步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④RNHOH与空气中的氧发生反应又得到RNO。
(1)写出上述四步反应的化学方程式_______ 。
(2)请对富玛克斯法的优点做一简要评价_______ 。
①用2%~3%的Na2CO3溶液作吸收剂生成2种酸式盐;
②再加入一种RNO(液)(R表示芳香烃基)与生成的一种酸式盐的水溶液反应生成硫、碱和RNHOH;
③第②步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④RNHOH与空气中的氧发生反应又得到RNO。
(1)写出上述四步反应的化学方程式
(2)请对富玛克斯法的优点做一简要评价
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学与生活密切相关。回答下列问题:
(1)Na2O2常用于解决潜艇的供氧问题。Na2O2降低潜艇内CO2浓度化学方程式表示为_______ 。
(2)NaHCO3的水溶液呈碱性,常用于处理食品生产中面粉过度发酵产生的有机酸(HA),又能使面食疏松多孔,有关反应的化学方程式为_______ 。
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为_______ ;漂白粉的有效成分是(填化学式)_______ 。
(4)漂白液的主要成分是NaClO和NaCl。其中的NaClO久置于空气中易失效的原因是_______ (用语言描述)。
(1)Na2O2常用于解决潜艇的供氧问题。Na2O2降低潜艇内CO2浓度化学方程式表示为
(2)NaHCO3的水溶液呈碱性,常用于处理食品生产中面粉过度发酵产生的有机酸(HA),又能使面食疏松多孔,有关反应的化学方程式为
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(4)漂白液的主要成分是NaClO和NaCl。其中的NaClO久置于空气中易失效的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】胃酸(主要成分为盐酸)过多是常见的胃病。甲、乙两种中学课本中用以治疗胃酸过多的常见胃药,以下是它们的说明摘要。
甲:(1)白色结晶状粉末,可缓缓分解;
(2)能溶于水,水溶液呈弱碱性;
(3)遇酸及酸性药物则产生二氧化碳;
乙:(1)与胃酸是中和作用缓慢而持久,可维持3~4小时。
(2)凝胶本身覆盖于溃疡面上,具有保护作用。
(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是___________________ (填中文名称);乙中含有的主要化学成分是_______________________ (填化学式)。
(2)试写出甲中含有的主要化学成分引起胃胀气反应的化学方程式:______________ 。
(3)试写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式:
__________________________ ;___________________________________ 。
甲:(1)白色结晶状粉末,可缓缓分解;
(2)能溶于水,水溶液呈弱碱性;
(3)遇酸及酸性药物则产生二氧化碳;
乙:(1)与胃酸是中和作用缓慢而持久,可维持3~4小时。
(2)凝胶本身覆盖于溃疡面上,具有保护作用。
(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是
(2)试写出甲中含有的主要化学成分引起胃胀气反应的化学方程式:
(3)试写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】金属钠及其化合物的用途广泛。请根据所学知识,回答下列问题:
I.
(1)钠与水反应过程中可看到钠熔成闪亮的小球,产生这一现象的原因是___________ ,写出金属钠与水反应的化学方程式:___________ 。
(2)氢氧化钠溶液露置在空气中易变质,写出反应的离子方程式:___________ ,用无色酚酞试液___________ (填“能”或“不能”)判断 溶液的变质情况,其理由是
溶液的变质情况,其理由是___________ 。
II.将 、
、 的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
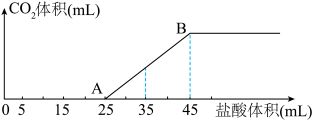
已知:逐滴将盐酸加入碳酸钠溶液中时,盐酸先与碳酸钠反应生成碳酸氢钠。
(3)AB段发生反应的化学方程式为___________ 。
(4)当加入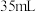 盐酸时,产生
盐酸时,产生 的体积(标准状况)为
的体积(标准状况)为___________ mL。
(5)原固体混合物中 与
与 的物质的量之比为
的物质的量之比为___________ 。
I.
(1)钠与水反应过程中可看到钠熔成闪亮的小球,产生这一现象的原因是
(2)氢氧化钠溶液露置在空气中易变质,写出反应的离子方程式:
 溶液的变质情况,其理由是
溶液的变质情况,其理由是II.将
 、
、 的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
已知:逐滴将盐酸加入碳酸钠溶液中时,盐酸先与碳酸钠反应生成碳酸氢钠。
(3)AB段发生反应的化学方程式为
(4)当加入
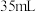 盐酸时,产生
盐酸时,产生 的体积(标准状况)为
的体积(标准状况)为(5)原固体混合物中
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是__________ ,原子半径最小的是_________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是_________________ 。
(4)元素⑦的氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为__________ 和__________ 。①和⑨两元素形成化合物中化学键的类型为____________ ,该化合物灼烧时焰色为_________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑨的最高价氧化物对应的水化物化学式为
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某同学欲检验抗酸药中是否含有Al(OH)3,操作如下:取药剂3~4片研碎,向样品中加入过量的盐酸,过滤,得澄清溶液,向澄清溶液中滴加NaOH溶液,观察到有白色沉淀,继续加过量NaOH溶液,白色沉淀又溶解。你能得出该抗酸药中是否含有Al(OH)3?______________________ (填含或不含),请写出有关反应的化学方程式:
①__________________________________
②__________________________________
③___________________________________
①
②
③
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠、铝、铁是三种重要的金属,三种金属及其化合物在生活生产中有重要作用。请回答下列问题:
(1)将一小块钠投入到CuCl2溶液中,观察到的现象是____ 。
(2)工业上通过以下反应生产高铁酸钠(Na2FeO4):3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O,此反应中氧化剂和还原剂的物质的量之比为____ 。
(3)胃舒平是日常生活中常用的抗酸药,其成分含有Al(OH)3,其抗酸原理是(用离子方程式表示)____ 。
(4)Fe在Cl2燃烧,所得产物的化学式是____ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成____ 色。
b.向另一支试管中滴加NaOH溶液,其反应的化学方程式为____ 。
(5)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100 mL2 mol·L-1的盐酸,恰好完全反应,放出11.2 mL(标准状况)气体,所得溶液加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的此混合物,所得铁的质量为____ g。
(1)将一小块钠投入到CuCl2溶液中,观察到的现象是
| A.钠溶解,有铜析出并有气体产生 | B.只有气体产生 |
| C.只有沉淀产生 | D.既有气体产生,又有蓝色沉淀产生 |
(3)胃舒平是日常生活中常用的抗酸药,其成分含有Al(OH)3,其抗酸原理是(用离子方程式表示)
(4)Fe在Cl2燃烧,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,其反应的化学方程式为
(5)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100 mL2 mol·L-1的盐酸,恰好完全反应,放出11.2 mL(标准状况)气体,所得溶液加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的此混合物,所得铁的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】营养平衡、科学使用食品添加剂有助于健康和提高免疫力。
①向食品中加入调味剂,能改善或改变食品的口味,下列不属于调味剂的是________ (填字母)。
a.食盐 b.辣椒粉 c.小苏打
②人体如果缺乏某种微量元素将导致血液输送氧气的能力下降,人体内就无法获得充足的氧气,生理机能就会下降,儿童还可能会智力发育迟缓,该微量元素是_____ (填字母)。
a.碘 b.锌 c.铁
③抗生素是能抑制某些微生物生长或能杀灭某些微生物的一类物质,下列属于抗生素的是_______ (填字母)。
a.阿莫西林 b.胃舒平 c.阿司匹林
①向食品中加入调味剂,能改善或改变食品的口味,下列不属于调味剂的是
a.食盐 b.辣椒粉 c.小苏打
②人体如果缺乏某种微量元素将导致血液输送氧气的能力下降,人体内就无法获得充足的氧气,生理机能就会下降,儿童还可能会智力发育迟缓,该微量元素是
a.碘 b.锌 c.铁
③抗生素是能抑制某些微生物生长或能杀灭某些微生物的一类物质,下列属于抗生素的是
a.阿莫西林 b.胃舒平 c.阿司匹林
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】科学家通过乙二醇的桥梁作用把阿司匹林连接在高聚物上,制成缓释长效阿司匹林,用于关节炎和冠心病的辅助治疗,缓释长效阿司匹林的结构简式如下:
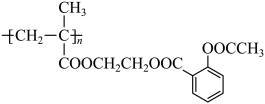
请回答下列问题:
(1)高分子载体的结构简式为___________ 。
(2)阿司匹林连接在高分子载体上的有机反应类型是___________ 。
(3)缓释长效阿司匹林在肠胃中变为阿司匹林的化学方程式是___________ 。
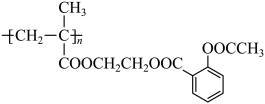
请回答下列问题:
(1)高分子载体的结构简式为
(2)阿司匹林连接在高分子载体上的有机反应类型是
(3)缓释长效阿司匹林在肠胃中变为阿司匹林的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有代表就食品和药品行业存在的问题向“两会”提交议案,得到与会众多代表的关注。
(1)某品牌抗酸药的主要成分有糖衣、氢氧化镁、淀粉。试写出该抗酸药发挥功效时的离子方程式:___ 。
(2)甲状腺肿大俗称“大脖子病”,是由身体缺少______ (填元素符号)所致,该元素属____ (填“常量元素”或“微量元素”)
(3)药物“速力菲”(琥珀酸亚铁薄膜衣片) 适用于明确原因的缺铁性贫血。其主要活性成分是琥珀酸亚铁(含Fe2+ 34.0%-36.0%的无水碱式盐,不溶于水也不溶于乙醇)。性状为薄膜衣片,除去薄膜衣后显 暗黄色。使用时与维生素C同服有利于吸收等。该药品的薄膜衣的作用是______ ,该药品与维生素C同服效果更好,这是因为维生素C具有__ (填“氧化”或“还原”)性,薄膜衣是一种淀粉制品,淀粉在人体内水解最终转化为______ 。
(1)某品牌抗酸药的主要成分有糖衣、氢氧化镁、淀粉。试写出该抗酸药发挥功效时的离子方程式:
(2)甲状腺肿大俗称“大脖子病”,是由身体缺少
(3)药物“速力菲”(琥珀酸亚铁薄膜衣片) 适用于明确原因的缺铁性贫血。其主要活性成分是琥珀酸亚铁(含Fe2+ 34.0%-36.0%的无水碱式盐,不溶于水也不溶于乙醇)。性状为薄膜衣片,除去薄膜衣后显 暗黄色。使用时与维生素C同服有利于吸收等。该药品的薄膜衣的作用是
您最近一年使用:0次



