化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原科,实验室常用 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数为_______ 个,此时被氧化的物质的物质的量为_______ mol。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ 。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(1)氯气是重要的化工原科,实验室常用
 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
更新时间:2022-11-11 23:26:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在旧石器时代晚期,软锰矿(主要成分是MnO2,还含有硅、铁和少量重金属镍的化合物等杂质)就被人们当作颜料用于洞穴的壁画上。工业上常利用软锰矿制备MnSO4溶液,并以MnSO4溶液为原料制取单质锰和四氧化三锰。
(1)MnSO4溶液的制备:
步骤一:往软锰矿浆中通入SO2气体反应制备MnSO4,往往有副产物MnS2O6生成,温度对反应的影响如图所示。为减少MnS2O6的生成,“浸锰”的适宜温度是___________ ;写出反应生成MnSO4的化学方程式:___________ 。

步骤二:①取上述反应后的混合物,调节pH除杂。已知25℃时,Ksp[Fe(OH)3]=4×10-38,欲使铁离子沉淀完全[c(Fe3+)≤1×10-5],应调节溶液pH不低于___________ 。(lg2=0.3)
②过滤除去硅、铁等杂质后,通常用BaS来除去溶液中的镍,pH对除镍效果的影响如图所示。当pH<4.2,pH越小除镍效果越差的原因是___________ 。

(2)制取金属锰:
惰性电极电解硫酸锰溶液制取金属锰的化学方程式为___________ 。工业上也可以用MnO2和Al粉作为原料,用铝热反应来制取金属锰,反应的化学方程式为___________ 。
(3)制取Mn3O4:
利用空气氧化法,用MnSO4溶液制备Mn3O4。在MnSO4溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备Mn3O4。
①写出上述反应的离子方程式:___________ 。
②Mn3O4与浓盐酸共热,有氯气生成,此反应中被氧化和被还原的物质的物质的量之比为___________ 。
(1)MnSO4溶液的制备:
步骤一:往软锰矿浆中通入SO2气体反应制备MnSO4,往往有副产物MnS2O6生成,温度对反应的影响如图所示。为减少MnS2O6的生成,“浸锰”的适宜温度是

步骤二:①取上述反应后的混合物,调节pH除杂。已知25℃时,Ksp[Fe(OH)3]=4×10-38,欲使铁离子沉淀完全[c(Fe3+)≤1×10-5],应调节溶液pH不低于
②过滤除去硅、铁等杂质后,通常用BaS来除去溶液中的镍,pH对除镍效果的影响如图所示。当pH<4.2,pH越小除镍效果越差的原因是

(2)制取金属锰:
惰性电极电解硫酸锰溶液制取金属锰的化学方程式为
(3)制取Mn3O4:
利用空气氧化法,用MnSO4溶液制备Mn3O4。在MnSO4溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备Mn3O4。
①写出上述反应的离子方程式:
②Mn3O4与浓盐酸共热,有氯气生成,此反应中被氧化和被还原的物质的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列10种物质:① ②
② ③
③ 固体 ④
固体 ④ 固体
固体
⑤葡萄糖 ⑥石墨 ⑦ 溶液 ⑧
溶液 ⑧ 气体 ⑨熔融氯化钾 ⑩生理盐水
气体 ⑨熔融氯化钾 ⑩生理盐水
请回答下列问题:
(1)与⑥互为同素异形体的一种物质是___________ (填物质的名称)。
(2)以上物质属盐的有___________ (填序号,下同)。
(3)以上物质属于电解质的有______________________ 。
(4)上述状态下能够导电的物质是______________________ 。
(5)小苏打治疗胃酸过多的离子反应方程式___________________ 。
(6)稀硫酸和澄清石灰水反应的离子反应方程式_________________ 。
(7)配平该离子反应方程式并用双线桥表示电子转移方向和数目__________ 。
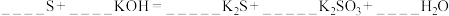
 ②
② ③
③ 固体 ④
固体 ④ 固体
固体⑤葡萄糖 ⑥石墨 ⑦
 溶液 ⑧
溶液 ⑧ 气体 ⑨熔融氯化钾 ⑩生理盐水
气体 ⑨熔融氯化钾 ⑩生理盐水请回答下列问题:
(1)与⑥互为同素异形体的一种物质是
(2)以上物质属盐的有
(3)以上物质属于电解质的有
(4)上述状态下能够导电的物质是
(5)小苏打治疗胃酸过多的离子反应方程式
(6)稀硫酸和澄清石灰水反应的离子反应方程式
(7)配平该离子反应方程式并用双线桥表示电子转移方向和数目
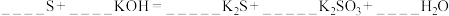
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求写出符合条件的离子方程式:
(1)醋酸与氢氧化钠反应:__________________________________________________________
(2)硝酸银溶液和氯化钠溶液反应:__________________________________________________
(3)铁与稀盐酸反应:______________________________________________________________
(4)氧化铜与稀硫酸反应:__________________________________________________________
(1)醋酸与氢氧化钠反应:
(2)硝酸银溶液和氯化钠溶液反应:
(3)铁与稀盐酸反应:
(4)氧化铜与稀硫酸反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】科学家也在尝试用 作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:
作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:

(1)该过程中,还原剂是_______ (用化学式表示)。
(2)某辆汽车的NO排放量为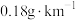 ,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为
,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为_______ g。
 作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:
作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:
(1)该过程中,还原剂是
(2)某辆汽车的NO排放量为
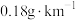 ,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为
,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为
您最近一年使用:0次
【推荐2】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)被还原的元素是__ ,还原剂是__ ,还原产物是__ 。
(2)该反应中的氧化剂与还原剂个数之比是__ 。
(3)完成NaClO3氧化FeCl2的离子方程式:________ ClO +
+________ Fe2++________ H+=________ Cl-+________ Fe3++________ H2O(化学计量数是 1 的也请填上)
(4)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为___ 。
(5)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)═KCl+MnCl2+Cl2↑+H2O(未配平)__ 。
配平该化学方程式:___KMnO4+___HCl═____KCl+__MnCl2+__Cl2↑+__H2O(化学计量数是 1 的也请填上) 并用单线桥 法标出电子转移情况。
(1)被还原的元素是
(2)该反应中的氧化剂与还原剂个数之比是
(3)完成NaClO3氧化FeCl2的离子方程式:
 +
+(4)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
(5)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)═KCl+MnCl2+Cl2↑+H2O(未配平)
配平该化学方程式:___KMnO4+___HCl═____KCl+__MnCl2+__Cl2↑+__H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】神舟十二号飞船携带3名航天员返回地球时,为了减弱返回舱着陆的速度,反推发动机的燃料是高氯酸铵(NH4ClO4)和铝粉混合物。
完成下列填空:
(1)上述燃料涉及的元素所形成的简单离子中,核外电子数相同的离子半径由大到小顺序为___________ (离子符号表示),上述元素的原子中,未成对电子数最多的核外电子排布式为___________ 。
(2)写出 的电子式
的电子式___________ ,其空间构型与甲烷空间构型相同,为___________ 型。
(3)配平以下方程式:____Al+______NH4ClO4→____Al2O3+____AlCl3+_____N2↑+___ H2O___________ 。若产生42g氮气,过程中氮元素转移电子为___________ mol。
完成下列填空:
(1)上述燃料涉及的元素所形成的简单离子中,核外电子数相同的离子半径由大到小顺序为
(2)写出
 的电子式
的电子式(3)配平以下方程式:____Al+______NH4ClO4→____Al2O3+____AlCl3+_____N2↑+___ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)某化学反应可用下式表示:A+B=C+D+H2O,若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式:_________
(2)硝酸铅的稀溶液中,滴入几滴稀 生成白色
生成白色 沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①
沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①_______ ②________
(3)边微热边向铵明矾[NH4Al(SO4)2`12H2O]溶液中逐滴加入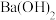 溶液至中性(提示:NH
溶液至中性(提示:NH 、Al3+恰好完全反应)
、Al3+恰好完全反应)
①此时发生反应的离子方程式为_________
②向以上所得中性溶液中继续滴加稀硫酸,相关反应的离子方程式是:____
(2)硝酸铅的稀溶液中,滴入几滴稀
 生成白色
生成白色 沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①
沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①(3)边微热边向铵明矾[NH4Al(SO4)2`12H2O]溶液中逐滴加入
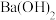 溶液至中性(提示:NH
溶液至中性(提示:NH 、Al3+恰好完全反应)
、Al3+恰好完全反应)①此时发生反应的离子方程式为
②向以上所得中性溶液中继续滴加稀硫酸,相关反应的离子方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO中Cl的化合价为______ ,有较强的______ (填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式______ 。
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为______ ;
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为______ ;
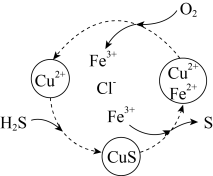
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有______ (写元素符号),Fe2+和Cu2+反应过程中起______ 作用,该图示的总反应的化学方程式为______ 。
(1)NaClO中Cl的化合价为
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有

您最近一年使用:0次
【推荐3】FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】补齐物质与其用途之间的连线。 _________
| 物质 | 用途 |
| A.氧化铁 | a.作红色颜料 |
| B.硝酸钾 | b.作膨松剂 |
| C.次氯酸钠 | c.作肥料 |
| D.碳酸氢钠 | d.作消毒剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学就在我们身边,它与我们的日常生活密切相关。按要求回答以下问题:
(1)明矾可用作净水剂,其化学式是________ ,漂白粉的有效成分是_______ (填化学式)。
(2)小苏打通常用来治疗胃酸过多,请用离子方程式解释原因_________ 。
(3)驰名世界的中国瓷器通常是由黏土经高温烧结而成。黏土的主要成分为 Al2Si2O3(OH)x,式中x=_______ ,若以氧化物形式表示黏土的组成,应写为:_________ 。
(4)洁厕灵(强酸性,含盐酸)与84消毒液(含NaClO)混用可产生一种黄绿色有毒气体,请写出该反应的离子方程式_________ 。
(1)明矾可用作净水剂,其化学式是
(2)小苏打通常用来治疗胃酸过多,请用离子方程式解释原因
(3)驰名世界的中国瓷器通常是由黏土经高温烧结而成。黏土的主要成分为 Al2Si2O3(OH)x,式中x=
(4)洁厕灵(强酸性,含盐酸)与84消毒液(含NaClO)混用可产生一种黄绿色有毒气体,请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空.
(1)可与KSCN溶液反应,溶液变红的是_________ ;
(2)常用于焙制糕点,也可用作抗酸药的是__________ ;
(3)可用于制备硅胶和木材防火剂的是__________ ;
(4)可用于制造计算机芯片的是__________ .
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
请根据题意选择恰当的选项用字母代号填空.
(1)可与KSCN溶液反应,溶液变红的是
(2)常用于焙制糕点,也可用作抗酸药的是
(3)可用于制备硅胶和木材防火剂的是
(4)可用于制造计算机芯片的是
您最近一年使用:0次



