FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
更新时间:2022-12-04 22:21:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为“一些物质与水”的分类图,利用化合价和物质类别预测物质的性质是化学研究的重要手段。

已知:3NO2+H2O =2HNO3+NO
(1)从化学反应类型的角度可以将物质分类。将上述物质分为A、B两组的依据是______________________________________________________________ ,C组物质与水反应时水既不是氧化剂又不是还原剂,则D组物质为_____________ 。
(2)从化合价的角度可以预测Na2O2的性质。
①Na2O2的性质_______________ (填序号)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
②Na2O2以氧化性为主,Na2O2加入含有 的溶液中反应结束后,硫元素存在形式合理的是
的溶液中反应结束后,硫元素存在形式合理的是________________ (填序号)。
a.S2- b.S C. d.
d.
(3)V2O5是钒的重要化合物,工业上多由各种类型的钒矿石提取。根据描述写方程式。
①用氯化焙烧法处理钒铅矿。具体为将食盐和钒铅矿(主要含V2O5)在空气中焙烧,产生黄绿色气体,并生成NaVO3。写出化学方程式______________________________ ;
②V2O5具有微弱的碱性,溶于强酸,当pH=1时生成淡黄色的VO2+的化学方程式_______________________________________________________________________ ; I-能将VO 还原为V3+
还原为V3+_____________________________ (写出对应离子方程式);

已知:3NO2+H2O =2HNO3+NO
(1)从化学反应类型的角度可以将物质分类。将上述物质分为A、B两组的依据是
(2)从化合价的角度可以预测Na2O2的性质。
①Na2O2的性质
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
②Na2O2以氧化性为主,Na2O2加入含有
 的溶液中反应结束后,硫元素存在形式合理的是
的溶液中反应结束后,硫元素存在形式合理的是a.S2- b.S C.
 d.
d.
(3)V2O5是钒的重要化合物,工业上多由各种类型的钒矿石提取。根据描述写方程式。
①用氯化焙烧法处理钒铅矿。具体为将食盐和钒铅矿(主要含V2O5)在空气中焙烧,产生黄绿色气体,并生成NaVO3。写出化学方程式
②V2O5具有微弱的碱性,溶于强酸,当pH=1时生成淡黄色的VO2+的化学方程式
 还原为V3+
还原为V3+
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁的重要化合物高铁酸钠 Na2FeO4 是一种新型净水剂,具有消毒能力强、安全性好等优点。
(1)高铁酸钠生产方法之一是 Fe+2NaOH+2H2O Na2FeO4+3H2↑,该反应中还原剂是
Na2FeO4+3H2↑,该反应中还原剂是 ____________ (填化学式,下同),还原产物是___________ 。
(2)高铁酸钠生产方法之二是2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O,用双线桥表示该反应的电子转移的方向和数目:___________ 。
(3)高铁酸钠在水中可以发生如下反应 4FeO +10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有
+10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有________________ 性,而能够除去水中悬浮物是因为____________________ 。
(1)高铁酸钠生产方法之一是 Fe+2NaOH+2H2O
 Na2FeO4+3H2↑,该反应中还原剂是
Na2FeO4+3H2↑,该反应中还原剂是 (2)高铁酸钠生产方法之二是2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O,用双线桥表示该反应的电子转移的方向和数目:
(3)高铁酸钠在水中可以发生如下反应 4FeO
 +10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有
+10H2O = 4Fe(OH)3(胶体)+8OH–+3O2 ↑。 由此看来,高铁酸钠能够杀菌消毒是因为它具有
您最近一年使用:0次
【推荐3】一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
(2)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 :而中毒的事件,其原因是
:而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。下列也能实现这种转化的物质是___________ (填字母序号)。
A. B.
B. C.
C.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___________ 性。
(4)在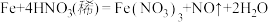 的反应中,
的反应中, 表现了
表现了___________ 性和___________ 性,每有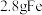 参加反应,转移电子数
参加反应,转移电子数___________ 个;生成的 (标准状况下)体积为
(标准状况下)体积为___________  。
。
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
(2)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 :而中毒的事件,其原因是
:而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有A.
 B.
B. C.
C.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在
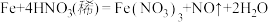 的反应中,
的反应中, 表现了
表现了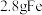 参加反应,转移电子数
参加反应,转移电子数 (标准状况下)体积为
(标准状况下)体积为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:_________________________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:__________________________ 。
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:__________________________ 。
(2)海水开发利用的部分过程如图所示:
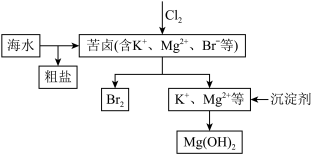
④向苦卤中通入氯气,发生反应的离子方程式是_____________________________________
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是______________________
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是_______ 。
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:
(2)海水开发利用的部分过程如图所示:

④向苦卤中通入氯气,发生反应的离子方程式是
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用
 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】NaCN超标的电镀废水可用两段氧化法处理:
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为___________ (选填“酸性”、“碱性”或“中性”);原因是___________ 。
(2)写出第二次氧化时发生反应的离子方程式。___________
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成___________ 、___________ 和H2O。
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为
(2)写出第二次氧化时发生反应的离子方程式。
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】完成下列反应的反应方程式:
(1)NaOH溶液吸收氯气的反应:____________________________
(2)铁与水蒸气在高温下的反应:____________________________
(3)氢氧化铁溶于盐酸:____________________________
(4)铝单质溶解在氢氧化钠溶液中:____________________________
(5)过氧化钠与二氧化碳反应:____________________________
(1)NaOH溶液吸收氯气的反应:
(2)铁与水蒸气在高温下的反应:
(3)氢氧化铁溶于盐酸:
(4)铝单质溶解在氢氧化钠溶液中:
(5)过氧化钠与二氧化碳反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】纳米硫化亚铁是一种很有潜在价值的新材料,值得深入研究。
1.关于铁元素的认识正确的是_________。
2.可用于检验FeSO4溶液是否变质的是_________。
3.高铁酸钠( Na2FeO4) 可用作净水剂,其原因是_________。
4.Fe、Co、Ni三种元素二价氧化物的晶胞类型相同,其熔点最高的是____ 。
A. FeO B. CoO C. NiO
纳米FeS可去除水中微量六价铬[Cr(Ⅵ)]。在pH=4~7的水溶液中,纳米FeS颗粒表面带正电荷,Cr(Ⅵ)主要以CrO 等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。
等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。
5.在弱酸性溶液中,反应FeS+H+ Fe2++HS-的平衡常数K的数值为
Fe2++HS-的平衡常数K的数值为____ 。
在pH=4~7溶液中,pH越大,FeS去除水中Cr(Ⅵ)的速率越慢,原因是____________ 。
6.FeS2的一种晶体与NaCl晶体的结构相似,该FeS2晶体的一个晶胞中S 的数目为_________。
的数目为_________。
7.在FeS2晶体中,每个S原子与三个Fe2+紧邻,且Fe—S间距相等,如图给出了FeS2晶胞中的Fe2+和位于晶胞体心的S (S
(S 中的S—S键位于晶胞体对角线上,晶胞中的其他S
中的S—S键位于晶胞体对角线上,晶胞中的其他S 已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来
已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来_________ 。

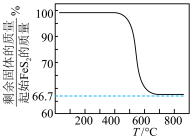
8.FeS2、FeS在空气中易被氧化。将FeS2在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS2的质量的比值随温度变化的曲线如图所示。800℃时,FeS2氧化成含有两种元素的固体产物_______ 。
1.关于铁元素的认识正确的是_________。
| A.能存在于人体的血红蛋白中 | B.是地壳中含量最多的金属元素 |
| C.单质是人类最早使用的金属 | D.铁的氧化物都具有致密的结构 |
| A.稀盐酸 | B.酚酞试液 | C.KSCN溶液 | D.苯酚 |
| A.能吸附水中杂质,氧化产物能消毒杀菌 |
| B.可消毒杀菌,氧化产物能吸附水中杂质 |
| C.能吸附水中杂质,还原产物能消毒杀菌 |
| D.可消毒杀菌,还原产物能吸附水中杂质 |
A. FeO B. CoO C. NiO
纳米FeS可去除水中微量六价铬[Cr(Ⅵ)]。在pH=4~7的水溶液中,纳米FeS颗粒表面带正电荷,Cr(Ⅵ)主要以CrO
 等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。
等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。5.在弱酸性溶液中,反应FeS+H+
 Fe2++HS-的平衡常数K的数值为
Fe2++HS-的平衡常数K的数值为在pH=4~7溶液中,pH越大,FeS去除水中Cr(Ⅵ)的速率越慢,原因是
6.FeS2的一种晶体与NaCl晶体的结构相似,该FeS2晶体的一个晶胞中S
 的数目为_________。
的数目为_________。| A.2 | B.4 | C.6 | D.8 |
 (S
(S 中的S—S键位于晶胞体对角线上,晶胞中的其他S
中的S—S键位于晶胞体对角线上,晶胞中的其他S 已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来
已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来
8.FeS2、FeS在空气中易被氧化。将FeS2在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS2的质量的比值随温度变化的曲线如图所示。800℃时,FeS2氧化成含有两种元素的固体产物

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】过去电子工业常用30%的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板,发生反应的化学方程式为:2FeCl3+Cu=2FeCl2+CuCl2。
(1)检验腐蚀后的溶液中是否含有Fe3+应选用的试剂是_________ ,该反应说明Fe3+氧化性比Cu2+氧化性_________ (填“强”或“弱” )。
(2)采用下列实验步骤从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液,其中步骤①中加过量的铁粉,③中加过量的盐酸,⑤中通入过量的氯气,请按要求填空。

C处物质的化学式为________ 分别写出步骤①、⑤中反应的离子方程式①_________ 、______ ⑤____
(1)检验腐蚀后的溶液中是否含有Fe3+应选用的试剂是
(2)采用下列实验步骤从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液,其中步骤①中加过量的铁粉,③中加过量的盐酸,⑤中通入过量的氯气,请按要求填空。

C处物质的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物与生产、生活关系密切
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为_______________ 。
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是____________ (用化学方程式表示)。
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤I若要检验是否有Fe3+生成,方法是_________________ 。
②步骤II中发生反应:4Fe(NO3)2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为____________ 。
③上述生产流程中,能体现“绿色化学”思想的是_____________ (任写一项)。
(4)Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4。
_____Fe2O3+ _____NaClO+ _____KOH _____K2FeO4(高铁酸钾)+ _____NaCl+ _____H2O
_____K2FeO4(高铁酸钾)+ _____NaCl+ _____H2O
①配平上述反应,并用单线桥法表示反应过程中转移电子数目和方向_____ 。此过程中氧化剂是______ (填化学式)。
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是_________ 、___________ 。
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤I若要检验是否有Fe3+生成,方法是
②步骤II中发生反应:4Fe(NO3)2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为
③上述生产流程中,能体现“绿色化学”思想的是
(4)Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4。
_____Fe2O3+ _____NaClO+ _____KOH
 _____K2FeO4(高铁酸钾)+ _____NaCl+ _____H2O
_____K2FeO4(高铁酸钾)+ _____NaCl+ _____H2O ①配平上述反应,并用单线桥法表示反应过程中转移电子数目和方向
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是
您最近一年使用:0次



