回答下列问题
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:_________________________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:__________________________ 。
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:__________________________ 。
(2)海水开发利用的部分过程如图所示:
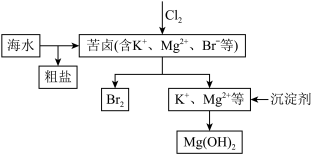
④向苦卤中通入氯气,发生反应的离子方程式是_____________________________________
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是______________________
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是_______ 。
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:
(2)海水开发利用的部分过程如图所示:

④向苦卤中通入氯气,发生反应的离子方程式是
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用
 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是
更新时间:2023/03/08 21:53:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某兴趣小组在两份相同的 Ba(OH)2溶液中,分别滴入相同浓度的 H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
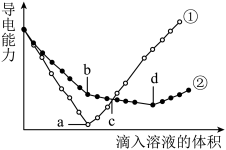
(1)图中①代表滴加_____ (填化学式)溶液的曲线。
(2)b点溶液中大量存在的离子是_____ 。
(3)曲线①中_____ 点对应的溶液呈中性(填a或c);曲线②中_____ 点对应的溶液中Ba2+恰好沉淀完全(填b或d)。
(4)写出bd段发生反应的离子方程式_____ 。
(5)下列说法不正确的是_____。

(1)图中①代表滴加
(2)b点溶液中大量存在的离子是
(3)曲线①中
(4)写出bd段发生反应的离子方程式
(5)下列说法不正确的是_____。
| A.曲线①中a点导电能力很差,说明生成物不是电解质 |
| B.曲线①、②中,c点溶液酸碱性不同 |
| C.曲线①、②对应的反应过程中均有白色沉淀产生 |
| D.曲线①中 ac段导电能力不断增大,主要是由于过量的 Ba(OH)2电离出的离子导电 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)按要求完成下列各题内容:
①NH4Cl的电子式:______ 。
②HClO的结构式:______ 。
③写出Cl-的结构示意图______ 。
④已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w克R2-所含有电子的物质的量是_____ 。
(2)写出下列符合要求的方程式:
①写出NaHSO4在水溶液中的电离方程式______ 。
②二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为______ 。
③金属铝和氢氧化钠溶液反应的化学方程式______ 。
(1)按要求完成下列各题内容:
①NH4Cl的电子式:
②HClO的结构式:
③写出Cl-的结构示意图
④已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w克R2-所含有电子的物质的量是
(2)写出下列符合要求的方程式:
①写出NaHSO4在水溶液中的电离方程式
②二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为
③金属铝和氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】沉淀的生成及转化在实际生产中有重要作用。
资料:部分难溶电解质的溶度积(均为18-25℃数据,单位省略)
(1)在粗盐提纯流程中,可用 溶液一次性除去粗盐水中的
溶液一次性除去粗盐水中的 和
和 ,反应的离子方程式是
,反应的离子方程式是___________ 。
(2)利用FeS作为沉淀剂除去某工业废水中 的部分流程如下:
的部分流程如下:
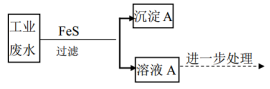
①结合化学用语,从平衡移动角度解释可用FeS除去 的原因
的原因___________ 。
②可使①中平衡发生移动所需最小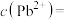
___________  。(只写计算结果)
。(只写计算结果)
③处理1L含 浓度为
浓度为 的该废水至合格(
的该废水至合格( 浓度小于1 mg/L)最少所需FeS的质量是
浓度小于1 mg/L)最少所需FeS的质量是___________ mg。
资料:部分难溶电解质的溶度积(均为18-25℃数据,单位省略)
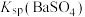 | 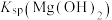 | 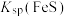 | 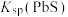 |
约为 | 约为 | 约为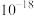 | 约为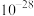 |
 溶液一次性除去粗盐水中的
溶液一次性除去粗盐水中的 和
和 ,反应的离子方程式是
,反应的离子方程式是(2)利用FeS作为沉淀剂除去某工业废水中
 的部分流程如下:
的部分流程如下:
①结合化学用语,从平衡移动角度解释可用FeS除去
 的原因
的原因②可使①中平衡发生移动所需最小
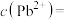
 。(只写计算结果)
。(只写计算结果)③处理1L含
 浓度为
浓度为 的该废水至合格(
的该废水至合格( 浓度小于1 mg/L)最少所需FeS的质量是
浓度小于1 mg/L)最少所需FeS的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】完成下列填空:
(1)+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。工业上常用Cl2处理含Fe2+的FeCl3溶液,请写出该反应的离子方程式:_______ 。
(2)2020年突如其来的“新冠肺炎”使人们认识到含氯消毒剂的重要性。
①“84”消毒液(有效成分为次氯酸钠)在此次抗疫中发挥了重要作用,其工业制备的化学方程式_______ 。
②已知KMnO4与浓盐酸反应也可以用来制取氯气:2KMnO4+16HCl=2KCl+ 2MnCl2+ 5Cl2↑+ 8H2O。氧化剂是_______ (填化学式);若有15.8g KMnO4参与反应,反应中转移的电子为_______ mol。请用单线桥法表示电子转移的方向和数目:_______ 。
(3)某实验小组用“套管实验”来探究Na2CO3和NaHCO3的性质。
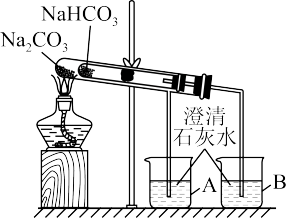
①整个实验过程中,能观察到烧杯B中的现象是_______ 。
②该实验可证明NaHCO3的热稳定性_______ (填“强于”“弱于”或“等于”)Na2CO3;_______ (填“能”或“不能”)将NaHCO3、Na2CO3的位置互换。
(1)+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。工业上常用Cl2处理含Fe2+的FeCl3溶液,请写出该反应的离子方程式:
(2)2020年突如其来的“新冠肺炎”使人们认识到含氯消毒剂的重要性。
①“84”消毒液(有效成分为次氯酸钠)在此次抗疫中发挥了重要作用,其工业制备的化学方程式
②已知KMnO4与浓盐酸反应也可以用来制取氯气:2KMnO4+16HCl=2KCl+ 2MnCl2+ 5Cl2↑+ 8H2O。氧化剂是
(3)某实验小组用“套管实验”来探究Na2CO3和NaHCO3的性质。

①整个实验过程中,能观察到烧杯B中的现象是
②该实验可证明NaHCO3的热稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上,我们用电解饱和食盐水制取氯气,请写出其中的化学方程式:_______ ,阳极产物是_______ 。实验室制备氯气时,为防止氯气污染空气,通常将氯气通入氢氧化钠溶液中,写出化学方程式:_______ ;对应的离子方程式_______ 。
您最近一年使用:0次
【推荐1】海洋是地球上最大的资源宝库,海水淡化及海水资源的综合利用具有重要意义。回答下列问题:
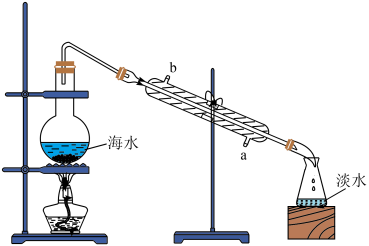
(1)用蒸馏法将海水淡化的装置如图,冷凝管的进水口是___________ (填“a”或“b”)。
(2)海水提溴技术涉及反应: 是利用了
是利用了 的
的___________ (填“氧化性”或“还原性”)。
(3)粗盐中常含有 、
、 、
、 等杂质离子,正确的除杂操作顺序为___________。
等杂质离子,正确的除杂操作顺序为___________。
①加入稍过量的 溶液;②加入稍过量的
溶液;②加入稍过量的 溶液;③加入适量的稀盐酸;④加入稍过量的
溶液;③加入适量的稀盐酸;④加入稍过量的 溶液;⑤过滤。
溶液;⑤过滤。
(4)用电解熔融氯化镁的方法可制取镁,该反应为___________ ;检验 溶液中是否含有
溶液中是否含有 残留的方法是
残留的方法是___________ 。

(1)用蒸馏法将海水淡化的装置如图,冷凝管的进水口是
(2)海水提溴技术涉及反应:
 是利用了
是利用了 的
的(3)粗盐中常含有
 、
、 、
、 等杂质离子,正确的除杂操作顺序为___________。
等杂质离子,正确的除杂操作顺序为___________。①加入稍过量的
 溶液;②加入稍过量的
溶液;②加入稍过量的 溶液;③加入适量的稀盐酸;④加入稍过量的
溶液;③加入适量的稀盐酸;④加入稍过量的 溶液;⑤过滤。
溶液;⑤过滤。| A.④①②③⑤ | B.②①④⑤③ | C.①②⑤③④ | D.①④②⑤③ |
 溶液中是否含有
溶液中是否含有 残留的方法是
残留的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面。
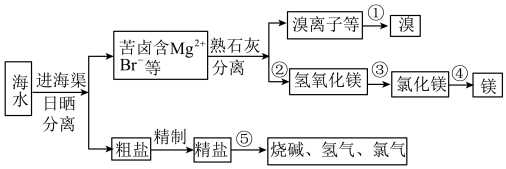
请回答下列问题:
(1)①步主要反应的的离子方程式:_____________________________ 。
(2)分离出氢氧化镁的操作为__________ ,第③步需要加入_________ 。
(3)将粗食盐中含有的Mg2+、Ca2+和SO 等杂质除去,加入的试剂有(按加入顺序填入)
等杂质除去,加入的试剂有(按加入顺序填入)___________ (只要求填一组合理的答案即可)。
(4)⑤产物氢气在__________ 极生成,若电解食盐水时消耗NaCl的质量为234g,则在理论上最多可得氯气的体积为_______________ 升(标准状况)。

请回答下列问题:
(1)①步主要反应的的离子方程式:
(2)分离出氢氧化镁的操作为
(3)将粗食盐中含有的Mg2+、Ca2+和SO
 等杂质除去,加入的试剂有(按加入顺序填入)
等杂质除去,加入的试剂有(按加入顺序填入)(4)⑤产物氢气在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海水中有非常丰富的化学资源,从海水中可提取多种化工原料。某工厂对海水资源综合开发利用的部分工艺流程如图所示,回答下列问题
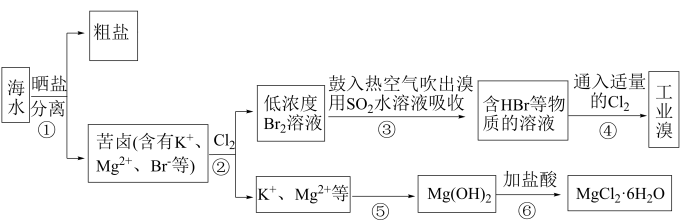
(1)海水中的镁、溴、碘元素都处于_______ (填“化合”或“游离”)态。
(2)步骤②④中通入Cl2,能制得单质溴,说明Cl2的氧化性比Br2_______ (填“强”或“弱”),发生反应的离子方程式为_______ 。
(3)步骤③中鼓入热空气分离出 Br2,利用了Br2的_______ 性。
(4)步骤③中发生反应的离子方程式为_______ ,当转移3.01×1023个电子时,吸收 Br2的物质的量为_______ moL。
(5)步骤⑤中加入的物质是_______ (填物质名称)。

(1)海水中的镁、溴、碘元素都处于
(2)步骤②④中通入Cl2,能制得单质溴,说明Cl2的氧化性比Br2
(3)步骤③中鼓入热空气分离出 Br2,利用了Br2的
(4)步骤③中发生反应的离子方程式为
(5)步骤⑤中加入的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】海洋是一个巨大的物质资源和能量宝库,世界各国都在研究如何充分利用海洋资源。
Ⅰ. 从海水中可以提取食盐。
Ⅱ.从海水中提取镁。已知MgO、MgCl2的熔点分别为2800℃、604℃,从海水中提
取镁,最合理的方法是_____ 。
Ⅲ.从海水中提溴。其工业方法有:空气吹出纯碱吸收法、空气吹出SO2吸收法、溶
剂萃取法等。
(1)空气吹出纯碱吸收法。将氯气通入富含溴离子的海水中,再用空气将溴吹出,
用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及的反应有:
①______________________________ (写出离子方程式);
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3CO2↑;
③BrO3﹣+5Br﹣+6H+═3Br2+3H2O
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,
然后再用氯气氧化即得单质溴。
写出溴与二氧化硫反应的化学方程式:_____________________________ 。
Ⅰ. 从海水中可以提取食盐。
Ⅱ.从海水中提取镁。已知MgO、MgCl2的熔点分别为2800℃、604℃,从海水中提
取镁,最合理的方法是
A.海水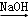 Mg(OH)2 Mg(OH)2 Mg Mg |
B.海水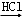 MgCl2溶液→MgCl2熔融 MgCl2溶液→MgCl2熔融 Mg Mg |
C.海水 Mg(OH)2 Mg(OH)2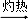 MgO MgO Mg Mg |
D.海水 Mg(OH)2 Mg(OH)2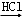 MgCl2溶液→MgCl2熔融 MgCl2溶液→MgCl2熔融 Mg Mg |
Ⅲ.从海水中提溴。其工业方法有:空气吹出纯碱吸收法、空气吹出SO2吸收法、溶
剂萃取法等。
(1)空气吹出纯碱吸收法。将氯气通入富含溴离子的海水中,再用空气将溴吹出,
用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及的反应有:
①
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3CO2↑;
③BrO3﹣+5Br﹣+6H+═3Br2+3H2O
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,
然后再用氯气氧化即得单质溴。
写出溴与二氧化硫反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是_________ 。(填“游离态”或“化合态”)
②下列物质不经过化学变化就能从海水中获得的是______ 。(填字母)
A.单质钠 B.单质钾 C.氯化钠
③目前化学工业的主要支柱之一是氯碱工业,它是以电解_______ 为基础制取氯气等产品的工业。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①工业上制造光导纤维的基本原料是_______ 。
②下列物质中,不能用来制造耐火材料的是_______ 。(填字母)
A.氧化镁 B.三氧化二铝 C.过氧化钠
③在生铁和钢这2种金属材料中,含碳量较高的是_______ 。
(3)保持洁净安全的生存环境已成为全人类的共识。
①pH<_______ 的雨水称为酸雨。
②下列物质中,会破坏臭氧层的是_______ 。(填字母)
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3 +3Cl2=6HCl + N2,则如果氯气管道某处漏气,用该方法检查时的现象是______ 。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是
②下列物质不经过化学变化就能从海水中获得的是
A.单质钠 B.单质钾 C.氯化钠
③目前化学工业的主要支柱之一是氯碱工业,它是以电解
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①工业上制造光导纤维的基本原料是
②下列物质中,不能用来制造耐火材料的是
A.氧化镁 B.三氧化二铝 C.过氧化钠
③在生铁和钢这2种金属材料中,含碳量较高的是
(3)保持洁净安全的生存环境已成为全人类的共识。
①pH<
②下列物质中,会破坏臭氧层的是
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3 +3Cl2=6HCl + N2,则如果氯气管道某处漏气,用该方法检查时的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海洋资源和新型燃料电池的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是______ (填写字母)。
A. B.淡水 C.烧碱 D.食盐
B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是______ 。
(3)下圈是从海水中提取镁的简单流程。
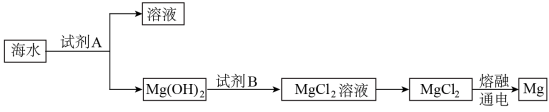
工业上常用于沉淀 的试剂
的试剂 是
是______ , 转化为
转化为 的离子方程式是
的离子方程式是______ 。
(4)海带灰中富含以碘离子形式存在的碘元素。 实验室提取 的途径如下所示,
的途径如下所示,
干海带 海带灰
海带灰 滤液
滤液
 I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ 。
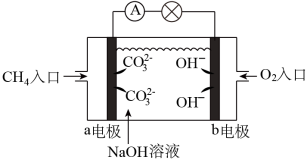
(5)甲烷燃料电池应用十分广泛。如下图,甲烷通入的一极的电极反应式为:______ ;当电路中累计有 电子通过时,消耗的氧气体积为
电子通过时,消耗的氧气体积为______  (在标准状况下)。
(在标准状况下)。
(1)无需经过化学变化就能从海水中获得的物质是
A.
 B.淡水 C.烧碱 D.食盐
B.淡水 C.烧碱 D.食盐(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
(3)下圈是从海水中提取镁的简单流程。

工业上常用于沉淀
 的试剂
的试剂 是
是 转化为
转化为 的离子方程式是
的离子方程式是(4)海带灰中富含以碘离子形式存在的碘元素。 实验室提取
 的途径如下所示,
的途径如下所示,干海带
 海带灰
海带灰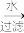 滤液
滤液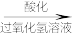
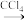
 I2
I2①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
(5)甲烷燃料电池应用十分广泛。如下图,甲烷通入的一极的电极反应式为:
 电子通过时,消耗的氧气体积为
电子通过时,消耗的氧气体积为 (在标准状况下)。
(在标准状况下)。
您最近一年使用:0次



